微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某种牙膏中的摩擦剂是碳酸钙,可以用石灰石(含杂质SiO 2)来制备。某同学甲设计了一种制备碳酸钙的方案,其流程图为:
2)来制备。某同学甲设计了一种制备碳酸钙的方案,其流程图为:

请回答下列问题:
(1)假设第①步反应完全进行,则第②步反应过滤后得到的滤渣的成分为?。
(2)第③步反应不使用CO2,其主要原因是(用离子方程式表示)?
?。
(3)第③步反应使用Na2CO3而不使用NaHCO3,从提高企业经济效益的角度考虑,其原因是?。
(4)某同学乙用石灰石为原料(其他试剂自选),设计了另一种制备碳酸钙的实验方案,请你完成他的实验方案。

乙同学所设计的方案的优点是?。
参考答案:(1)CaSiO3(1分)?
(2)Ca2++2OH- ="===" CaCO3↓+H2O
CaCO3+CO2+H2O ="===" Ca2++2HCO3-(2分)?
(3)生成等质量的CaCO3消耗NaHCO3多于Na2CO3;使用Na2CO3可制取副产品NaOH(答一条合理即可,1 分)?
分)?
(4)①稀盐酸(1分)?CaCl2 (1分)
△========
本题解析:略
本题难度:一般
2、选择题 在实验室进行物质制备,下列从原料及试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是( )
A.C
COCO2Na2CO3
B.CuCu(NO3)2 溶液Cu(OH)
C.FeFe2O3Fe2(SO4)3溶液
D.CaOCa(OH)2溶液NaOH溶
参考答案:A、碳不完全燃烧可生成一氧化碳,一氧化碳高温下与氧化铜反应生成铜和二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠;理论上正确,一氧化碳是有毒的气体,碳在氧气中燃烧生成的进行实验时要进行尾气处理,且一氧化碳是可燃性气体,不纯时加热或点燃引起爆炸,操作上较为复杂,故A错误;
B、铜与硝酸银反应可生成硝酸铜,硝酸铜与氢氧化钠可生成氢氧化铜沉淀;理论上正确,操作上也较简便,银比铜要贵重,利用硝酸银、氢氧化钠制取氢氧化铜,经济上不合理,故B错误;
C、铁在氧气中燃烧生成四氧化三铁而不能生成三氧化二铁,因此该方案在理论上就是错误的,故C错误;
D、氧化钙与水反应可生成氢氧化钙,氢氧化钙与碳酸钠反应可生成氢氧化钠;理论上正确,操作也只需要加入液体较为简便,利用碳酸钠获得氢氧化钠,经济上也合理,故D正确.
故选:D.
本题解析:
本题难度:一般
3、填空题 2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的,回收利用锂资源成为重要课题.某研究小组对某废旧锂离子电池正极材料(图中简称废料,成份为LiMn2O4、石墨粉和铝箔)进行回收研究,工艺流程如下:
已知:Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g.
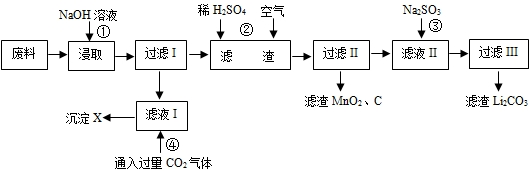
(1)废料在用NaOH溶液浸取之前需要进行粉碎操作,其目的是______.
(2)废旧电池可能由于放电不完全而残留有锂单质,为了安全对拆解环境的要求______.
(3)写出反应④生成沉淀X的离子方程式:______.
(4)己知LiMn2O4中Mn的化合价为+3和+4价,写出反应②的化学反应方程式:______.
(5)生成Li2CO3的化学反应方程式为______.已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应______.
参考答案:第一步就是铝溶解在氢氧化钠溶液中(注意LiMn2O4不溶于水)生成四羟基合铝酸钠,即滤液的主要成分,第二步就是四羟基合铝酸钠与二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠的过程,第三步是LiMn2O4在酸性环境下能被空气中的氧气氧化发生的氧化还原反应,得到的滤液中有生成的硫酸锂,可能有过量的硫酸,最后一步加入碳酸钠之后所得的滤液主要成分为硫酸钠;
(1)粉碎废料,能增大废料与氢氧化钠溶液的接触面积,加快反应速率,故答案为:增大接触面积,加快反应速率.
(2)金属锂性质活泼,易与氧气、水发生反应,故答案为:隔绝空气和水分;
(3)四羟基合铝酸钠与过量二氧化碳反应得产物是Al(OH)3沉淀和碳酸氢钠,所以离子方程式为CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-,
故答案为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3-.
(4)在酸性环境下,LiMn2O4能被空气中的氧气氧化,生成二氧化锰、硫酸锂和水,所以化学方程式为:4LiMn2O4+2H2SO4+O2=8MnO2+2Li2SO4+2H2O,
故答案为:4LiMn2O4+2H2SO4+O2=8MnO2+2Li2SO4+2H2O;
(5)硫酸锂和碳酸钠反应生成硫酸钠和碳酸锂沉淀,化学反应方程式为:Li2SO4+Na2CO3=Na2SO4+Li2CO3↓;Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应趁热过滤,
故答案为:Li2SO4+Na2CO3=Na2SO4+Li2CO3↓;趁热过滤.
本题解析:
本题难度:一般
4、实验题 某研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的性质和用途,进行了如图所示实验:
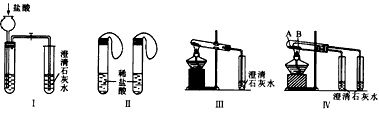
(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是____ ,实验现象是___________________。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)_________。其中能够说明泡沫灭火器中选择碳酸氢钠与酸反应制CO2而不选择碳酸钠的实验是_____________。
(3)若测定Na2CO3固体中混有的少量NaHCO3。的质量分数,Ⅲ能否达到实验目的?若能,请说明其计算所需的数据___________;若不能,请简要说明理由________。
参考答案:(1) NaHCO3;左边试管中的石灰水变浑浊
(2)Ⅱ、Ⅲ、Ⅳ;Ⅱ
(3)能;固体样品的质量和沉淀总质量(或反应前后固体的质量)
本题解析:
本题难度:一般
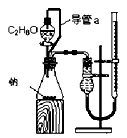
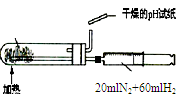
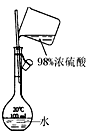
5、选择题 下列实验装置设计正确,且能达到目的的是
| 
| 
| 
|
A.测定乙醇分子结构
| B.合成氨并检验氨的生成并回收CCl4
| C.碘的CCl4溶液中分离I2
| D.配制稀硫酸溶液
|
?
参考答案:A
本题解析:A、装置中左边是反应装置,右边是量气装置,正确;B、应用湿润的红色石蕊试纸或pH试纸检验氨气,错误;C、蒸馏操作中应把温度计的水银球放在蒸馏烧瓶的支管口处测定出去气体的温度,错误;D、浓硫酸溶解放出大量热,不能直接在容量瓶中稀释,错误。
本题难度:一般