��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��20�֣�
�� �������й�SO2��Cl2������ʵ�顣
(1)ijС�������ͼ��ʾ��װ��ͼ��ͼ�мгֺͼ���װ����ȥ�����ֱ��о�SO2��Cl2�����ʡ�

��?������˷ֱ�ͨ ��SO2��Cl2��װ��A�й۲쵽�������Ƿ���ͬ��?(���ͬ������ͬ��)����װ��D��װ��
��SO2��Cl2��װ��A�й۲쵽�������Ƿ���ͬ��?(���ͬ������ͬ��)����װ��D��װ�� ��V2O5(����)��ͨ��SO2ʱ����Kͨ������O2�Ļ�ѧ��Ӧ����ʽΪ?��
��V2O5(����)��ͨ��SO2ʱ����Kͨ������O2�Ļ�ѧ��Ӧ����ʽΪ?��
��SO2ͨ��B�У���Һ��ɫ��ȥ����÷�Ӧ�����ӷ���ʽΪ?��
(2) ijͬѧ��������SO2ͨ��һ֧װ���Ȼ�����Һ���Թܣ�δ���������ɣ�������Թ��м�������(����ĸ)?����Ȼ���۲쵽����������
A����ˮ? B��ϡ�� ��? C���������
��? C��������� Һ? D��������Һ
Һ? D��������Һ
(3)����Ԫ��S��O��ɨC2���������X��X��S��O��������Ϊ4��3����Cl2�뺬X����Һ��ȫ��Ӧ�ó�����Һ��ȡ��������Һ���������ữ���Ȼ�����Һ���а�ɫ����������д��C l2�뺬X����Һ��Ӧ�����ӷ���ʽ?��
l2�뺬X����Һ��Ӧ�����ӷ���ʽ?��

(4)ij���е�λ���õ绯ѧԭ����SO2���Ʊ����ᣬװ������ͼ������ij�ִ������缫Ϊ��IJ��ϣ����������壬ͬʱҲ��ʹ������������Һ��ֽӴ���ͨ��SO2�ĵ缫Ϊ_________������缫��ӦʽΪ?����ص��ܷ�Ӧʽ ?
?
�� ʵ���ǻ�ѧ�о��Ļ������������и�װ��ͼ��������ȷ����?������ţ�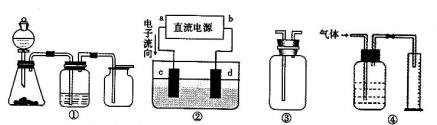
A��װ�âٿ���ɶ�������ķ������������ռ�����ͭм��ϡ���ᷴӦ
B��װ�â��� ��aΪ���⣬dΪ����
��aΪ���⣬dΪ����
C��װ�âۿ������ռ�H 2��NH3��Cl2,��HCl��NO2��
2��NH3��Cl2,��HCl��NO2��
D ��װ�â������ڲ����������
��װ�â������ڲ����������
��?��Ǧ���ص���±ˮ����Cl-��Br-��Na+��Mg2+����װ����ͼ��ʾ��a��bΪʯī�缫��������˵������ȷ����?������ţ�
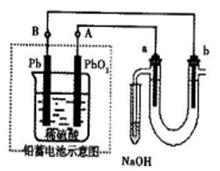
A��Ǧ���ظ����ķ�ӦʽΪ��Pb��2e-=Pb2+
B��Ǧ���طŵ�ʱ��B���������ᣬA����������
C��Ǧ���س��ʱ��A��Ӧ�����Դ��������
D������±ˮʱ��a�缫���ȷŵ����Br-
�ο��𰸣���20�֣��� (1) ����ͬ? 2SO2 + O2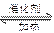 2SO3
2SO3
��SO2 + I2 + 2H2O = 4H��+ 2I��+ SO42��? ��NaOH������������Ҳ�ɣ�
(2) B? (3) 4Cl2 + S2O32��+ 5H2O = 2SO42��+ 8Cl��+ 10H��
(4) ��? SO2 �C 2e��+ 2H2O = 4H��+ SO42��? 2SO2 + O2 + 2H2O = 2H2SO4
��ÿ������ʽ2�֣�����ÿ��1�֣��� C (3 ��)? ��? D(3��)
�����������
�����Ѷȣ�һ��
2��ʵ���� ��12�֣�ij�о���С����0.20 mol/L NaOH��Һ�ζ�δ֪Ũ�ȵİ״ף�ָʾ��Ϊ��̪����
��ش�
��1����ͼ��ʾ50 ml�ζ�����Һ���λ�ã���A��C�̶ȼ����1ml��A���Ŀ̶�Ϊ20����ʱ�ζ�����Һ������??mL��
��2���ζ������У��۾�ʼ��ע�� ?��ֱ����ƿ��Һ�����ɫ������
 ?
?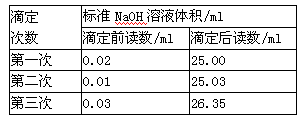
��3��ͬѧ�ǽ���������ʵ�飬ÿ��ȡ�״� 20.00 ml�� ʵ������¼���ϱ��������״����ʵ���Ũ��Ϊ_________?��������λ��Ч���֣���
��4������ʱ�ð״���ϴ��ƿ���Եζ����������Ӱ����________���ƫ��ƫС������Ӱ�족����ͬ�������ð״���ϴ��ʽ�ζ��ܣ��Եζ����������Ӱ����?��
��5�����ζ��յ�ʱ���pH=7����������Ũ�ȵıȽ���ȷ����?��
A��c��Na+����c��CH3COO����
B��c��Na+����c��CH3COO����
C��c��Na+��=c��CH3COO����
D������ȷ��
�ο��𰸣���12�֣���1����29.60Ml?��2����ƿ��Һ����ɫ�ı仯
��3��0.25 mol/L?��4��ƫ��?��Ӱ��?��5��C
�����������1���ζ��ܵĿ̶����϶�����������ģ�����ȷ������0.1ml�����Ը���ͼ�п̶��ߵ�λ�ÿ�֪����ʱ�ζ�����Һ����������50.00ml��20.40ml��29.60ml��
��2���ζ������У��۾�ʼ��ע����ƿ��Һ����ɫ�ı仯��ֱ����ƿ��Һ�����ɫ�����仯��
��3�����ݱ������ݿ�֪������ʵ������������������Һ������ֱ���24.98ml��25.02mol��26.32ml����Ȼ�����ε�ʵ�����̫����ȥ����ʵ����������������Һ�����ƽ��ֵ�ǣ�24.98ml��25.02mol����2��25.00ml�����״����ʵ���Ũ���� ��
��
��4������ʱ�ð״���ϴ��ƿ������������������Һ��������ӣ���ζ����ƫ�����ð״���ϴ��ʽ�ζ��ܣ���ⶨ�����Ӱ�졣
��5�����ݵ���غ��֪c��Na+��+c��H+��=c��OH����+c��CH3COO������������Һ�����ԣ���c��H+��=c��OH����������c��Na+��=c��CH3COO��������ѡC��
�������������е��Ѷȵ����⣬���������ǿ���������У������߿���������ע�ض�ѧ��������֪ʶ������ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ�������������������Ӧ��������������ѵ�����������������Ũ�ȴ�С�Ƚϡ�
�����Ѷȣ�һ��
3������� 1��2��3��4-���⻯���Ľṹ��ʽ��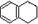 ������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�
������ʽ��C10H12��������Ϊ��ɫҺ�壬�д̼�����ζ���е�207�棬������ˮ����һ���������ܼ�������Һ�巢����Ӧ��C10H12+4Br2��C10H8Br4+4HBr�����ɵ����廯��������Ϊ��̬��������ˮ�����������⻯����Һ�塢����ˮ�ʹ�����Ϊԭ�ϣ��Ʊ�����������������Һ��ʵ�鲽�����£�

�ٰ�һ�������Ȱ����⻯����ˮ�����ʵ��������У��������������ۣ�
����������Һ�壬���Ͻ��裬ֱ����Ӧ��ȫ��
��ȡ�·�Ӧ�����������������⻯����ֱ����Һ��ɫ��ʧ�����ˣ�����Һ�����Һ©�������ã�
�ܷ�Һ���õ��ġ�ˮ�㡱����������Һ���ش��������⣺
��1������ͼ��ʾ��װ�ã��ʺϲ���ٺ͢ڵIJ�������______��
��2��������в����������⻯����Ŀ����______��
��3��������й��˺�õ��Ĺ���������______��
��4���ڢܻ�õ�Ũ��Һ�м����Ҵ������ȣ��ɻ��һ�ֲ�����ˮ���л��д���÷�Ӧ�ķ���ʽ______��ʵ������ȡ��Ȳ������ͼ�е�װ��D����ʱ��Һ©���е�Һ��ͨ����______��
��5����Ȳ�ܱ����Ը��������Һ����������ƽ����Ӧ�ķ���ʽ��
______C2H2+______KMnO4+______H2SO4=______K2SO4+______MnSO4+______CO2+______H2O��
�ο��𰸣���1�����ղ���٣���ʵ���ǰ����⻯����ˮ�����ۼ���ͬһ�����з�Ӧ������B����ȷ������A�е�װ�ý��з�Ӧ���������ʹ̼�����ζ�����⻯��������Ⱦ������ͬ��Cװ���ڲ���ڷ�Ӧʱ��Ҳ����ɻ�����Ⱦ������A��C�����ԣ���ѡDװ�ã�
�ʴ�Ϊ��D��
��2�����ڲ���ڼ����˹�����Һ�壬������в����������⻯������ʣ����嵥�ʣ�
�ʴ�Ϊ����Ӧ�������Br2��
��3���������ɵ����廯��������Ϊ��̬�����Թ��˺�õ��Ĺ������������廯�������ۣ�
�ʴ�Ϊ�����廯�������ۣ�
��4���ڢܻ�õ�Ũ��Һ�к����廯�⣬�廯�����Ҵ��ڼ������������������飬��Ӧ�ķ���ʽΪ��CH3CH2OH+HBr��
���������
�����Ѷȣ�һ��
4������� ��12�֣�����ij��ȤС��Ϊ��֤�ճ������õĻ��ͷ�Ϻ���KClO3��MnO2��S�����ʣ����������ʵ������ͼ��
��ش��������⣺
��1��Ϊ��֤����A������ͼ��ʾװ�ý���ʵ�飺���ܹ۲쵽���Ը��������Һ��ɫ������֤�����ͷ�Ϻ���SԪ�أ���д������Aʹ���Ը��������Һ��ɫ�����ӷ���ʽ?��
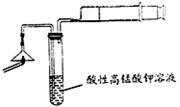
��2������ڵ�ʵ�����װ������ͼ��ʾ���ò�����������?�����ŵ���?��
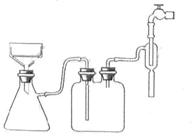
��3��ָ��ͼ�еĴ���
�����?��
�����?��
�����?��
���м�������д��������һ��Ҫ������
����������������ijЩ��Ҫ�ɷֵļ����ʵ������ͼ
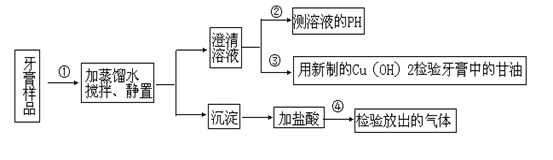
��1����������ʵ��˵������ȷ���ǣ�
A���ڢ��У�����������������Һ�ͳ�����
B���ڢ��У����PH��7������������ɷ���NaFˮ������ģ�
C���ڢ��У�������Cu(OH)2�����������ɫ������
D���ڢ��У��ų�������ͨ������ʯ��ˮ��һ�����ֳ�����