微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业上为从4J29合金(铁钴镍合金)废料中提取钴和镍,一般先用硫酸溶解合金,使其转化为Fe2+、Co2+、Ni2+,再把Fe2+氧化为Fe3+,从而使Fe3+转化为某种沉淀析出,达到与Ni2+、Co2+分离的目的.生产上要使Fe2+氧化为Fe3+,而不使Co2+、Ni2+氧化的试剂是NaClO或NaClO3(均含少量H2SO4)溶液.反应的部分化学方程式如下(A为还原剂):?
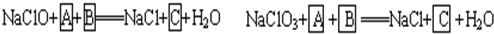
试回答下列问题:
(1)上述反应中,A为:______(写化学式,下同),C为:______.
(2)配平下列离子方程式:?
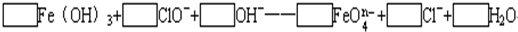
(3)已知有3.21g?Fe(OH)3参加反应,共转移了5.42×1022个电子,则n=______,FeO
中铁的化合价为______.
(4)根据(2)、(3)推测FeO能与下列哪些物质反应(只填序号)______.
A.Cl2?B.SO2C.H2S?D.O2?
2、选择题 实现下列变化,一定要加入氧化剂的是
A.HCl→Cl2
B.Na2SO3→SO2
C.HCl→H2
D.HNO3→NO
3、选择题 氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,下列说法正确的是(? )
A.由反应可知,氧气、氯气均为氧化产物
B.若化学计量数a=8,则该反应转移电子数为12e-
C.若b确定,则方程式中其他物质的化学计量数均能确定
D.若氯酸分解所得混合气体,1 mol混合气体质量为51.5 g,则反应方程式可表示为:5HClO3=O2↑+Cl2↑+3HClO4+H2O
4、填空题 (3分)工业上冶炼金属铁的主要反应为:Fe2O3 + xCO 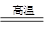 2Fe + 3CO2
2Fe + 3CO2
其中该化学方程式中x的数值是?, CO作?(填“氧化剂”或“还原剂”)。在该反应中,若消耗了1 mol Fe2O3,则生成?mol Fe。
5、计算题 将25.6g铜与含0.3molH2SO4的浓硫酸充分反应,(1)若在反应过程中消耗了0.2mol的H2SO4,则生成的气体标况下体积为多少?(2)若以上反应产生的气体全部逸出后,继续在剩余物质中加入2mol/L的稀硝酸100ml,充分反应后产生NO的物质的量为多少?