��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����ս̰滯ѧ1��75ҳ�ϡ����������Խ������������������ᡢ����ͭ��Һ�ȣ���Ӧת��Ϊ+2�����Ļ��������������Խ�ǿ������������������˫��ˮ�ȣ���Ӧ��ת��Ϊ+3�۵Ļ��������������ѧ�о���ѧϰС����ͨ������ʵ��̽�������ƵĻ�ԭ�����ۺ�����ķ�Ӧ���������������������̽�����ش��й����⣺
��1������KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽����������______������ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ����______��ѧ������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�д������������Ļ�ѧ����ʽ��______��
��2�������Ͻ��ܡ�ȡ������ӦҺ�������������ȵμ��������Ʊ�����ˮ��Ȼ��μ�KSCN��Һ������Ѫ��ɫ�����ٵμӹ���������ˮ��ȴ���ֺ�ɫ��ȥ��ͬѧ�Ժ�ɫ��ȥ��ԭ��������Եļ��裮ijͬѧ�ļ����ǣ���Һ�е�+3����������Ϊ���ߵļ�̬�������+3����������ΪFeO42-����д���÷�Ӧ�����ӷ���ʽ______��
��3��̽��������ص�ij�����ʣ�
��ʵ��һ��������K2FeO4����ֱ��ܽ���pH?Ϊ?4.74��7.00��11.50?��ˮ��Һ�У����FeO42-Ũ��Ϊ?1.0mmol?L-1��1mmol?L-1=10-3mol?L-1�������������ã����첻ͬ��ʼ?pH?��ˮ��Һ��K2FeO4ij�����ʵ�Ӱ�죬�����ͼ1��ע��800min��������Һ�и�����ص�Ũ�Ȳ��ٸı䣩��


���������������?K2FeO4�ܽ���pH=4.74?��ˮ��Һ�У����Ƴ�FeO42-Ũ��Ϊ?1.0mmol?L-1?���������������ֱ�����?20�桢30�桢40���?60��ĺ���ˮԡ�У����첻ͬ�¶ȶ�K2FeO4ij�����ʵ�Ӱ�죬�����ͼ2����
��ʵ��1��Ŀ����______��
��ʵ��2�ɵó��Ľ�����______��
�۸��������ˮ�еķ�ӦΪ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2������ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���Ҫԭ����______��
�ο��𰸣���1�����������Ӿ��л�ԭ�ԣ���������KSCN��Һ��Ѫ��ɫ����KSCN��H2O2��ҩƷ���鷴Ӧ��Ļ��Һ�к��ж�������ʵ�鷽�����������ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ����ʵ���������ֿ�����ɫѸ����ȥ��ͬʱ��Һ�ʻ�ɫ������ܵ�ԭ�������������������ʵ��ʱ�����μ�˫��ˮ��Ũ�ȹ����߹�����������Ѹ�ٲ����������ݣ�����2H2O2?FeCl3?.?2H2O+O2����
�ʴ�Ϊ���ȼ����軯����Һ���������ٵμ�˫��ˮ������������Һ��Ѫ��ɫ���������������2H2O2?FeCl3?.?2H2O+O2����
��2������Ϣ��֪�������ӱ���������ΪFeO42-�����ᣬ�����ӷ�ӦΪ2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
�ʴ�Ϊ��2Fe3++3Cl2+8H2O�T2FeO42-+6Cl-+16H+��
��3������ʵ��һ��֪��pH��ͬ��FeO42-�ȶ��Բ�ͬ����ʵ��1��Ŀ��Ϊ�о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
�ʴ�Ϊ���о�FeO42-�ڲ�ͬpH��Һ�е��ȶ��ԣ���Ӧ�����ʣ���
����ͼ2��֪���¶Ȳ�ͬ��FeO42-�ȶ��Բ�ͬ������ʵ��2�ɵó��Ľ������¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
�ʴ�Ϊ���¶�Խ�ߣ�FeO42-Խ���ȶ�������ˮ��Ӧ������Խ�죩��
����ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���pH=11.50����Һ��OH-����Ũ�ȴ�ʹ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2��ƽ�������ƶ���
�ʴ�Ϊ��pH=11.50����Һ��OH-����Ũ�ȴ�ʹƽ�������ƶ���
���������
�����Ѷȣ�һ��
2��ѡ���� �����������Ⱥ��ȶ�������ǣ�������
A��FeO
B��NaHCO3
C��Al��OH��3
D��Na2CO3
�ο��𰸣�D
���������
�����Ѷȣ���
3������� ������ҵ�Դٽ����ú���ᷢչ������Ҫ���á�



 ��1��������¯��Ϊ�岿�֣�����ʯ�����ú����Ҫ��?���ַ�����Ӧ����?���ֿ�ʼ��������¯����
��1��������¯��Ϊ�岿�֣�����ʯ�����ú����Ҫ��?���ַ�����Ӧ����?���ֿ�ʼ��������¯����
 ��2������ʱ�����Ļ�ѧ����ʽΪ?��
��2������ʱ�����Ļ�ѧ����ʽΪ?��
 ����衢�̺�����Ŀ����?��
����衢�̺�����Ŀ����?��
 ��3������ֺ��е�CrԪ���������ֹ��̵�����?���ǰ�������룬ԭ����?��
��3������ֺ��е�CrԪ���������ֹ��̵�����?���ǰ�������룬ԭ����?��
 ��4�����������������У�β�������е���Ҫ��Ⱦ����?��
��4�����������������У�β�������е���Ҫ��Ⱦ����?��
 �ӻ����;��ýǶȿ��ǣ�����β��������������?��
�ӻ����;��ýǶȿ��ǣ�����β��������������?��
�ο��𰸣���1��¯��?¯��

 ��2��2P+5FeO+3CaO? Ca3(PO4)2+5Fe?�����͵����ֵijɷ�
��2��2P+5FeO+3CaO? Ca3(PO4)2+5Fe?�����͵����ֵijɷ�
 ��3����?����Cr��������������ǰ����Cr���γ�¯������ȥ����
��3����?����Cr��������������ǰ����Cr���γ�¯������ȥ����
 ��4��CO?ȼ�ϣ���ԭ����
��4��CO?ȼ�ϣ���ԭ����
��������� ��1����¯����������ʯ����Ҫ��Ӧ����¯�����ַ�������¯��������������¯����
��1����¯����������ʯ����Ҫ��Ӧ����¯�����ַ�������¯��������������¯����

 ��2�������е��Ļ�ѧ����ʽΪ2P+5FeO+3CaO? Ca3��PO4��2+5Fe������衢�̺�����Ŀ������ȥ���͵������еijɷ֡�
��2�������е��Ļ�ѧ����ʽΪ2P+5FeO+3CaO? Ca3��PO4��2+5Fe������衢�̺�����Ŀ������ȥ���͵������еijɷ֡�
 ��3��Ϊ�˷�ֹCrԪ�ر������µ���������Ӧ����������롣
��3��Ϊ�˷�ֹCrԪ�ر������µ���������Ӧ����������롣



 ��4������ʱ�õ�C��ȼ������CO����ԭ��������ʱ���б�������C����˶���CO��������CO���ж����壬�Ի�������Ⱦ��ͬʱCO����ȼ������CO2��
��4������ʱ�õ�C��ȼ������CO����ԭ��������ʱ���б�������C����˶���CO��������CO���ж����壬�Ի�������Ⱦ��ͬʱCO����ȼ������CO2��
�����Ѷȣ�һ��
4������� ��1.000gFeC2O4��2H20������Ʒ�������ط������н������ط������y�������ط������ߣ���Ʒ�������¶ȱ仯�����ߣ�����ͼ��ʾ��
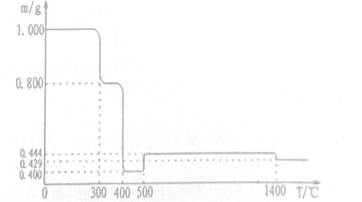
��֪���ٲ��������ȷֽ��ų�̼���������5000C֮ǰ�������ط����ǵ���Ʒ�ش���Ar�������У�5000Cʱ����Ʒ���������ͨ�����������գ�
(1)3000Cʱ����Ʒ��ˮ�Ĺ��̣���ȷ��3500Cʱ��Ʒ�Ƿ���ˮ��ȫ_____ (���"������жϵ�������____(Ҫ��д��������̣���
(2 ) 4000Cʱ�����仯�Ļ�ѧ����ʽ��_______��
(3) ��6000Cʱ��Ʒ���в����Ĺ������������ȴ�����£�����ù����м���һ������ϡ����պ���ȫ�ܽ⣬��pH��ֽ���������Һ��PH��3����ԭ����____(�����ӷ���ʽ�ش𣩣������Һ�еμ�����NaOH��Һ���ɺ��ɫ�������y�ô�ʱ��Һ����Ԫ��������Ũ��Ϊ4.0x10-11mol/L�����ʱ��Һ��pH��_______(��֪��Ksp[Fe(OH)2]��8.0��10��16��Ksp[Fe(OH)3]��4.0��10��38)
(4) ��15000Cʱ��Ʒ���в����Ĺ������������ȴ����ϡ�����ܽ��һ�ػ�ɫ��Һ��ȡ��������Һ�μ�KSCN,��Һ�Ժ�ɫ����ȡ��������Һ�μ�K3[Fe(CN)6)(���軯�أ���Һ������������ɫ��������д��ͼ��14000Cʱ������Ӧ�Ļ�ѧ����ʽ_________ ,����������ɫ���������ӷ�Ӧ����ʽ______��
�ο��𰸣���1���ǣ�2�֣���2��FeC2O4 FeO��CO����CO2����2�֣�
FeO��CO����CO2����2�֣�
��3��Fe3����3OH�� Fe(OH)3��3H����2�֣� �� 5��2�֣� ��4��6Fe2O3
Fe(OH)3��3H����2�֣� �� 5��2�֣� ��4��6Fe2O3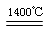 4Fe3O4��O2����2�֣���
4Fe3O4��O2����2�֣���
3Fe2����2[Fe(CN)6]3����Fe3[Fe(CN)6]2����K����Fe2����[Fe(CN)6]3����KFe[Fe(CN)6]����2�֣�
�����������1����Ʒ�ֽ�ķ���ʽ��
FeC2O4��2H2O FeC2O4��(2��n)H2O��nH2O
FeC2O4��(2��n)H2O��nH2O
180g?18n
1.000g?��1.000g��0.800g��
���n��2��������Ʒ�Ѿ���ȫ�ֽ�
��2��400��ʱ�����ּ�����0.800g��0.400g��0.400g
������ԭ���غ��֪��400�����ĺ���Ӧ����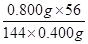 ��
��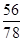 ����˸û������������������仯ѧʽ��FeO�����Է�Ӧ�Ļ�ѧ����ʽ��FeC2O4
����˸û������������������仯ѧʽ��FeO�����Է�Ӧ�Ļ�ѧ����ʽ��FeC2O4 FeO��CO����CO2����
FeO��CO����CO2����
��3��600����Ʒ����Ԫ�صĺ�����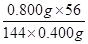 ��0.70����˸ù��������������������������������Ȼ�����������ˮ����Һ�����ԣ������ӷ���ʽ��Fe3����3OH��
��0.70����˸ù��������������������������������Ȼ�����������ˮ����Һ�����ԣ������ӷ���ʽ��Fe3����3OH�� Fe(OH)3��3H�������������������ܶȻ�������֪������Һ�������ӵ�����Ũ��Ϊ4.0x10-11mol/Lʱ����Һ��c(OH��)��
Fe(OH)3��3H�������������������ܶȻ�������֪������Һ�������ӵ�����Ũ��Ϊ4.0x10-11mol/Lʱ����Һ��c(OH��)��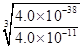 ��10��9mol/L��������Һ��c(H��)��10��5mol/L�����pH��5��
��10��9mol/L��������Һ��c(H��)��10��5mol/L�����pH��5��
��4����ȡ��������Һ�μ�K3[Fe(CN)6)(���軯�أ���Һ������������ɫ��������˵����Һ�л��������������ɡ����1400��ʱ�������ֽ���������������������Ӧ�Ļ�ѧ����ʽ��6Fe2O3 4Fe3O4��O2��������������ɫ���������ӷ�Ӧ����ʽ3Fe2����2[Fe(CN)6]3����Fe3[Fe(CN)6]2����K����Fe2����[Fe(CN)6]3����KFe[Fe(CN)6]����
4Fe3O4��O2��������������ɫ���������ӷ�Ӧ����ʽ3Fe2����2[Fe(CN)6]3����Fe3[Fe(CN)6]2����K����Fe2����[Fe(CN)6]3����KFe[Fe(CN)6]����
�����Ѷȣ�һ��
5�������
��������������Ҫ�ɷ�ΪFe2O3��Fe3O4��FeO��SiO2�ȣ�����������Ĺ�ҵ���������ۺ����öԻ�������������ʵ���壮���������������Ʊ�����Ȳ�Ʒ��ʵ���������£�
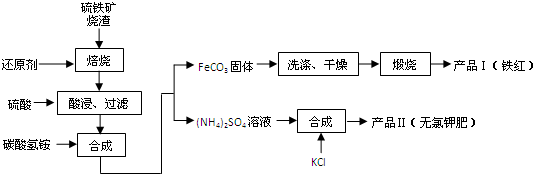
��֪�����ε��ܽ�����¶ȱ仯����������ͼ��ʾ��
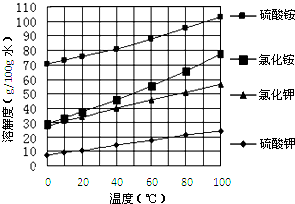
�ش��������⣺
��1����������˺���Һ�еĽ�����������______��
��2������FeCO3���ɲ�ƷI�Ļ�ѧ��Ӧ����ʽΪ______��ʵ���ҽ������ղ��������������˾ƾ��ơ������ǡ����żܡ��������⣬����______��
��3����Ʒ��Ļ�ѧʽΪ______��Ϊ�˻�ò�Ʒ����NH4��2SO4��Һ�м���KCl��Һ����Ҫ���еIJ����ǣ�______��
��4�������ƷII���Ƿ����Ȼ������ʵ�ʵ������ǣ�ȡ������Ʒ�����Թ��������Һ��______��
�ο��𰸣���1����Fe2O3��Fe3O4��FeO�뻹ԭ����Ӧ������������ϡ���ᷴӦ��������������������������Һ�е���Ҫ�����������������ʴ�Ϊ��Fe2+��
��2����̼��������������Ӧ�������������ж�����̼��4FeCO3+O2?����?.?2Fe2O3+4CO2����ʵ���ҽ������ղ������������оƾ��ơ������ǡ����żܡ�������������������ǯ��
�ʴ�Ϊ��4FeCO3+O2?����?.?2Fe2O3+4CO2��?����������ǯ��
��3����������Ȼ��ط�Ӧ��������غ��Ȼ�泥�������ص��ܽ�����¶ȱ仯�����������ᾧ�����ȹ��ˡ�ϴ�ӡ�����õ�����أ�
�ʴ�Ϊ��K2SO4�������ᾧ�����ȹ��ˡ�ϴ�ӡ����
��4��������ƷII���Ƿ����Ȼ����������ȳ�ȥSO4���ټ���Cl-�����Եμӹ���Ba��NO3��2��Һ�����˺�����Һ�μ�AgNO3��Һ��
�ʴ�Ϊ���μӹ���Ba��NO3��2��Һ�����˺�����Һ�μ�AgNO3��Һ��
���������
�����Ѷȣ�һ��