��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (8��) �������£�����A��B��C�ֱ�Ϊ���塢����ɫ���塢��ɫ���壬�ں��ʷ�Ӧ�����£����ǿ������п�ͼ���з�Ӧ����֪E��Һ����ɫ��Һ����ش�
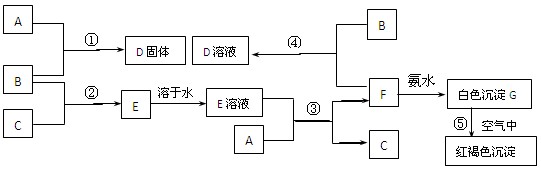
(1)? (�û�ѧʽ���)
A��______________B��________________
(2)��Ӧ�ٵĻ�ѧ����ʽΪ___________________________________________
��Ӧ�۵����ӷ���ʽΪ___________________________________________
��Ӧ�ݵĻ�ѧ����ʽΪ___________________________________________________
�ο��𰸣�(1) A��Fe? B��Cl2? (2)?�� 2Fe + 3Cl2 ="=" 2FeCl3?�� Fe +2H+ ="=" Fe2+? + H2��
�� 4Fe(OH)2 + O2 + 4H2O ="=" 4Fe(OH)3
�������������������ͼ�⣬������Ѱ��ͻ�Ƶ㡣B�ǻ���ɫ���壬��B����������ɫ����G���ڿ�����ת��Ϊ���ɫ����������G����������������˵���A����������ΪC����ɫ���壬����C��������D���Ȼ�������E���Ȼ��⣬F���Ȼ�������
�����Ѷȣ�һ��
2������� ��12�֣�A��J����ѧ��ѧ���������ʣ�����֮���ת����ϵ����ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�D��һ�ֺ���ɫ���塣
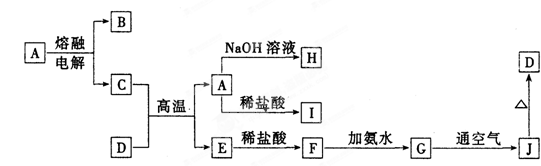 ��ش�
��ش�
�������⣺
��1��A���ʵ�����Ϊ_________��H��I��Ӧ�Ļ�ѧ����ʽ??
��2��C��D�ڸ����µķ�Ӧ��ұ��ҵ�ϳ�Ϊ?��Ӧ�������÷�Ӧ��ʵ�������?
___?
��3��д��G��J�Ļ�ѧ����ʽ��___?��
��4��A��H�����ӷ���ʽΪ___________________________________________
��5�������ӷ���ʽ��ʾI���������ھ�ˮ��ԭ��_____________________?_
�ο��𰸣���1����������1�֣�? 3NaAlO2+AlCl3+6H2O=4Al(OH)3+3NaCl��2�֣�
��2�����ȣ�1�֣�?������KClO3������þ���������ȼ��2�֣�
��3��4Fe(OH)2+O2+2H2O=4Al(OH)3��2�֣�
��4��Al2O3+2OH-+H2O=2AlO2-+H2O��2�֣�
��5��Al3++3H2O Al(OH)3(����)+3H+��2�֣�
Al(OH)3(����)+3H+��2�֣�
�������������������ͼ�⣬��������ͻ�Ƶ㡣D��һ�ֺ���ɫ���壬����D����������J������������G������������������E������F���Ȼ�������A��һ�ָ��۵����ʣ���A��������������B��������C������H��ƫ�����ƣ�I���Ȼ���.
�����Ѷȣ�һ��
3������� ��15�֣�A��B��C��D���־�Ϊ������Ԫ�أ�ԭ��������������
��1��AԪ��ԭ�������������Ǻ�����Ӳ�����3����A��Dͬ���壬A��D���γ����ֻ�����X��Y��X��ˮ��Ӧ������һ�־��л�ԭ�ԵĶ�Ԫ��M��M����ʹ��ˮ��ɫ��
��2��AԪ�صĵ��ʺ�CԪ�صĵ��ʻ��Ͽ�����Z�� Z�ڼ��������¸�ˮ��Ӧ�IJ���1 mol����3mol KOH������ȫ�к͡�
��3��AԪ�صĵ��ʺ�BԪ�صĵ���һ�������·�Ӧ���ɻ�����N��DԪ�صĵ��ʺ�BԪ�صĵ��ʷ�Ӧ���ɻ�����G��������N�ͻ�����G����Է���������ȣ�����ɫ��Ӧ���ʻ�ɫ��
�ش��������⣺
��1������Ԫ��D�����ӽṹʾ��ͼ��?��
��2��A��B��C��D����Ԫ�ص�ԭ�Ӱ뾶����С�������е�˳��Ϊ������Ӧ��Ԫ�ط��ű�ʾ��:?
��3��M����ʹ��ˮ��ɫ��д���÷�Ӧ�����ӷ���ʽ?��
��4��Z����ˮ��Ӧ�Ļ�ѧ����ʽ?��
��5��������N�뻯����G��ˮ��Һ��Ӧ�����������뻹ԭ�����ʵ���֮��Ϊ1��1���÷�Ӧ�����ӷ���ʽΪ??
��6�������£�D���⻯�����̬���ж���ˮ��Һ�����ԡ��ѳ���Ȼ����D���⻯����ܼ��ٻ�����Ⱦ���ֿɻ���D�ĵ��ʡ��ù���NaOH��Һ����D���⻯�����ʯī���缫������Һ�ɻ���D�ĵ��ʣ������ܷ�Ӧ�Ļ�ѧ����ʽ�������ܽ�����������ԭ��Ӧ��Ϊ?��
�÷������ŵ���?��
�ο��𰸣���1��?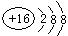 ?��1�֣���?��2��O��S ��P�� Na?��2�֣�
?��1�֣���?��2��O��S ��P�� Na?��2�֣�
��3��H2SO3 + Br2 + H2O = 4H+ + SO42- + 2Br- ��2�֣�?
��4��P2O5+3H2O(��)=2H3PO4?��2�֣�
��5��Na2O2 + S2- + 2H2O = 2Na+ + S + 4OH- ��3�֣�
��6��Na2S + 2H2O S��+ H2��+ 2NaOH��3�֣�
S��+ H2��+ 2NaOH��3�֣�
������������ɵ�NaOH��ѭ�����ã���������������Ϊ����ԭ�ϻ�ȼ�� ��2�֣�
�ɣ�1��֪A��D�ֱ�ΪO��S���γɵĻ�����X��Y�ֱ�ΪSO2��SO3��MΪH2SO3���ɣ�2��֪CԪ��ΪP��Z��P2O5���ɣ�3��֪BΪNa��������N��G�ֱ���Na2O2��Na2S��Ȼ������Ԫ�������ɺ��й����ʵ����ʿ�˳���Ľ���й����⡣
�����Ѷȣ�һ��
4������� �ס��ҡ���Ϊ������Ԫ���γɵij������ʣ�A��B��C��D��E��F��G��X��Ϊ�����Ļ����B��X��ʽ��������������ͬ��E��ʽ����D��16����һ�������¸�����֮���ת������ͼ��ʾ��
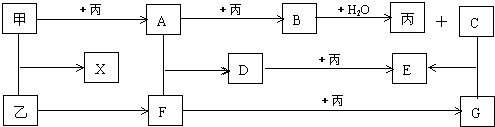
��1��X�ĵ���ʽ��______��G�Ļ�ѧʽ��______��
��2����������������ˮ������Ӧ�������ǵ������ε�ˮ�⣩�ҷ�Ӧ��ˮ�Ȳ���������Ҳ���ǻ�ԭ�������ʵĴ���______��
��3����Ӧ��D+�����Ļ�ѧ����ʽ��______��
��4��д��X��D��ϡ�����з�Ӧ�����ӷ���ʽ______��
�ο��𰸣��ס��ҡ���Ϊ������Ԫ���γɵij������ʣ�A��B��C��D��E��F��G��X��Ϊ�����Ļ����B��ˮ��Ӧ���ɵ��ʱ���C���ܺ�ˮ��Ӧ���ɵ��ʵĶ�����Ԫ�ػ�����ֻ�й������ƣ����Ա���������C���������ƣ�B�ǹ������ƣ�������A��������Ӧ���ɹ������ƣ���A�������ƣ��ƺ�������Ӧ���������ƣ�������ƣ�
B��X��ʽ��������������ͬ����X�к�����Ԫ�أ����ƺ������Ƶ�ʽ����ͬ������X�����ƣ����������ʣ���Ӧ����F����F�к�����Ԫ�أ�F�ܺ�������Ӧ����G���������ƺ�G�ܷ�Ӧ����E��G��������������ᣬ��F��������������������һ����Ӧ���������ᣬ����F�Ƕ���������G���������������ƺͶ�������Ӧ����D��D���������ƣ��������ƺ�������Ӧ���������ƣ��������Ʊ��������Ƶ�ʽ����16������֪�������ϣ����ƶ���ȷ��
��1������Ʒ�Ӧ�������ƣ����������ӻ���������ʽΪ��

��G�����������仯ѧʽΪ��SO3���ʴ�Ϊ��

��SO3��
��2������ˮ������Ӧ�������ǵ������ε�ˮ�⣩�ҷ�Ӧ��ˮ�Ȳ���������Ҳ���ǻ�ԭ����˵����Ӧ������ˮ�и�Ԫ�صĻ��ϼ۶��������仯���ܺ�ˮ��Ӧ���������ơ������ơ��������ơ���������Ͷ��������ں�ˮ��Ӧ��ˮ�Ȳ���������Ҳ���ǻ�ԭ�����������ơ��������ơ������������������ѡA��B��F��G��?
��3���������Ʋ��ȶ����ױ������������������ƣ���Ӧ����ʽΪ��2Na2SO3+O2�T2Na2SO4��
�ʴ�Ϊ��2Na2SO3+O2�T2Na2SO4��
��4�������Ӻ�����������ӷ�Ӧ�������ʺ�ˮ�����ӷ�Ӧ����ʽΪ��2S2-+SO32-+6H+�T3S��+3H2O��
�ʴ�Ϊ��2S2-+SO32-+6H+�T3S��+3H2O��
���������
�����Ѷȣ�һ��
5������� ��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ������ʣ����ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬��

�����������գ�
��1��H�Ļ�ѧʽ______���侧����������ѧ������Ϊ______������H�������ӵķ�����______��
��2��A��B�ڼ��������·�Ӧ����Ҫ������______��F��H2O��Ӧ�Ļ�ѧ����ʽΪ______��д��G��Һ�м��������I��Һ��Ӧ�����ӷ���ʽ______��
��3��ij�¶�ʱ����2L�����У�D��E��J�������ʵ����ʵ�����ʱ��仯��������ͼ��ʾ����ͼ�����ݷ������÷�Ӧ�Ļ�ѧ����ʽΪ______����Ӧ��ʼ��2min����J��ʾ��ƽ����Ӧ����Ϊ______��
�ο��𰸣���֪B��C��D��E�Ƿǽ������ʣ����ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬������ת����ϵ�еķ�Ӧ����������C+D=I�ķ�Ӧ�����ǹ��գ��ƶ�Ϊ�����������ķ�Ӧ��I+J=���H��˵��I��HCl��J��NH3��DΪH2��C��Cl2��EΪN2��������G����ɫ��ӦΪ��ɫ˵������Ԫ�أ�G+I=CO2��֤��GΪ̼���Σ�B�Ƿǽ���������F�Ͷ�����̼��Ӧ���ɵģ��ƶ�FΪNa2O2��BΪO2��AΪNa��
��1��H�Ļ�ѧʽΪNH4Cl��������������ѧ������Ϊ���Ӽ������ۼ�������H��NH4Cl���������ӣ�NH4+���ķ���Ϊ��ȡ����H��Ʒ�����Թܣ���������������Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬֤����笠����ӣ�
�ʴ�Ϊ��NH4Cl�����Ӽ������ۼ���ȡ����H��Ʒ�����Թܣ���������������Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬֤����笠����ӣ�
��2��A��Na����B��O2���ڼ��������·�Ӧ����Ҫ�����ǣ����ҷ�Ӧ������Ϊ��ɫ�����ɵ���ɫ�Ĺ��壻F��Na2O2����H2O��Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����G��NH4Cl����Һ�м��������I��HCl����Һ��Ӧ�����ӷ���ʽ��CO32-+2H+=CO2��+H2O��
�ʴ�Ϊ�����ҷ�Ӧ������Ϊ��ɫ�����ɵ���ɫ�Ĺ��壻2Na2O2+2H2O=4NaOH+O2����CO32-+2H+=CO2��+H2O��
��3����ͼ�����ݷ��������ķ�ӦΪD+E=J��D��E�������ʵ���Ϊn��H2��=1.0mol-0.7mol=0.3mol��n��N2��=1.0mol-0.9mol=0.1mol������J�����ʵ���Ϊ��n��NH3��=0.2mol����Ӧ���ʵ���֮��Ϊn��H2����n��N2����n��NH3��=0.3mol��0.1mol��0.2mol=3��1��2���÷�Ӧ�Ļ�ѧ����ʽΪN2+3H2 2NH3����J��NH3����ʾ�ķ�Ӧ����=0.2mol2L2min=0.05mol/L?min��
2NH3����J��NH3����ʾ�ķ�Ӧ����=0.2mol2L2min=0.05mol/L?min��
�ʴ�Ϊ��N2+3H2 2NH3��0.05mol/L?min��
2NH3��0.05mol/L?min��
���������
�����Ѷȣ���