��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ѧ�г���������ͼ����ʾij�ֱ仯���̣��й������ĸ�����ͼ��˵����ȷ����
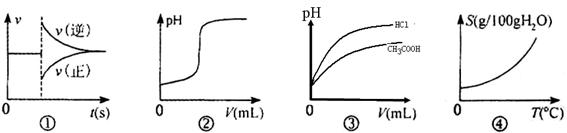
A������ͼ�ٿ��Ա�ʾ��ij��ѧƽ����ϵ�ı��¶Ⱥ�Ӧ������ʱ��ı仯
B������ͼ�ڿ��Ա�ʾ��һ����������������Һ�еμ�һ��Ũ�ȵ�ϡ����ʱpH�仯
C������ͼ�ۿ��Ա�ʾ��ͬpH��CH3COOH��HCl��Һ�ֱ��ˮϡ��ʱ��Һ��pH����Һ����仯������
D������ͼ�ܿ��Ա�ʾ���еĹ��������ܽ�����¶ȵı仯
�ο��𰸣�C
����������ٲ���ȷ�������¶ȷ�Ӧ���ʶ�Ӧ��������ġ�ϡ����ζ��������ƣ�pHӦ���Ǽ�С�ģ��ڲ���ȷ�����������ᣬϡ�ʹٽ����룬����ϡ�ͺ�����pH��С������ģ�����ȷ���������ʵ��ܽ�Ȳ�һ���������¶����߶�����ģ������������Ƶȣ��ܲ���ȷ����ѡC��
�����Ѷȣ���
2��ѡ���� �����£���20mL0.2mol/LH2A��Һ�еμ�0.2mol/LNaOH��Һ���й��������ʵ����仯����ͼ�����Т����H2A�������HA-�������A2-��������ͼͼʾ�жϣ�����˵��������ǣ�?��
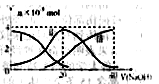
A����V��NaOH��=20mLʱ����Һ������Ũ�ȴ�С��ϵ��c(Na+)>c(HA����>c(H+)>?c(A2��)>c(OH��) ?
B���������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮ�Ĵ�?
C��NaHA��Һ�У�c(OH-)��c(A2�C)��c(H+)��c(H2A)?
D����Na2A��Һ����ˮ�Ĺ����У�pH��С
�ο��𰸣�B
���������A����V��NaOH��="20" mLʱ��������ӦΪNaOH+H2A=NaHA+H2O����Һ��ҪΪNaHA����ͼ��֪c��A2-����c��H2A����˵��HA-�������ˮ��̶ȣ���Һ�����ԣ���c��Na+����c��HA-����c��H+����c��A2-����c��OH-������ȷ��B����ͼʾ��ϵ֪��c��A2-����c��H2A����˵���������ˮ��̶ȣ���Һ�����ԣ�ˮ�ĵ����ܵ������ƣ�����C�����ݵ���غ��c��OH-��+2c��A2-��+c��HA-��=c��H+��+c��Na+�������������غ��c��Na+��=c��HA-��+c��H2A��+c��A2-�������Ե�c��OH-��+c��A2-��=c��H+��+c��H2A������ȷ��D��Na2A��Һ��ˮϡ�ͣ��ٽ���ˮ�⣬����Һ������������Ũ�ȼ�С��������Һ��pH��С����ȷ����ѡB��
�����Ѷȣ�һ��
3��ѡ���� ��pH������4��HCl��NH4Cl������Һ�У�����ˮ���������H+ ����Ũ�ȷֱ�ΪA mol/L��B mol/L����A��B��ϵΪ��?��
A��A>B
B��A=10��6 B
C��B=10��6 A
D��A=B
�ο��𰸣�B
���������pH=4��HCl��Һ����ˮ�������c(H+)Ϊ10-10��pH=4��NH4Cl��Һ����ˮ�������c(H+)Ϊ10-4������A=10-6 B����ѡB��
����������Һ���β��ܵ����H+����������Һ�е�H+����ˮ��������ġ�
�����Ѷȣ�һ��
4������� ��ѧ��Ӧ���̷������ʱ仯ͬʱ�����������仯������������ʽ���ֳ������з�Ӧ�ȣ����кܶ��֣�ȼ���ȣ��к��ȵȣ�
��1�����ѧ��Ӧ�ķ�Ӧ�ȿ���ֱ�Ӳ�����������������______��
��2�����С�H��ʾ����ȼ���ȵ���______������ţ�����ʾ�к��ȵ���______�����H1����H2�����H3���ȣ���
A.2H2��g��+O2��g���T2H2O��l������H1
B��C��s��+
O2��g���TCO��g������H2
C��CH4��g��+2O2��g���TCO2��g��+2H2O��l������H3
D��C��s��+O2��g���TCO2��g������H4
E��C6H12O6��s��+6O2��g���T6CO2��g��+6H2O��l������H5
F��NaOH��ag��+HCl��ag���TNaCl��ag��+H2O��l������H6
G.2NaOH��ag��+H2SO4��ag���TNa2SO4��ag��+2H2O��l������H7
��3����֪15g������ȫȼ������CO2��Һ̬ˮ������akJ�������Ȼ�ѧ����ʽ��ȷ��______��
A��C2H6��g��+O2��g���T2CO2��g��+3H2O��l������H1=+2akJ/mol
B��C2H6��g��+O2��g���T2CO2��g��+3H2O��g������H2=-2akJ/mol
C.2C2H6��g��+7O2��g���T4CO2��g��+6H2O��l������H3=-4akJ/mol
D.2C2H6��g��+7O2��g���T4CO2��g��+6H2O��g������H4=-2akJ/mol
��4�����ȼ��һ������ų�����161.9kJ�����ɵ�CO2ǡ����5mol/L100mLKOH��Һ��ȫ��Ӧ�������Σ���ȼ��1mol����ų�����Ϊ______��
��5����һ���о���������ѧ��Ӧ�����仯������йأ����ܼ�����Ͽ�1mol��ѧ�������������±��Ǽ������ݣ�
| ��ѧ�� | P-P | P-O | O=O | P=O
���ܣ�kJ/mol��
197
360
499
X
|
��֪����ȼ����Ϊ2378.0kJ/mol����X=______��

�ο��𰸣���1�����ڲⶨ���ʵ����ݼ����ַ�Ӧ�ȵ������������ȼƣ�Ҳ�������ǡ���������
�ʴ�Ϊ�����ȼƣ�
��2��A�����������ʵ���Ϊ2mol����Ӧ�ȡ�H1���ܱ�ʾȼ���ȣ�
B��̼ȼ�յ�������ΪCO����ʾ�¶ȵ�������CO2����Ӧ�ȡ�H2���ܱ�ʾȼ���ȣ�
C��1mol������ȫȼ�գ����ɵ�ˮ����̬�������ȶ���״̬��ӦΪҺ̬ˮ���ʷ�Ӧ�ȡ�H3���ܱ�ʾȼ���ȣ�
D��C��s��+O2��g���TCO2��g����H4��1molC��ȫȼ�����ɶ�����̼������ȼ���ȸ����Ӧ�ȡ�H4�ܱ�ʾȼ���ȣ�
E��C6H12O6��s��+6O2��g���T6CO2��g��+6H2O��l����H5��1molC6H12O6��ȫȼ�����ɶ�����̼��Һ̬ˮ������ȼ���ȸ����Ӧ�ȡ�H5�ܱ�ʾȼ���ȣ�
F��NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H6��ʵ����1mol��������1mol���������ӷ�Ӧ����1molH2O�������к��ȸ����Ӧ�ȡ�H6�ܱ�ʾ�к��ȣ�
G��2NaOH��ag��+H2SO4��ag���TNa2SO4��ag��+2H2O��l������H7��Ӧ���ɵ�ˮΪ2mol����Ӧ�ȡ�H7���ܱ�ʾ�к��ȣ�
�ʴ�Ϊ����H4����H5����H6��
��3��A��C2H6��g��+72O2��g���T2CO2��g��+3H2O��l������H1=+2akJ/mol���Ȼ�ѧ��Ӧ����ʽ�С�H��0����ʾ���ȣ���C2H6ȼ�շ�Ӧ�Ƿ��ȷ�Ӧ����A����
B��C2H6��g��+72O2��g���T2CO2��g��+3H2O��g������H2=-2akJ/mol����ȫȼ��1mol�������ɶ�����̼��Һ̬ˮ����2akJ���÷���ʽ��ʾ������̬ˮ����B����
C.2C2H6��g��+7O2��g���T4CO2��g��+6H2O��l������H3=-4akJ/mol����ȫȼ��2mol�������ɶ�����̼��Һ̬ˮ����4akJ����C��ȷ��
D.2C2H6��g��+7O2��g���T4CO2��g��+6H2O��g������H4=-2akJ/mol����ȫȼ��2mol�������ɶ�����̼��Һ̬ˮ����4akJ����D����
��ѡ��C��
��4��KOH�����ʵ���Ϊ0.1L��5mol/L=0.5mol�����ݼ������غ㣬��n��K2CO3��=0.5mol��12=0.25mol��
����̼Ԫ���غ���n��CO2��=n��K2CO3��=0.25mol��
����̼Ԫ���غ��֪����������ʵ���n��C4H10��=14��0.25mol���ų�����161.9kJ��
����1mol������ȫȼ�շų�������Ϊ161.9kJ��16=2590.4kJ��
�ʴ�Ϊ��2590.4kJ��
��5������ȼ�յ��Ȼ�ѧ����ʽΪP4��s��+5O2��g���TP4O10��s����H=-2378.0kJ/mol��
��6��197kJ/mol+5��499kJ/mol-12��360kJ/mol-4X=-2378kJ/mol��
X=433.75kJ/mol��
�ʴ�Ϊ��433.75��
���������
�����Ѷȣ�һ��
5������� (6��)KMnO4��Һ��H2C2O4��Һ�ɷ������·�Ӧ��
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O
��1���÷�Ӧ���ʿ�ʼʮ�ֻ�����һ��ʱ���ͻȻ�ӿ죬������Ϊ_____(�ѧʽ)�Ը÷�Ӧ���д����á�
��2���ݴ�ԭ������������KMnO4��Һ���ⶨH2C2O4��Һ��Ũ�ȣ������������£�
��ȷ����0.10mol/L��KMnO4��Һ
�ڽ�KMnO4��Һʢ����______�ζ����У����ʽ����ʽ����
��ȷ��ȡ25.00mL H2C2O4��Һ����ƿ��
�ܽ��еζ�
�ζ��յ���ʲô����_________________,�Ƿ���Ҫָʾ��__________(��ǡ���)
��3�������в����У���ʹ�ⶨ��H2C2O4��ҺŨ��ƫ�����___________��
��ʢװKMnO4��Һ�ĵζ���������ˮϴ����δ��KMnO4��Һ��ϴ
����ƿ��ʢ����������ˮ���ټӴ���Һ
��ʢװH2C2O4��Һ�ĵζ���������ˮϴ����δ��H2C2O4��Һ��ϴ
�ܵζ���۲�ζ��ܶ���ʱ�����߸��ڿ̶���
��4���ζ�ʱ���õ�ʵ���������£��Լ�������H2C2O4��Һ��Ũ��Ϊ_________mol/L
ʵ��������
| ����Һ���mL
| ����ı�Һ�����mL��
|
1
| 25.00
| 28.95
|
2
| 25.00
| 25.05
|
3
| 25.00
| 24.95
�ο��𰸣���6�֣���1��MnSO4?��2����ʽ?��Һ����ɫ��Ϊ�Ϻ�ɫ?��?��3����?��4��0.25
�����������1�����ݷ���ʽ��֪�������ɵ������������̺�CO2����CO2�����壬����������õ��������̡�
��2�����������Һ����ǿ�����ԣ��ܸ�ʴ������Ӧ������ʽ�ζ���ʢ�Ÿ��������Һ���������Ը��������Һ�����Ϻ�ɫ�ģ����Բ���Ҫ����ָʾ���յ�ʱ����������Һ����ɫ��Ϊ�Ϻ�ɫ��
��3�����൱��ϡ���˸��������Һ��Ũ�ȣ��������ĸ��������Һ�����ƫ�ⶨ���ƫ�ߡ���ƿ�����ñ�Һ��ϴ�����Ԣڲ�Ӱ�졣��Ҳ���൱��ϡ�Ͳ����Ũ�ȣ��������ĸ��������Һ�����ƫ�٣��ⶨ���ƫ�͡��ζ���۲�ζ��ܶ���ʱ�����߸��ڿ̶��ߣ�˵������ƫС�����Բⶨ���ƫ�ͣ���ѡ�١�
��4������ʵ�����ݿ�֪����һ��ʵ�����̫�����á�ʵ����ݺ����ε����ݿ�֪�����ĸ��������Һ�������ƽ��ֵ��25.00ml�����Ը��ݷ���ʽ��֪��������Һ��Ũ����0.10mol/L��2.5��0.25mol/L��
�����Ѷȣ�һ��
|