��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��8�֣� ��֪ij��ӦA(g)��B(g)?C(g)��D(g)���й����е������仯��ͼ��ʾ����ش��������⣺
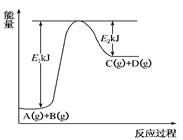
(1)�÷�Ӧ�Ħ�H��________kJ��mol��1(�ú�E1��E2�Ĵ���ʽ��ʾ)����1�֣�
(2)���ڷ�Ӧ��ϵ�м������ʹ�淴Ӧ����������E1________(���������С�����䡱����ͬ)����H________����2�֣�
(3)����ͬ�¶Ⱥ�ѹǿ�£��Է�ӦA(g)��B(g)
�ο��𰸣�
���������
�����Ѷȣ�һ��
2������� ����������һ�ֽྻ����������Դ����������(��Ҫ�ɷ�Ϊ CO��CO2��H2��)��H2��ϣ����ϳɼ״��Ͷ����ѣ�CH3OCH3���������������ʵȣ��������������õķ���֮һ.
��1����֪̼��������Ӧ�ڲ�ͬ�¶���ƽ�ⳣ���Ķ���ֵ��lgK�����±�:
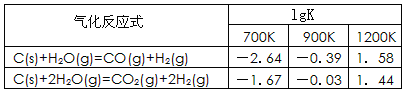
��Ӧ��CO(g)+H2O(g)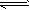 CO2(g)+H2(g)���÷�Ӧ�ġ�H________0��ѡ�����������������������������900Kʱ���÷�Ӧƽ�ⳣ���Ķ���ֵ��lgK��=_____________.
CO2(g)+H2(g)���÷�Ӧ�ġ�H________0��ѡ�����������������������������900Kʱ���÷�Ӧƽ�ⳣ���Ķ���ֵ��lgK��=_____________.
��2���״���һ����Ҫ����Դ�ͻ���ԭ�ϣ���ҵ�Ϻϳɼ״��ķ�ӦΪ��CO+2H2?CH3OH������֪��H2(g)��CO(g)��CH3OH(l)��ȼ���Ȧ�H�ֱ�Ϊ-285.8KJ/mol��-283.0KJ/mol��-726.5KJ/mol����CH3OH����ȫȼ������CO��Һ̬H2O���Ȼ�ѧ��Ӧ����ʽ .
��3����һ���¶ȡ�ѹǿ�ʹ������£���ҵ����CO��H2��Ӧ���ɶ����ѣ�ͬʱ����һ�ֲ������ѭ���������÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ�� ��
��4����ͼ��Ϊ��ɫ��Դ��������ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��a�缫�Ϸ�����Ӧ�ĵ缫��ӦʽΪ .
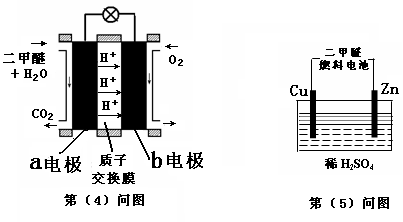
��5��������ͼ��װ�õĵ�ԴΪ��4�����еĶ�����ȼ�ϵ�ء���ͨ��Դһ��ʱ��۲쵽װ���е������Һ��ɫ����ɫ��Ϊ��ɫ����������װ���е�Cu�缫Ӧ�������ȼ�ϵ���� �缫����a��b��������ͨ��ʱ������Ӧ���ܵ����ӷ�Ӧ����ʽΪ�� .
�ο��𰸣���1������ 0.36 ��2��CH3OH��l��+O2��g��=CO��g��+2H2O��l������H=-443.5KJ/mol
��3��3CO+3H2 =��CH3��2O+CO2����2CO+4H2 =��CH3��2O+ H2O��
��4����CH3��2O-12e-+3H2O=2CO2+12H+��5��b Cu+2H+ Cu2++H2��
Cu2++H2��
���������K1="{" C(CO)·C(H2)} /C(H2O);K2=" {" C(CO2)·C2(H2)} /C2(H2O) ��-�������ã�CO(g)+H2O(g)  CO2(g)+H2(g)������ƽ�ⳣ��Ϊ��K="{" C(CO2)·C(H2)} /{ C(CO) ·C(H2O)}.="K2/K1." KԽ��lgK��Խ�������¶ȣ˼�С��˵�������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ����淴Ӧ�����ȷ�Ӧ����������ӦΪ���ȷ�Ӧ�����ԡ�H����.��900Kʱ���÷�Ӧƽ�ⳣ���Ķ���ֵlgK ="lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36." ��2���������д��CO��CH3OHȼ�յ��Ȼ�ѧ����ʽ��CO(g)+(1/2)O2(g)=CO2(g) ��H=-283.0KJ/mol����CH3OH��l��+(3/2)O2��g��=CO2��g��+2H2O.��-�ٵã�CH3OH��l��+O2��g��=CO��g��+2H2O��l������H=-443.5KJ/mol����3����������ɵ÷�Ӧ�Ļ�ѧ����ʽ��3CO+3H2 =��CH3��2O+CO2����2CO+4H2 =��CH3��2O+ H2O����4����ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫��������ͨ�������ĵ缫��������a�缫�������Ϸ�����Ӧ�ĵ缫��Ӧʽ�ǣ���CH3��2O-12e-+3H2O=2CO2+12H+����5���ڵ����й۲쵽װ���е������Һ��ɫ����ɫ��Ϊ��ɫ�������˵��Cuʧȥ�˵��ӡ�Cu�缫��������������ȼ�ϵ����b�缫����������������ͨ��ʱ������Ӧ���ܵ����ӷ�Ӧ����ʽΪ��Cu+2H+
CO2(g)+H2(g)������ƽ�ⳣ��Ϊ��K="{" C(CO2)·C(H2)} /{ C(CO) ·C(H2O)}.="K2/K1." KԽ��lgK��Խ�������¶ȣ˼�С��˵�������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ����淴Ӧ�����ȷ�Ӧ����������ӦΪ���ȷ�Ӧ�����ԡ�H����.��900Kʱ���÷�Ӧƽ�ⳣ���Ķ���ֵlgK ="lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36." ��2���������д��CO��CH3OHȼ�յ��Ȼ�ѧ����ʽ��CO(g)+(1/2)O2(g)=CO2(g) ��H=-283.0KJ/mol����CH3OH��l��+(3/2)O2��g��=CO2��g��+2H2O.��-�ٵã�CH3OH��l��+O2��g��=CO��g��+2H2O��l������H=-443.5KJ/mol����3����������ɵ÷�Ӧ�Ļ�ѧ����ʽ��3CO+3H2 =��CH3��2O+CO2����2CO+4H2 =��CH3��2O+ H2O����4����ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫��������ͨ�������ĵ缫��������a�缫�������Ϸ�����Ӧ�ĵ缫��Ӧʽ�ǣ���CH3��2O-12e-+3H2O=2CO2+12H+����5���ڵ����й۲쵽װ���е������Һ��ɫ����ɫ��Ϊ��ɫ�������˵��Cuʧȥ�˵��ӡ�Cu�缫��������������ȼ�ϵ����b�缫����������������ͨ��ʱ������Ӧ���ܵ����ӷ�Ӧ����ʽΪ��Cu+2H+ Cu2++H2����
Cu2++H2����
���㣺����ԭ��ء����صķ�Ӧԭ������ѧƽ�ⳣ���ļ��㡢�Ȼ�ѧ����ʽ����д��֪ʶ��
�����Ѷȣ�����
3������� (14��)Ϊ�˼���CO�Դ�������Ⱦ��ij�о���ѧϰС�����о�����CO��H2O��Ӧת��Ϊ��ɫ��ԴH2����֪��
2CO��g��+O2��g����2CO2��g�� ��H����566kJ?moL-1
2H2��g��+O2��g����2H2O��g�� ��H����483.6kJ?moL-1
H2O��g����H2O��l�� ��H����44.0kJ?moL-1
��1��д��CO��H2O(g)��������CO2��H2���Ȼ�ѧ����ʽ��___________________________��
��2�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
N2(g)��3H2(g) 2NH3(g) ��H����92.4kJ/mol
2NH3(g) ��H����92.4kJ/mol
���ϳɰ���Ӧ�ﵽƽ��ı�ijһ�������(���ı�N2��H2��NH3����)����Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��
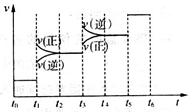
��ͼ��t3ʱ����ƽ���ƶ�������������__________________________________________�����б�ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����_____________��
���¶�ΪT��ʱ����1 mol N2��2 mol H2�����ݻ�Ϊ0.5 L���ܱ������У���ַ�Ӧ����N2��ƽ��ת����Ϊ50������Ӧ��T��ʱ��ƽ�ⳣ��Ϊ____________mol-2��L2��
��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�
��ͼ��ʾ�������ı䣬ƽ����ϵ�а�����������ı仯���ơ�
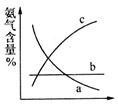
��������Ϊѹǿʱ���仯������ȷ����(����ţ���ͬ)__________����������Ϊ�¶�ʱ���仯������ȷ����___________��
��3�������°�����HCl����������ˮ���ֽ���ͬ�������ͬ���ʵ���Ũ�ȵİ�ˮ�������ϣ�������Һ�и����ӵ����ʵ���Ũ�Ȱ����ɴ�С��˳����������Ϊ_______>_______>_______>________��
�ο��𰸣���ÿ��2�֣���14�֣���1��CO(g)��H2O(g)=CO2(g)��H2(g) ��H=��41.2kJ��mol��1
��2�������� t2-t3 ��4 ��c a
��3��c(Cl��)>c(NH4��)>c(H��)>c(OH��) ��˳����ȷ��2�֣�˳�����÷֣�
�����������1����֪����2CO��g��+O2��g����2CO2��g�� ��H����566kJ?moL-1����2H2��g��+O2��g����2H2O��g����H����483.6kJ?moL-1������ݸ�˹���ɿ�֪���١��ڣ���2���ɵõ�CO��H2O(g)��������CO2��H2���Ȼ�ѧ����ʽΪCO(g)��H2O(g)=CO2(g)��H2(g) ��H=��41.2kJ��mol��1��
��2�������Ǻϳɰ�����Ҫԭ�ϣ��ϳɰ���Ӧ���Ȼ�ѧ����ʽ���£�
N2(g)��3H2(g) 2NH3(g) ��H����92.4kJ/mol
2NH3(g) ��H����92.4kJ/mol
��t3ʱ���淴Ӧ���ʾ����������淴Ӧ���ʴ�������Ӧ���ʣ�ƽ�����淴Ӧ������С���������Ӧ�������С�ķ��ȵĿ��淴Ӧ��������ƽ���ƶ��������������¶ȡ�ƽ��������Ӧ������У������ĺ����ߣ���˸���ͼ���֪��ʾƽ��������NH3�ĺ�����ߵ�һ��ʱ����t2-t3��
���¶�ΪT��ʱ����1 mol N2��2 mol H2�����ݻ�Ϊ0.5 L���ܱ������У���ַ�Ӧ����N2��ƽ��ת����Ϊ50��������ݷ���ʽ��֪���ɰ�����0.5mol��2��1.0mol��ʣ�ఱ��0.5mol������2mol��1.5mol��0.5mol����Ӧ��T��ʱ��ƽ�ⳣ��Ϊ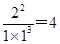 mol-2��L2��
mol-2��L2��
��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�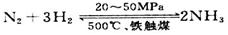
ͼ��ʾ�������ı䣬ƽ����ϵ�а�����������ı仯���ơ���������Ϊѹǿʱ������ѹǿƽ��������Ӧ������У������ĺ������ߣ����Ա仯������ȷ����c����������Ϊ�¶�ʱ�������¶�ƽ�����淴Ӧ������У������ĺ������ͣ���仯������ȷ����a��
��3�������°�����HCl����������ˮ���ֽ���ͬ�������ͬ���ʵ���Ũ�ȵİ�ˮ�������ϣ�����ǡ�÷�Ӧ�����Ȼ�泥�笠�ˮ����Һ�����ԣ���������Һ�и����ӵ����ʵ���Ũ�Ȱ����ɴ�С��˳����������Ϊc(Cl��)>c(NH4��)>c(H��)>c(OH��) ��
���㣺�����˹���ɡ����������ƽ��״̬��Ӱ�졢ƽ�ⳣ�������Լ�Ũ�ȴ�С�Ƚ�
�����Ѷȣ�����
4������� ��������ɴ��Ļ���ƽ�����ʢ��ǿ��ԭ��Һ̬�£�N2H4����ǿ������Һ̬˫��ˮ������0.4molҺ̬�º�0.8mol?H2O2��Ϸ�Ӧ�����ɵ�����ˮ�������ų�256.7kJ��������
��1����Ӧ���Ȼ�ѧ����ʽΪ______��
��2������֪H2O��l��=H2O��g����H=+44kJ/mol����16gҺ̬����Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų���������______kJ��
��3���˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���______��
��4����֪N2��g��+2O2��g���T2NO2��g������H=+67.7kJ-mol-1��N2H4��g��+O2��g���TN2��g��+2H2O?��g������H=-534kJ-mol-1�����ݸ�˹����д������NO2��ȫ��Ӧ���ɵ�������̬ˮ���Ȼ�ѧ����ʽ______��
�ο��𰸣���1��0.4molҺ̬�·ų�256.652KJ����������1molҺ̬�·ų�������Ϊ256.7kJ0.4�T614.75kJ�����Է�Ӧ���Ȼ�ѧ����ʽΪ��N2H4��g��+2H2O2��l��=N2��g��+4H2O��g����H=-614.75kJ/mol��
�ʴ�Ϊ��N2H4?��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.75kJ?mol-1
��2����N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.675KJ/mol��
? ��H2O��l��=H2O��g����H=+44KJ/mol��
���ݸ�˹���ɢ�-�ڡ�4�õ���N2H4��l��+2H2O2��l���TN2��g��+4H2O��L����H=-817.75KJ/mol����ѧ����ʽ��32gȫ����Ӧ����817.675KJ��16gҺ̬��������˫��ˮ��Ӧ���ɵ�����Һ̬ˮʱ���ų���������408.875KJ��
�ʴ�Ϊ��408.875��
��3����ԭ���£�N2H4����ǿ������H2O2�������ǻ��ʱ�������������ĵ�����ˮ���������ͷŴ��������Ϳ��ٲ������������⣬���к�ͻ�����ŵ��ǣ�����Ϊ������ˮ������Ⱦ��
�ʴ�Ϊ������Ϊ������ˮ������Ⱦ��
��4����N2��g��+2O2��g��=2NO2��g����H=+67.7kJ/mol
? ��N2H4��g��+O2��g���TN2��g��+2H2O?��g������H=-534kJ?mol-1
�ɸ�˹���ɣ��ڡ�2-�ٵ� 2N2H4��g��+2NO2?��g���T3N2��g��+4?H2O��g����H=-1135.7kJ?mol-1
�ʴ�Ϊ��2N2H4��g��+2NO2?��g���T3N2��g��+4?H2O��g����H=-1135.7kJ?mol-1
���������
�����Ѷȣ�һ��
5��ѡ���� ��CO��O2�ķ�Ӧ�У��ƻ�1molCO�еĻ�ѧ�����ĵ�����ΪA���ƻ�1molO=O�����ĵ�����ΪB���γ�1molC=O���ͷŵ�����ΪC�������й�ϵ��ȷ����
A��2A+B>2C B��2A+B>4C C��2A + B < 2C D��2A + B < 4C
�ο��𰸣�D
�����������Ӧ�Ⱦ��Ƕϼ��γɵ��������γɻ�ѧ�����ų��������IJ�ֵ��COȼ���Ƿ��ȷ�Ӧ������ݷ���ʽ2CO��O2=2CO2�����ʵĽṹʽ��֪��һ����2A��B��4C����ѡD��
���㣺���鷴Ӧ�ȵļ���
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Է�Ӧ���뻯ѧ�����ܹ�ϵ����Ϥ�˽�̶ȣ�����������ѧ������˼ά�����ͳ���˼ά��������ȷ��ѧ�������뷴Ӧ�ȵĹ�ϵ�Ǵ���Ĺؼ���
�����Ѷȣ�һ��