微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知N≡N键的键能是945kJ
2、选择题 下列有关热化学方程式的叙述正确的是
[? ]
A.已知2H2(g)+O2(g)==2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol
B.已知C(石墨,s)= C(金刚石,s);△H>0,则金刚石比石墨稳定
C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH+HCl=NaCl+H2O;△H=-57.4 kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g) ;△H2。则△H1<△H2
3、选择题 中和热是在稀溶液中,强酸强碱中和反应生成1mol水时放出的热量,中和热为57.3kJ/mol 。下列热化学方程式正确的是
[? ]
A.HNO3(aq)+KOH(aq)=H2O(l) +KNO3(aq) ΔH > -57.3kJ/mol
B.HNO3(aq)+NH3・H2O(aq)=H2O(l) +KNO3(aq) ΔH < -57.3kJ/mol
C.CH3COOH(aq)+KOH(aq)=H2O(l) + CH3COOK(aq) ΔH< -57.3kJ/mol
D.CH3COOH(aq)+NH3・H2O(aq)=H2O(l) + CH3COONH4(aq) ΔH > -57.3kJ/mol
4、填空题 (14分)硝酸厂废气、汽车尾气中的氮氧化物可污染大气,现有几种消除氮氧化物的方法如下:
目前,消除氮氧化物污染有多种方法。
(1)方法一:CH4催化还原法。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ・mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
③H2O(g)=H2O(l) ΔH3=-44 kJ・mol-1
现有一混合气体中NO与NO2的体积比为3:1,用22.4L(标准状况下)甲烷气体催化还原该混合气体,恰好完全反应(已知生成物全部为气态),并放出1013.5KJ的热量,则ΔH2为______;写出CH4(g)与NO2(g)反应生成N2(g) 、CO2(g)和H2O(l)的热化学方程式_______________________。
(2)方法二:活性炭还原法。
某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,只生成甲和乙,甲和乙均为参与大气循环的气体,且反应进行到不同时间测得各物质的浓度如下:
 物质的量/mol 物质的量/mol
时间/min
| NO
| 甲
| 乙
|
0
| 0.200
| 0
| 0
|
10
| 0.116
| 0.042
| 0.042
|
20
| 0.080
| 0.060
| 0.060
|
30
| 0.080
| 0.060
| 0.060
|
由以上信息可知:
①该原理的化学方程式为____________________________________________________.
②该温度下的平衡常数K=_____________________________。(保留小数点后两位有效数字)
③若20min后升高温度至T2℃,达到平衡后,若容器中NO、甲、乙的浓度之比为1:1:1,
则该反应的ΔH_______ 0 。(填">"、"<"、"=")
(3)方法三:NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。
反应原理为:2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
2N2(g)+3H2O(g) 每生成1molN2转移的电子数为_____________________________________________________________。
(4)方法四:ClO2氧化氮氧化物。其转化流程如下:
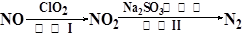
已知反应Ⅰ的化学方程式为2NO+ ClO2+ H2O = NO2+ HNO3+ HCl,则反应Ⅱ的化学方程式是 。
5、简答题 如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(1)下列措施中,有利于降低大气中的CO2、SO2、NO2浓度的有______.(填字母)
a.减少化石燃料的使用,开发新能源?b.使用无氟冰箱,减少氟利昂排放
c.多步行或乘公交车,少用专车或私家车?d.将工业废气用碱液吸收后再排放
(2)为开发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料.一定条件下由CO和H2生产甲醇的化学方程式为______.该反应合成l?molCH3OH(1)放出热量131.9kJ,又知2H2(g)+CO(g)+
O2(g)=CO2(g)+2O(g)?
△H=594.1kJ/mol.请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式:______.
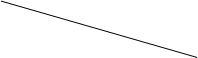
(3)硫酸工业生产中,SO2催化氧化生成SO3反应为2SO2+O2?2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图.
根据图示回答下列问题:
①2SO2(g)+O2(g)+O2(g)?2SO3(g)的△H______0?(填“>”或“<”).
②若温度T1、T2时,反应的化学平衡常数分别为K1、K2,则K1______K2;若反应进行到状态D时,v正______v逆(填“>”“<”或“=”).