微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)已知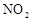 和
和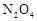 可以相互转化:
可以相互转化: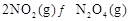 △H<0。现将一定量
△H<0。现将一定量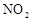 和
和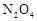 的混合气体通入一个体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。
的混合气体通入一个体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图。

(1)图中共有两条曲线X和Y,其中曲线________表示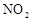 浓度随时间的变化;若在实现X、Y两条曲线变化过程中,共吸收
浓度随时间的变化;若在实现X、Y两条曲线变化过程中,共吸收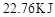 的热量,则该反应的热化学方程式为__________。
的热量,则该反应的热化学方程式为__________。
(2)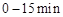 ,反应
,反应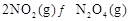 的平衡常数K(b)=__________;比较
的平衡常数K(b)=__________;比较 在
在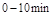 时平均反应速率
时平均反应速率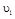 与
与 时平均反应速率
时平均反应速率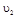 的大小__________。
的大小__________。
(3)反应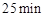 时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是________(用文字表达);其平衡常数K(d)_______K(b)(填“>”、“=”或“<”)。
时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是________(用文字表达);其平衡常数K(d)_______K(b)(填“>”、“=”或“<”)。
(4)若要达到使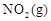 的体积百分含量与d点相同的化学平衡状态,在
的体积百分含量与d点相同的化学平衡状态,在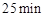 时还可以采取的措施是___________。
时还可以采取的措施是___________。
A.加入催化剂
B.缩小容器体积
C.升高温度
D.加入一定量的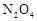
2、选择题 反应4A(g) + 5B(g) 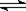 ?4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:(?)
?4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:(?)
A. 若增大压强,A和B的转化率都增大
B. 若升高温度最终能生成更多的C和D
C. 单位时间里有4n mol A消耗,同时有5n mol B生成
D. 容器里A、B、C、D的浓度比是4:5:4:6
3、选择题 某温度下,反应2CH3OH(g)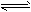 CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下
CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下
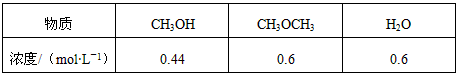
下列说法正确的是
[? ]
A.CH3OH的起始浓度为1.04 mol/L
B.此时逆反应速率大于正反应速率
C.平衡时CH3OH的浓度为0.04 mol/L
D.平衡时CH3OH的转化率小于80%
4、选择题 在一密闭容器中充入NO2,在一定条件下进行反应:2NO2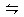 2NO+O2。达到平衡状态的标志是? (? )
2NO+O2。达到平衡状态的标志是? (? )
A.NO2的消耗速率与NO的生成速率相等
B.容器内压强不随时间变化而变化
C.NO2和O2的消耗速率之比为2:1
D.单位时间内生成2n mol NO同时生成n mol O2
5、选择题 在一固定容积的密闭容器中,进行如下化学反应:
CO2(g)+ H2(g) CO(g)+ H2O(g) △H =" Q" kJ・mol―1
CO(g)+ H2O(g) △H =" Q" kJ・mol―1
其化学平衡常数K和温度t的关系如下:
t℃
| 700
| 800
| 850
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
请回答:
(1)上述反应中Q ?0 (选填“>”或“<”)
(2)能判断该反应已达到化学平衡状态的依据是?。
(a) 容器中压强不变?(b) 反应热△H不变
(c)  正(H2)=
正(H2)= 逆(CO)?(d) CO2的质量分数不变
逆(CO)?(d) CO2的质量分数不变
(3)温度为850℃时,可逆反应CO(g)+H2O(g) CO2(g)+H2(g)在固定容积的密闭容器中进行,容器内各物质的浓度变化如下表:
CO2(g)+H2(g)在固定容积的密闭容器中进行,容器内各物质的浓度变化如下表:
850℃时物质浓度(mol/L)的变化
时间(min )
| CO
| H2O
| CO2
| H2
|
0
| 0.200
| 0.300
| 0
| 0
|
2
| 0.138
| 0.238
| 0.062
| 0.062
|
3
| C1
| C2
| C3
| C3
|
4
| C1
| C2
| C3
| C3
|
5
| 0.116
| 0.216
| 0.084
| ?
|
6
| 0.096
| 0.266
| 0.104
| ?
|
①计算:3min时(CO的浓度)c1=_?_mol/L,H2O(g)的转化率=?。
②反应在4min―5min之间,平衡向逆方向移动,可能的原因是?(单选),
表中5min―6min之间数值发生变化,可能的原因是?(单选)。
a.增加水蒸气? b.降低温度? c.使用催化剂? d.增加氢气浓度