微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)孔雀石主要含Cu2(OH)2CO3,还含少量铁的化合物和硅的化合物。以孔雀石为原料可制备CuCl2・3H2O及纯碱,流程如下图。

且知:溶液A只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀的pH如下表所示。回答下列问题:
金属离子
| Fe3+
| Fe2+
| Cu2+
|
PH
| 氢氧化物开始沉淀
| 1.9
| 7.0
| 4.7
|
氢氧化物完全沉淀
| 3.2
| 9.0
| 6.7
|
(1)孔雀石研磨的目的是 。
(2)孔雀石的主要成分与足量稀硫酸反应的化学方程式为 。
(3)使用上图中“试剂1”的目的是将溶液中的Fe2+转化为Fe3+,试剂B宜选用 (填选项序号)。
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)加入CuO作用是调节溶液pH,使Fe3+转化为沉淀予以分离。则pH的范围为 。
(5)气体E、F与饱和食盐水作用生成H和G时,E和F应按一定先后顺序通入饱和食盐水中,其中,应先通入气体是 (填代号及对应物质的化学式)。
(6)由溶液C获得CuCl2・3H2O,需要经过 、 、过滤等操作。
(7)已知:常温下Cu(OH)2的Ksp=2×10-20。计算Cu2++2H2O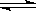 Cu(OH)2+2H+反应平衡常数 。
Cu(OH)2+2H+反应平衡常数 。
参考答案:(14分)
(1)增大固体表面积,从而增大反应速率(2分)
(2)Cu2(OH)2CO3+2H2SO4===2CuSO4+3H2O+CO2↑(2分)
(3)B(2分)
(4)3.2≤pH<4.7(2分)
(5)F(1分)NH3(1分)
(6)蒸发浓缩冷却结晶(各1分共2分)
(7)5×10-9(2分)
本题解析:(1)固体研磨是为了增大固体表面积,从而增大反应速率。(2)碱式碳酸铜和硫酸反应生成硫酸铜和水和二氧化碳,方程式为:Cu2(OH)2CO3+2H2SO4===2CuSO4+3H2O+CO2↑。(3)亚铁离子氧化成铁离子,尽量不引入新的元素,所以选择双氧水,选B。(4)调节溶液的pH使铁离子完全沉淀,但铜离子还没有开始沉淀,所以pH的范围为:3.2≤pH<4.7。(5)气体E、F与饱和食盐水作用生成H和G,最后得到碳酸钠,说明是侯式制碱法,需要通入氨气和二氧化碳,应先通入氨气,增加溶液的碱性,吸收更多的二氧化碳,得到更多的产物。(6)从氯化铜溶液中得到氯化铜晶体,所以需要先蒸发浓缩,然后冷却结晶。(7)平衡常数为[Cu(OH)2][H+]2/[Cu2+]=[Cu(OH)2][H+]2[OH-]2/[Cu2+][OH-]2=KW2/Ksp=10-28/2×10-20=5×10-9。
考点:物质的制备,难溶电解质的溶度积的计算
本题难度:困难
2、填空题 已知Ksp(Ag2S)=1.6×10-49,Ksp(CuS)=6.3×10-36,Ksp(PbS)=8×10-28,则推断可以实现的沉淀转化关系为________________。
参考答案:PbS→CuS→Ag2S
本题解析:
本题难度:一般
3、填空题 已知:Ksp(AgCl)=c(Ag+) ・c(Cl-)=1.8 ×10-10,Ksp(Ag2CrO4)=c2(Ag+) ・ c(CrO42-)=1.9 ×10-12,现用0.01 mol/L AgNO3溶液滴定0.01 mol/L KCl和0.001 mol/L K2CrO4混合溶液,通过计算回答:
(1)Cl-、CrO42-先生成沉淀的是________。
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是________mol/L。(设混合溶液在反应中体积不变)
参考答案:(1)Cl-先沉淀
(2)4.13×10-6mol/L
本题解析:
本题难度:一般
4、填空题 从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问题:
物质
| CaCO3
| MgCO3
| Ca(OH)2
| Mg(OH)2
|
溶度积
| 2.8×10
|
参考答案:
本题解析:
本题难度:一般
5、选择题 已知PbI2的Ksp=7.0×10-9,将7.5×10-3 mol/L的KI与Pb(NO3)2溶液按体积比为2:1混合,则生成PbI2沉淀所需Pb( NO3)2溶液的最小浓度(mol/L)为
?[? ]
A.8.4×10-4
B.5.6×10-4
C.4.2×10-4
D.2.8×10-4
参考答案:A
本题解析:
本题难度:一般