微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 Na2S2O3溶液跟稀H2SO4反应的化学方程式为: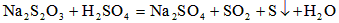 下列各组实验中,溶液中最先变浑浊的是
下列各组实验中,溶液中最先变浑浊的是
[? ]
反应温度℃ 反应物Na2S2O3、H2SO4[v(mL)、c(mol×L-1)] H2O[v(mL)]
A. 10 5 0.1、10 0.1 5
B. 10 5 0.1、5 0.1 10
C. 30 5 0.1、5 0.1 10
D. 30 5 0.2、5 0.2 10
参考答案:D
本题解析:
本题难度:一般
2、选择题 反应2SO2+O2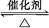 2SO3经一段时间后,SO3的浓度增加了0.4 mol・L-1,在这段时间内用O2表示的反应速率为0.04 mol・(L・s)-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4 mol・L-1,在这段时间内用O2表示的反应速率为0.04 mol・(L・s)-1,则这段时间为( )
A.0.1 s
B.2.5 s
C.10 s
D.5 s
参考答案:D
本题解析:根据题意,SO3的浓度增加了0. 4 mol・L-1,则O2的浓度减少了0.2 mol・L-1,v(O2)=
Δt="5" s。
本题难度:简单
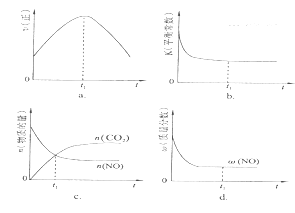
3、填空题 2014年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气是造成空气污染的原因之一。汽车尾气净化的主要原理为2NO(g)+2CO(g)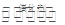 2 CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2 CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
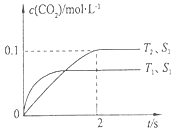
(1)该反应的△H??0(选填“>’’、“<")。
(2)在T2温度下,0~2 s内的平均反应速率v(N2)=?
(3)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
(4)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是?(填代号)。
参考答案:(1)<;(2)0.025mol/(L?s);(3)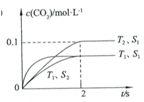 ;(4)bd。
;(4)bd。
本题解析:(1)根据题给图像知,温度T1时先达平衡,即温度为T1时反应速率快,根据温度对反应速率的影响规律知,温度T1>T2;温度为T1时,二氧化碳的平衡浓度较低,说明升高温度平衡向逆反应移动,根据温度对化学平衡的影响规律知,该反应放热反应,△H<0;(2)根据题给图像知,T2温度时2s到达平衡,二氧化碳的浓度变化为0.1mol/L,根据公式v=△c/△t知,v(CO2)=0.05mol/(L?s),利用速率之比等于化学计量数之比知,v(N2)=0.025mol/(L?s);(3)固体催化剂表面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同,故c(CO2)在T1、S2条件下达到平衡过程中的变化曲线为: ;(4)a、可逆反应到达平衡后正、逆速率相等且不再变化,由图像a知,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,错误;b、该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,平衡常数不变,与图像符合,正确,c、t1时刻后二氧化碳、NO的物质的量发生变化,t1时刻未到达平衡状态,错误;d、NO的质量分数为定值,t1时刻处于平衡状态,正确;选bd。
;(4)a、可逆反应到达平衡后正、逆速率相等且不再变化,由图像a知,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,错误;b、该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,平衡常数不变,与图像符合,正确,c、t1时刻后二氧化碳、NO的物质的量发生变化,t1时刻未到达平衡状态,错误;d、NO的质量分数为定值,t1时刻处于平衡状态,正确;选bd。
本题难度:一般
4、实验题 (12分)根据我国目前汽车业发展速度,预计2020年汽车保有量超过2亿辆,中国已成为全球最大的汽车市场。因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题。目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:
2NO+2CO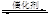 2CO2+N2。为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究。
2CO2+N2。为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究。
【资料查阅】①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响。
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
(1)完成以下实验设计表(表中不要留空格)。
实验编号
| 实验目的
| T/℃
| NO初始浓度
mol/L
| CO初始浓度
mol/L
| 同种催化剂的比表面积
m2/g
|
Ⅰ
| 为以下实验作参照
| 280
| 6.50×10-3
| 4.00×10-3
| 80
|
Ⅱ
|
|
|
|
| 120
|
Ⅲ
| 探究温度对尾气转化速率的影响
| 360
|
|
| 80
|
【图像分析与结论】利用气体传感器测定了三组实验中CO浓度随时间变化的曲线图,如下:
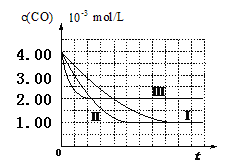
(2)计算第Ⅰ组实验中,达平衡时NO的浓度为__________________;
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率_____________
(填“增大”、“减小”、“无影响”);
参考答案:(1)
实验编号
实验目的
T/℃
NO初始浓度
mol/L
CO初始浓度
mol/L
同种催化剂的比表面积
m2/g
Ⅰ
Ⅱ
探究催化剂比表面积对尾气转化速率的影响(2分)
280
(1分)
6.50×10-3
(1分)
4.00×10-3
(1分)
Ⅲ
6.50×10-3
(1分)
4.00×10-3
(1分)
(2)3.50×10-3 mol/L(3分) (3)增大(2分)
本题解析:(1)由于Ⅰ与Ⅱ是同种催化剂的比表面积m2/g不同,其它应该是相同的所以Ⅱ是探究催化剂比表面积对尾气转化速率的影响。其余的都和Ⅰ是相同的,即温度是280℃;NO初始浓度是6.50×10-3mol/L;CO初始浓度是4.00×10-3mol/L;Ⅲ与Ⅰ相比较,是温度不同,而同种催化剂的比表面积相同,因此Ⅲ是探究温度对尾气转化速率的影响,其余的都和Ⅰ相同。NO初始浓度6.50×10-3mol/L;CO初始浓度4.00×10-3mol/L;(2)根据题意可知在反应开始时c(CO)=4.0×10-3mol/L;在达到平衡时c(CO)=1.0×10-3mol/L;浓度减小Δc(CO)=3.0×10-3mol/L;根据反应方程式中CO、NO的浓度关系 www.91exAm.org可知Δc(NO)=3.0×10-3mol/L;所以达平衡时NO的浓度为6.50×10-3 mol/L-3.0×10-3mol/L=3.50×10-3 mol/L;(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,达到平衡所需要的时间缩短,但是达到平衡时汽车尾气转化率不变。即:增大催化剂比表面积,汽车尾气转化速率增大。
考点:考查温度、催化剂的表面积对尾气的治理的影响的知识。
本题难度:困难
5、选择题 某一反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的反应速率为 (? )
A.0.04
B.0.04mol / (L.s)
C.0.08mol(L.s)
D.0.04mol / L
参考答案:B
本题解析:△v(A)=△c(A)/△t =(1.0mol/L―0.2mol/L)/20s="0.04mol" / (L.s),故选B。
点评:化学反应速率就是化学反应进行的快慢程度(平均反应速度),用单位时间内反应物或生成物的物质的量来表示。化学反应速率的表达式:△v(A)=△c(A)/△t 运用公式便可以解决。
本题难度:一般