微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知Fe3+与I-在水溶液中发生:2I-+2Fe3+=2Fe2++I2。该反应正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)・cn(Fe3+)(其中k为常数)。
?
| cm(I-)(mol/L)m
| cn(Fe3+)[(mol/L)n]
| v[mol/(L・s)]
|
a
| 0.20
| 0.80
| 0.032
|
b
| 0.60
| 0.40
| 0.144
|
c
| 0.80
| 0.20
| 0.128
|
I-浓度对反应速率的影响________Fe3+浓度对反应速率的影响(填大于或小于或等于)
参考答案:大于
本题解析:将a和b中的数据带入v=kcm(I-)・cn(Fe3+)可知,m=n+1,所以I-浓度对反应速率的影响大于Fe3+浓度对反应速率的影响。
本题难度:一般
2、填空题 用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断________段化学反应速率最快,_______段收集的氢气最多。这段反应速率最快的原因是______________________________________
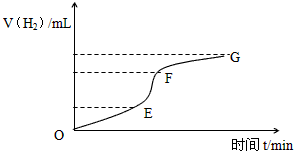
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是_____________________
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答一种)
______________________________________
参考答案:(1)EF;EF;因该反应是放热反应,这段反应温度高,速率快
(2)AC
(3)降低温度(答案合理即可)
本题解析:
本题难度:一般
3、选择题 反应3A+B=2C+D在四种不同情况下的反应速率分别为:
①v(A)=0.15 mol/(L・s);②v(B)=0.06 mol/(L・s);
③v(C)=0.05 mol/(L・s);④v(D)=0.045 mol/(L・s)。
则反应进行由快到慢的顺序为
A.④>③>①>② B.②>④>③>①
C.②>①>④>③ D.④>③>②>①
参考答案:C
本题解析: 同一化学反应方程式中,不同物质表示该反应的反应速率数值可能不同,但表示的意义完全相同,都是表示该反应的反应速率。并且,在同一化学反应方程式中,不同物质的速率之比等于化学计量数之比,所以,比较同一反应的反应速率快慢,需要将反应速率转化为同一种物质的反应速率才能比较;假设均将反应速率转化为v(B)的反应,则①v(A)=3v(B)=0.15mol/(L・s),得v(B)=0.05mol/(L・s);③v(C)=2v(B)=0.05mol/(L・s),得v(B)=0.025mol/(L・s);④v(D)=v(B)=0.045mol/(L・s),所以,正确的关系为:②>①>④>③
考点:化学反应速率的比较。
本题难度:一般
4、选择题 反应m A + n B  ?p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
?p C中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
A.2:3:1
B.1:3:2
C.2:3:3
D.3:2:1
参考答案:B
本题解析:根据题目可知,A、B、C的反应速率之比为0.5:1.5:1=1:3:2,又化学反应速率之比等于化学方程式中化学计量数之比,所以m:n:p为1:3:2,答案选B。
本题难度:简单
5、填空题 (6分)下图表示Zn投入一定浓度一定体积的稀H2SO4溶液中后,反应时间与生成H2的体积的图象。(纵坐标为H2的生成速率)

(1)反应前期速率加快的原因是:?。
(2)反应后期速率下降的原因是:?。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是:?。
A.蒸馏水
B.氯化钠固体
C.氯化钠溶液
D.浓盐酸
参考答案:
(1)该反应放热,随着反应进行,体系温度升高,因而反应速率逐渐加快。(2分)
(2)反应后期,稀硫酸浓度减小,因而反应速率逐渐减小。(2分)
(3)A、C? (各1分,共2分)
本题解析:略
本题难度:简单