��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ӵ���Ѿ���ΪӦ����㷺�Ŀɳ���ء�ij������ӵ�صĽṹʾ��ͼ����ͼ��������������ĸ�Ĥֻ����Li+ͨ������س��ʱ���ܷ�Ӧ��ѧ����ʽΪ��LiC002��Li1-xC002+xLi�����ڸõ�ص����۴������

A���ŵ�ʱ��Li+��Ҫ�Ӹ�����ͨ����Ĥ����������
B���ŵ�ʱ��������ӦxLi��xe-��xLi+
C�����ʱ���е���ת��Ϊ��ѧ��
D�����ʱ��������C�����Ԫ�ر�����
�ο��𰸣�D
���������A���ŵ��൱��ԭ��أ�Li+��Ҫ�Ӹ�����ͨ����Ĥ������������A��ȷ��B���ŵ�ʱLi��������Ϊԭ��صĸ������缫��ӦʽΪxLi��xe-��xLi+��B��ȷ��C�����ʱ��Ϊ���ط�Ӧ������ת��Ϊ��ѧ�ܣ�C��ȷ��D���ɷ�ӦLiC002��Li1-xC002+xLi��֪�����ʱ������������ԭ��Ӧ������Li������ԭ��D����ѡD��
���㣺����绯ѧԭ����Ӧ��
�����Ѷȣ�һ��
2��ѡ���� �ö��Ե缫���һ����������ͭ��Һ�����һ��ʱ�������Һ�м���0.1mol��ʽ̼��ͭ���壨�����ᾧˮ ����ǡ��ʹ��Һ�ָ������ǰ��Ũ�Ⱥ�pH�������й���������ȷ���ǣ�������
A�������̲���������������ڱ�״���£�Ϊ5.6L
B��������ת�Ƶĵ�����Ϊ3.612��1023��
C�������ʽ̼��ͭ�ķ�Ӧ�ǣ�Cu2��OH��2CO3+2H2SO4�T2CuSO4+CO2��+3H2O
D��������ֻ������2CuSO4+2H2O
2Cu+O2��+2H2SO4
�ο��𰸣��������ͭ��Һ����Һ�����ԣ���������Һ�м����ʽ̼��ͭ�ָܻ�ԭ��Һ����ʽ̼��ͭ�����ᷴӦ��������ͭ��ˮ�Ͷ�����̼����Һ�������ӵ�����ͭ�����������ӣ�����ʵ���ϵ������ͭ��Һ�������Σ�
��һ��2CuSO4+2H2Oͨ��.2Cu��+O2��+2H2SO4��
�ڶ��Σ�2H2Oͨ��.2H2��+O2����
����ʽ̼��ͭ��ѧʽ�ı�Ϊ2CuO?H2O?CO2�����Լ���0.1molCu2��OH��2CO3 ���൱�ڼ���0.2molCuO��0.1molˮ��
��һ�Σ�����ͭԭ���غ�֪���������ͭ��Һ����n��Cu��=n��CuO��=0.2mol��ת�Ƶ��ӵ����ʵ���=0.2mol��2=0.4mol��
�ڶ��Σ��������0.1molˮת�Ƶ��ӵ����ʵ���=0.1mol��2=0.2mol��
���Խ�����й�ת�Ƶĵ�����Ϊ0.4mol+0.2mol=0.6mol��
A������Ϊ�����������ͭ��ˮ��������0.1mol�����0.1molˮ����0.1mol������0.05mol����������������0.15mol+0.1mol=0.25mol�������״�����=0.25mol��22.4L/mol=5.6L����A��ȷ��
B���������������֪����ת������Ϊ0.6mol��������ת�Ƶĵ�����=0.6mol��6.02��1023=3.612��1023������B��ȷ��
C������ļ�ʽ̼��ͭ�ķ�Ӧ�ǣ�Cu2��OH��2CO3+2H2SO4�T2CuSO4+CO2��+3H2O����C��ȷ��
D���������ͭ��Һ�������Σ���һ��2CuSO4+2H2Oͨ��.2Cu��+O2��+2H2SO4���ڶ��Σ�2H2Oͨ��.2H2��+O2������D����
��ѡD��
���������
�����Ѷȣ�һ��
3������� ����ӵ�нϳ��ĺ����ߣ���嫵ĺ�����һ��������ʱ��⡣Ŀǰ������������о���γ�����ú�����Դ�� ����ͼ��ʾ���ڵ糡������Ĥ�����������ӽ���Ĥֻ����������ͨ���� �����ӽ���Ĥֻ����������ͨ����������ˮ���÷�����Ϊ����������
��ͼ��ĤaӦѡ��____Ĥ��
�ڵ���������������������Ʒ�Һ��д���ø÷�����������������Һʱ��������Ӧ�Ļ�ѧ����ʽ___ ��
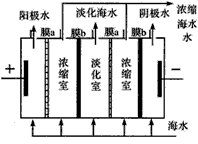
�ο��𰸣��������ӽ���Ĥ����4AgNO3+2H2O 4Ag+O2��+4HNO3
4Ag+O2��+4HNO3
���������
�����Ѷȣ�һ��
4������� ��8�֣��縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ�ִ�����ˮ��������ͼ�ǵ����ˮʵ��װ��ʾ��ͼ����ֱͨ����Դ��һ��ʱ�䣬��A�缫��������ɫ�����������������B�缫���������ݲ��������ݿɽ���ˮ�е����������ˮ���γɸ����㣬���۵�һ�����ʱ��ȥ�����㣬�����˸�ѡ���������á�
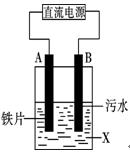
�Ը�������ʵ�������Լ�ͼʾ�ش��������⣺
��1�����صĵ缫A��B���Էֱ�Ϊ?��?���� ������������������ ��
��2��ʵ��ʱ����ˮ������Ũ�Ƚ�С�����������ϲ�����������ʻ�������ʹ�������γɸ�������ʱ��Ӧ����ˮ�м���������?��
a��H2SO4? b��BaSO4? c��Na2SO4? d��NaOH? e��CH3CH2 OH
OH
��3�����������ĵ缫��Ӧ�ֱ��Ǣ�?����4OH��- 4 e���� 2H2O ����2����
��4���缫��Ӧ�ٺ͢ڵ������ﷴӦ�õ�Fe(OH)3���������ӷ���ʽ��?��
�ο��𰸣�
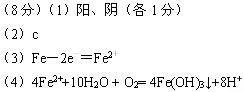
�����������
�����Ѷȣ�һ��
5������� ��13�֣�����ͼװ�ý���ʵ�飬���ش��������⡣
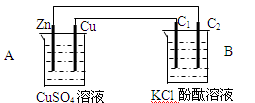
��1���ж�װ�õ����ƣ�A��Ϊ___________B��Ϊ______________
��2��п���缫��ӦʽΪ_________________________
ʯī��C1�缫��ӦʽΪ________________________
ʯī��C2����������ʵ������Ϊ______________________________
��3����C2������224mL���壨��״����ʱ��CuSO4��Һ����������_________g��
�ο��𰸣���13�֣���1��ԭ��أ�����
��2��Zn-2e-=Zn2+�� 2Cl--2e-= Cl2�� C2�������ݲ���������Χ��Һ��ɫ����ɫ��Ϊdz�죨���Ϊ��ɫ�����������1�֣���˼�Լ����֣�
��3��0.01��3�֣�
�����������1��A�д���Zn������ͭ�ķ�Ӧ������AΪԭ��أ���BΪ���أ�
��2��A��Zn��Cu���ã�����Zn��ԭ��صĸ���������������Ӧ��ʧȥ��������п���ӣ���缫��ӦʽΪZn-2e-=Zn2+��ʯīC1��ԭ��ص�������������ʯīC1Ϊ����������������Ӧ��������ʧȥ���������������缫��ӦʽΪ2Cl--2e-= Cl2����ʯīC2Ϊ������������ԭ��Ӧ�������ӵõ��������������������������ӵ�Ũ����������ʯīC2���������ݲ�������Һ���ɫ��
��3����C2������224mL���壨��״����ʱ��������0.224L/22.4L/mol=0.01mol����ʱ��ת�Ƶ��ӵ����ʵ�����0.02mol��A��ÿת��2mol���ӣ���65gп���ӽ�����Һ������64gCu��������Һ��������1g��CuSO4��Һ���������ӣ�����ת��0.02mol����ʱ������ͭ��Һ����������0.01g��
���㣺����绯ѧ��Ӧԭ�����ж�
�����Ѷȣ�һ��