微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 从下列事实所得出的解释或结论正确的是
选项
| 实验事实
| 解释或结论
|
A
| 氢氧化钠标准液滴定食醋的操作中,用甲基橙作指示剂会造成误差
| 恰好完全中和时溶液呈碱性,
应选用酚酞作指示剂
|
B
| 压缩针筒内的NO2和N2O4混合气体,
颜色先变深后变浅
| 增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强小
|
C
| 往氯化铁溶液中加入氯化铁固体,溶液颜色加深
| 水解平衡向右移动,氢氧化铁浓度增大,氯化铁水解程度增大
|
D
| 在室温下能自发进行反应:(NH4)2CO3 (s) =NH4HCO3 (s)+NH3(g) ΔH >0
| 这是一个熵增的反应
|
参考答案:AD
本题解析:A、氢氧化钠标准液滴定食醋的操作中,用甲基橙作指示剂,恰好完全中和时生成强碱弱酸盐,溶液呈碱性,溶液由红色刚好变橙色,应选用酚酞作指示剂,A正确; B、据勒夏特列原理,压缩气体的体积使其压强增大,平衡向气体体积减小的生成N2O4方向移动,但新平衡比旧平衡压强大, B错误;C、往氯化铁溶液中加入氯化铁固体,溶液颜色加深,氯化铁电离成离子,铁离子的浓度增大得多,氯化铁水解程度增大得少,故颜色的加深主要不是水解平衡移动引起的,C错误;D、熵增就是体系的混乱度增大,同一物质:固态、液态、气态的混乱度依次增大,该反应产生气体,故是一个熵增的反应,D正确;答案选AD。
考点:考查化学平衡原理。
本题难度:一般
2、选择题 下列电离方程式正确的是( )
A.NaHCO3(溶液):NaHCO3=Na++H++CO32-
B.NaHSO4(熔融):NaHSO4=Na++H++SO42-
C.(NH4)2SO4(溶液):(NH4)2SO4=(NH4)2++SO42-
D.NH3?H2O(溶液):NH3?H2O?NH4++OH-
参考答案:D
本题解析:
本题难度:简单
3、选择题 在25℃时,纯水的pH为( ? )
A.0
B.7
C.10
D.14
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列电离方程式,书写正确的是( )
A.Al2(SO4)3=2Al3++3SO42-
B.AlCl3=Al3++Cl3-
C.Mg(NO3)2=Mg+2+2NO3-
D.KMnO4=K++Mn7++4O2-
参考答案:A
本题解析:
本题难度:一般
5、填空题 (10分)有A、B、C、D四种强电解质,它们在水中电离可产生表中离子(每种物质只含一种阴离子且互不重复)。
阳离子
| Na+、Ba2+、NH4+
|
阴离子
| CO32-、Cl-、OH-、SO42-
|
已知:
①A、C溶液的pH均大于7,A、B的溶液中水的电离程度比纯水大,A、D焰色反应的火焰均为黄色;
②C溶液和D溶液相遇时只观察到有白色沉淀产生,B溶液和C溶液相遇时只观察到有刺激性气味的气体产生,A溶液和D溶液混合时无明显现象。
请填写下列空白:
(1)A是___________,B是___________,C是____________,D是___________。
(2)常温,将1 mL pH =12的C溶液加水稀释至100mL,所得溶液中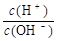 = 。
= 。
(3)常温下,0.15 mol・L-1的C溶液与0.20 mol・L-1盐酸混合,所得混合液的pH=13,则C溶液与盐酸的体积比= _______________。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是 。
参考答案:(10分)(1)Na2CO3 NH4Cl Ba(OH)2 Na2SO4(每空1分)
(2)10-6(2分) (3)3 : 2(2分)
(4)c(OH-)>c(Cl-)=c(Ba2+)>c(NH4+)>c(H+)(2分)
本题解析:①A、C溶液的pH均大于7,可能有OH-和CO ,CO水解呈碱性。又因为A中水电离程度比纯水大,故发生水解,焰色呈黄色,有Na+存在,A为Na2CO3,②另一能水解的离子为NH 在B中, B、C相遇有刺激性气味气体,为氨气,故C中有氢氧根;③C和D相遇产生白色沉淀,在上述离子中只有BaCO3和BaSO4,阴离子互不重复,故为D为Na2SO4,C为Ba(OH)2,B为NH4Cl。
本题难度:困难