微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分).实验室中要除去细碎铜屑中的少量细碎铁屑,某同学设计了两个方案:
(1)Cu、Fe 过滤
过滤 洗涤
洗涤
(2)Cu、Fe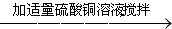 过滤
过滤 洗涤
洗涤
两个方案较好的是_______________(填序号),理由是______________________________。你是否有简便的方法,若有,请写出做法:__________________________________________。
参考答案:(2);既除去了铁,而同时又增加了铜;?用磁铁吸取铁屑
本题解析:由于在方案(2)中既除去了铁,而同时又增加了铜,而方案(1)不能使铜的质量增加,所以最后的是方案(2);由于磁铁能吸引铁,所以也可以用磁铁吸取铁屑。
本题难度:一般
2、选择题 FeSO4和Fe2(SO4)3的混合物中含硫的质量分数为a%,则含铁的质量分数为(? ).
A.2a%
B.3a%
C.1-2a%
D.1-3a%
参考答案:D
本题解析:在FeSO4和Fe2(SO4)3的混合物中,硫元素和氧元素质量比是固定的,即1:2,所以,氧的质量分数为2%,铁的质量分数为1-3a%,故选D
本题难度:一般
3、选择题 往100 mL FeCl3溶液中,通入0.672L标准状况下的硫化氢气体,设气体完全被吸收,再加入过量的铁粉,反应停止后,测得溶液中含有0.12mol金属阳离子,则原氯化铁溶液的物质的量浓度为
A.0.1 mo/L
B.1 mo/L
C.0.08 mo/L
D.0.8 mo/L
参考答案:D
本题解析:0.672L标准状况下的硫化氢气体的物质的量为0.03mol,与FeCl3溶液反应的方程式为: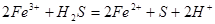 ,0.03mol硫化氢气体要消耗,0.06molFeCl3,生成FeCl20.06mol,及0.06molH+;再加入过量的铁粉其反应为
,0.03mol硫化氢气体要消耗,0.06molFeCl3,生成FeCl20.06mol,及0.06molH+;再加入过量的铁粉其反应为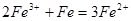 ,
, ;反应停止后,测得溶液中含有0.12mol金属阳离子,所以,有0.06mol FeCl2由
;反应停止后,测得溶液中含有0.12mol金属阳离子,所以,有0.06mol FeCl2由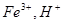 与铁反应而成,而H+的物质的量为0.06mol,与铁反应生成
与铁反应而成,而H+的物质的量为0.06mol,与铁反应生成 物质的量为0.03 mol,即还有0.03 mol
物质的量为0.03 mol,即还有0.03 mol 由
由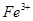 与铁反应生成,即
与铁反应生成,即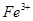 需0.02 mol;所以100 mL FeCl3溶液中FeCl3的物质的量为
需0.02 mol;所以100 mL FeCl3溶液中FeCl3的物质的量为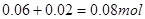 ,即其物质的量浓度为0.8 mo/L;
,即其物质的量浓度为0.8 mo/L;
本题难度:一般
4、填空题 (14分)回答下列关于铁元素及其化合物的知识:
(1)向一支装有FeCl3溶液的试管中滴加NaOH溶液,现象为 _________________,
其中含铁元素的产物的化学式是___________________ ;
(2)为了检验某未知溶液是否含有Fe2+离子,两位同学分别设计了以下实验方案加以证明。方案一:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液含有Fe2+离子;
方案二:向另一支装有该未知溶液的试管中先滴加KSCN溶液,无现象,再通入氯气,溶液变为红色,证明该未知溶液含有Fe2+离子;
则请回答:①你认为哪个方案较为合理 __________________ ;
②写出Fe2+与氯气反应的离子方程式 ____________________________;
③实验室在保存含有Fe2+离子的溶液时,为了防止Fe2+离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示)__________________________________________
(4)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,鲜榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的Fe3+,则这个变色的过程中Fe2+被______ ;若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有_______。
A.氧化性
B.还原性
C.酸性
D.碱性
参考答案:(1)红褐色沉淀? Fe(OH)3;
(2)①方案二
②2Fe2++ Cl2? =? 2Fe3+ + 2Cl-
③2Fe3+ + Fe? = 3Fe2+
(4)被氧化 ?B
本题解析:遇KSCN溶液呈血红色是Fe3+的特征反应,根据Fe3+的特征反应先加KSCN溶液,确定是否含有Fe3+;如果没有Fe3+,根据氯水的性质,再向溶液中加入氯水,观察溶液的颜色是否变化,从而确定是否含有Fe2+。
Fe2+与KSCN溶液反应无血红色出现,但Fe3+与KSCN反应产生血红色,因此,要证明某溶液中有无Fe2+,则先要在溶液中加入KSCN溶液,没有出现血红色,再向其中加入氯水出现血红色,则证明原溶液中含Fe2+。
点评:本题考查了Fe2+的检验方法,Fe2+呈中间价态,既有氧化性又有还原性,能被氯水等强氧化剂氧化成Fe3+,利用Fe3+的特征反应检验Fe2+的存在是较好的方法,但首先要排除Fe3+的干扰。
本题难度:一般
5、填空题 氢氧化亚铁与氢氧化铁都是铁的氢氧化物,它们有什么异同?
参考答案:列表将它们的性质与变化比较如下:
氢氧化铁
氢氧化亚铁
物理性质
红褐色,难溶于水
白色,难溶于水
化学性质
具有碱的通性
具有碱的通性,易被氧化为氢氧化铁
联系
4Fe(OH)2+O2+2H2O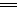 4Fe(OH)3(白色迅速变为灰色、绿色,最终成为红褐色)
4Fe(OH)3(白色迅速变为灰色、绿色,最终成为红褐色)
本题解析:从它们的物理性质与化学性质的不同方面来进行比较,同时对它们之间的转化关系也应该清楚。
本题难度:一般