微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料。
(1)合金是被广泛应用的金属材料。
① 下列有关合金性质的说法正确的是________________(填字母)。
A.合金的熔点一般比它的成分金属高B.合金的硬度一般比它的成分金属低
C.组成合金的元素种类相同,合金的性能就一定相同
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
② 钢属于_______________(填“铁合金”或“铝合金”)。
③ 铁锈蚀主要发生的是电化学腐蚀,其负极反应式为________。
(2)无机非金属材料包括玻 璃、水泥和___________________。
璃、水泥和___________________。
(3)合成塑料、合成橡胶和____________是常说的三大合成材料。下列属于塑料制品的是_______(填字母)。A.汽车轮胎B.涤纶? C.聚乙烯制品? D.玻璃钢
2、选择题 检查钢质设备完好性的方法之一是在被怀疑有裂纹处涂上10%的盐酸,过一段时间,如观察到有粗线裂纹,表明该部分原先确有裂纹,产生粗线裂纹的原因是( )?
A.裂纹处尘埃多,起催化作用?
B.裂纹里面含水分?
C.裂纹处铁的表面积大,反应快?
D.原裂纹处的Fe2O3与盐酸反应,生成可溶的FeCl3?
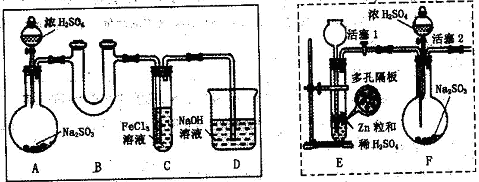
3、实验题 [2012・漳州质检](11分)某研究学习小组为探究Fe3+离子是否能氧化SO2,设计了如下的实验装置(假设实验中所用装置的气密性良好)。
 ?
?
(1)甲同学利用以上实线框内装置制取SO2并进行探究实验。
①装置A中发生反应的化学方程式为?。
②装置B的作用是?。
③反应一段时间后,甲同学取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液观察到有白色沉淀产生。由此他得出结论:Fe3+可氧化SO2。
(2)乙同学认为甲同学的实验不严谨,他用以上虚线框内装置替代装置A,先使装置E内试剂反应一段时间后,关闭活塞1,打开活塞2,又反应片刻后,取装置C中少量溶液,往其中加入酸性KMnO4溶液,观察到KMnO4溶液紫红色褪去。由此他得出结论:Fe3+已被SO2还原成Fe2+。
①该实验制H2时需用浓硫酸配制450mL3mol/L的稀硫酸,配制中所需的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需?。
配制过程中若其它操作无误,但没有洗涤烧杯与玻璃棒,则所配制溶液的浓度会??(填“偏高”、“偏低”或“无影响”)。
②在该实验过程中H2所起得作用是?。
(3)丙同学认为甲、乙的实验均不严谨,为此他沿用乙同学的实验装置及操作,重新实验。待装置F内反应一段时间后,取装置C中少量溶液,往其中加入HCl酸化的BaCl2溶液,得出与甲同学相同的结论。请你分析回答:
①甲同学实验不严谨的原因是?。(选填序号)
A.SO2溶解量太小
B.SO2不与Fe3+发生反应
C.H2SO3与BaCl2不反应
D.装置中的空气与SO2进入水中也可生成H2SO4