��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� (9��)��ͭƬ��пƬ��250mLϡ�������ԭ��أ�����ͭƬ�Ϸų�6.72L(��״����)������ʱ��H2S04ǡ�÷�Ӧ��ȫ��
��1����ԭ��صĸ�����ӦʽΪ
��2��ԭϡ�� ������ʵ���Ũ���� mol��L-1
������ʵ���Ũ���� mol��L-1
��3����ʽ����пƬ���� ��������
��������
�ο��𰸣���1��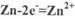
��2��1.2
��3��
�����������
�����Ѷȣ�һ��
2��ѡ���� ���ж���ͼ��ʾװ��ʵ���жϵ�������ȷ����(����)
?
| a�缫
| b�缫
| X��Һ
| ʵ���ж�
|
A
| Cu
| Zn
| H2SO4
| H+��b��Ǩ��
|
B
| Zn
| Fe
| H2SO4
| a��b�����ų���ɫ����
|
C
| Al
| Mg
| NaOH
| a������b����
|
D
| Cu
| ʯī
| FeCl3
| a����������b����������
|

�ο��𰸣�C
���������A��Cu��Zn��ϡ������ɵ�ԭ��أ�п�ϻ��ã���ԭ��صĸ�����ͭ��ԭ��ص��������������Һ�е�������H��������ͭ�缫�ƶ�������a��Ǩ�ƣ�����B��Zn��Fe��ϡ������ɵ�ԭ��أ�п�ϻ��ã���ԭ��صĸ������缫��ӦΪ��Zn - 2e- ="=" Zn2+������ԭ��ص��������缫��ӦʽΪ��2H+ + 2e- ="=" H2�����缫�Ϸų���ɫ���壬����C������þ������������Һ��ɵ�ԭ��أ���ط�ӦΪ��2Al+2NaOH+2H2O====2NaAlO2+3H2������ ����������Ӧ����ԭ��صĸ�����þ�缫��ԭ��ص���������aΪ������bΪ��������ȷ��D��ͭ��ʯī���Ȼ�����Һ��ɵ�ԭ��أ���ط�ӦΪ��2FeCl3+Cu====2FeCl2+CuCl2��ͭ�缫����������Ӧ����ԭ��صĸ������缫��ӦΪ��Cu - 2e- ="=" Cu2+���缫������С��ʯī��ԭ��ص��������缫��ӦʽΪ��2Fe3+ + 2e- ="=" 2Fe2+���缫�������䣬����
�����Ѷȣ�һ��
3��ѡ���� ����װ�����ܹ���ԭ��ص��ǣ�������
A��
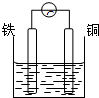
ϡ����
B��

ϡ����
C��
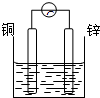
ϡ����
D��
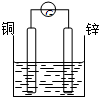
�Ҵ�
�ο��𰸣�A�����缫���ϲ�ͬ�����ϻ��ã�����ϡ���ᷴӦ���γɱպϻ�·���������γ�ԭ��أ���A��ȷ��
B�����缫������ͬ�������γ�ԭ��أ���B����
C�����缫���ϲ�ͬ��п�ϻ��ã�����ϡ���ᷴӦ���γɱպϻ�·���������γ�ԭ��أ���C��ȷ��
D���Ҵ���Һ�����磬�����γ�ԭ��أ���D����
��ѡAC��
���������
�����Ѷȣ���
4��ѡ���� ͼ1���ڽ���п��������һ����ij��Һ��ʪ����ֽ��ͼ2��NaBH4/H2O2ȼ�ϵ�أ�������˵����ȷ����
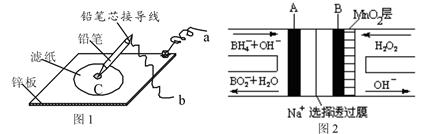
A��ͼ2��طŵ�����У�Na��������������Ǩ��
B��ͼ2��ظ������ĵ缫��ӦΪBH4���D 8e��+ 8OH����BO2��+ 6H2O
C�����������ƺͷ�̪�Ļ����Һ��ʪ��ֽ���õ��߽�a��bֱ����������Ǧ��оC�㴦���ֺ�ɫ
D������KI������Һ��ʪ��ֽ���õ��߽�a��b��A��B�缫������Ǧ��оC�㴦������ɫ����b�ӵ���A�缫
�ο��𰸣�BC
���������ͼ2����ԭ����У�����������������Ҫ�γ�����ɵıպϻ�·������Һ�е�������Ҫ�ɸ���������������A������ȼ�ϵ���У�ȼ�Ϸ�ӦʱҪʧ���ӣ���ȼ���ڸ�����A�缫����Ӧ��B��ȷ��
C����ʱͼ1����ԭ��أ�п����������Zn-2e-=Zn2+��Ǧ��о��������O2+2H2O+4e-=4OH-(����������ʴ)����̪�����죬��C��ȷ��
D������NaBH4/H2O2ȼ�ϵ������ӵ�Դ�����KI��Һ����Ǧ��оC�㴦������ɫ����C�㷢���ķ�Ӧ�ǣ�2I-2e-=I2��������������Ӧ�����ⵥ��ʹ���۱�������˵��bΪ���������ڵ����У����ص�����Ӧ����ӵ�Դ������������Ӧ��B�缫��D����
�����Ѷȣ�һ��
5��ѡ���� ԭ����ڷŵ�ʱ������ת����ʽ�ǣ�������
A���ѹ���ת����˻�ѧ��
B���ѻ�ѧ��ת��ɹ���
C��������ת����˵���
D���ѻ�ѧ��ת����˵���
�ο��𰸣�ԭ��طŵ�ʱ��������ʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ�����Ե��ӴӸ����ص��������������ڵ�·�У��������������ƶ������������ƶ������Թ����˱պϻ�·���γ��˵�������ԭ����ڷŵ�ʱ�ǰѻ�ѧ��ת����˵��ܣ�
��ѡD��
���������
�����Ѷȣ�һ��