微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
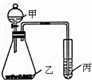
1、简答题 利用右图装置采用适当试剂可完成实验某探究实验,并得出相应实验结论,实验所用试剂或所得结论列于表中.请回答:
| 实验试剂 | 实验结论
甲
乙
丙
①
高锰酸钾
②
氧化性:KMnO4>Cl2>Br2
|
(1)图中①为______,②为______,
(2)请你根据上述实验装置设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表:
| 试剂甲 | 试剂乙 | 试剂丙 | 丙中现象 | 实验结论
______
______
______
______
______
|
2、实验题 铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

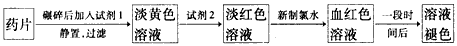
(1)试剂l是______________,试剂2是_______________,加入新制氯水后溶液中发生的离子反应方程式是_____________________________。
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为__________________________;写出+2价Fe在空气中转化为+3价Fe的离子方程式___________________________。
(3)该同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?________________________________。若你认为合理,请说明理由(若你认为不合理,该空不要作答)________________________; 若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不要作答): _______________________。
3、实验题 某化学研究性学习小组探究Fe3+和SO32-之间发生的反应。
(1)取5 mL浓FeCl3溶液于试管中,逐滴加入浓Na2SO3溶液,观察到溶液颜色由黄色变为红棕色,继续加入浓Na2SO3溶液至过量,溶液颜色加深,最终变为红褐色液体。无气泡产生,无沉淀生成。这种红褐色液体是___________________。
(2)除了以上观察到的现象外,该小组成员提出了另一种可能:发生氧化还原反应。反应的离子方程式为
_____________________。研究性学习小组设计两种实验方案证明发生了氧化还原反应。请把实验方案补充完整:
方案一:检验溶液中含有Fe2+证明发生了氧化还原反应;
方案二:检验溶液中含有___________证明发生了氧化还原反应。
实验用品:0.1 mol/L BaCl2溶液、3 mol/L盐酸、0.1 mol/L KMnO4(H+)溶液、氯水、20% KSCN溶液、0.5 mol/L KI溶液,试管若干、胶头滴管若干
(3)预处理:将(1)中获得的混合物放在如下图装置中处理足够时间。
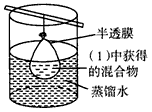
检验过程:

4、实验题 过氧化钙(CaO2)常用作种子消毒剂、药物制造、?油脂漂白及高温氧化剂,还可以作为鱼池增氧剂。将SO2通入过氧化钙固体粉末中有气体?生成。有人提出:CO2、SO2与过氧化?钙的反应原理相同;但也有人提出:SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断?。
实验一、通过气体体积的测量判断发生的化学反应,实验装置如下:?
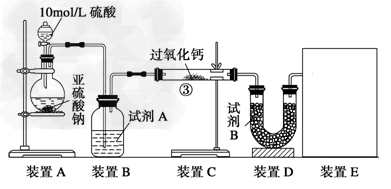
(1)试剂A可以选用____________,试剂B为碱石灰其作用是______________________。
(2)装置E用于测定氧气?的体积?,请在框中画出装置图。
(3)实验测得装?置C增重m1?g,装置D增重m2?g,装置E中收集到V?L气体(已换算成标准状况下),用上述有关测量数据判断,当SO2未氧化时,V与m1或m2的关系式为_________。若SO2完全氧化,写出反应的化学方程式:__________________________。
实验二、向一定量的过氧化钠固体中通入足量SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。提出假设:
假设1:反应后固体中只有Na2SO3,SO2未氧化;
假设2:反应后固体中只有Na2SO4,SO2完全氧化;
假设3?:________________________。
实验探究:
(4)设计实验证明假设3是正确的,简要回答实验过程、现象和结论:________________ ________________________________。
实?验评价:
(5)实验过程中SO2的通入量直接影响探究实验结果的科学性,请简要说明原因: _______________________________________。?
5、实验题 为证明化学反应有一定的限度,进行如下探究活动:
I.取5 mL 0.1 mol/L的KI溶液,滴加5~6滴稀FeCl3溶液;
Ⅱ.继续加入2 mL CCl4溶液,振荡;
Ⅲ.取萃取后的上层清液,滴加KSCN溶液。
(1)探究活动I的实验现象为_______________ 探究活动Ⅱ的实验现象为________________
(2)探究活动Ⅲ的目的是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色。对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+; 猜想二:生成的Fe(SCN)3溶液浓度极小,无法用肉眼观察其颜色。为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中的大;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN高。 结合新信息,现设计以下实验方案验证猜想:
①请完成下表:

②写出实验操作“方案一”中反应的离子方程式:_______________。
Ⅳ.为了测定探究活动I中的稀FeCl3溶液的浓度,现进行以下操作:
(3)移取25.00 mL稀FeCl3溶液至锥形瓶中,加入__________作指示剂,再用c mol/LKI标准溶液滴定,达到滴定终点时的现象是____________________。
(4)重复滴定三次,平均耗用c mol/L KI标准溶液V mL,则稀FeCl3溶液中溶质的物质的量浓度为_______
mol/L。