��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʵ��װ��ͼ��ȫ��ȷ����?

[? ]
A�������������ƹ���?
B������150mL0.10mol��L-1����
C���ⶨ�к���?
D�����뱽�ͼױ�
�ο��𰸣�C
���������
�����Ѷȣ���
2������� ��50mL 0.55mol/L NaOH��Һ��50mL 0.25mol/L H2SO4��Һ�����к��Ȳⶨ��ʵ�飬�����Һ�ڷ�Ӧǰ����¶ȱ仯Ϊt1�桫t2�� ��t2>t1��,��Ϻ���Һ�ı�����Ϊc = 4.18J����g���棩,��Һ���ܶȶ�����Ϊ1g/mL���к��ȡ�H=_________(�����ʽ�����û���) ����H2SO4��Һ������ͬ���ʵ���Ũ�ȵ�CH3COOH��Һ����õġ�H______��(��ƫ����ƫС������ͬ��������ϡ���ỻ��Ũ����������ʵ�飬��õġ�H________���ƫ����ƫС������ͬ����
�ο��𰸣�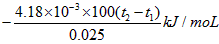 ?��ƫ�� ��ƫС
?��ƫ�� ��ƫС
���������
�����Ѷȣ�һ��
3������� ����ͼ��ʾװ�ý����к��Ȳⶨʵ�飬��ش����⣺
��1����С�ձ�֮����������ĭ���ϵ�������______����ʵ��װ���Ͽ���ͼ��ȱ�ٵ�һ�ֲ���������______��
��2��ʹ�ò�ȫ�������װ�ý���ʵ�飬ȡ50mL0.25mol/LH2SO4��Һ��50mL0.55mol/LNaOH��Һ��С�ձ��н����кͷ�Ӧ������ʵ���¶�ƽ������3.4�森��֪�кͺ����ɵ���Һ�ı�����Ϊ4.18J/��g-�棩����Һ���ܶȾ�Ϊ1g/cm3��ͨ������ɵ��к��ȡ�H=______��H2SO4��NaOH��Ӧ���Ȼ�ѧ����ʽΪ______��
��3��ʵ��������60mL0.25mol-L-1H2SO4��Һ��50mL0.55mol-L-1NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������______?�����ȡ���������ȡ����������к���______?�����ȡ���������ȡ�����������50mL0.50mol-L-1�������H2SO4��Һ��������ʵ�飬��÷�Ӧǰ���¶ȵı仯ֵ��______?���ƫ����ƫС����������Ӱ�족����
�ο��𰸣���1���к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�������С�ձ�֮����������ĭ���ϵ������ǣ����¡����ȡ�����ʵ������е�����ɢʧ���������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β������������ʴ�Ϊ�����¡����ȡ�����ʵ������е�����ɢʧ�����β�����������
��2��Q=��H=-��Tcm=-3.4��C��4.18J/��g?�棩��100g�T1421.2J=1.42KJ/mol����H=-Q/n��H2O��=-56.8KJ/mol���Ȼ�ѧ����ʽΪ��12H2SO4��aq��+NaOH��aq��=Na2SO4��aq��+H2O��l������H=-56.8KJ/mol���ʴ�Ϊ��12H2SO4��aq��+NaOH��aq��=Na2SO4��aq��+H2O��l������H=-56.8KJ/mol��
��3����Ӧ�ų����������������Լ�������Ķ����йأ�������60mL0.25mol?L-1H2SO4��Һ��50mL0.55mol?L-1NaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ��к�����ȣ��ִ��������ᣬ����������ȣ�������50mL0.50mol?L-1�������H2SO4��Һ��������ʵ�飬��÷�Ӧǰ���¶ȵı仯ֵ���С��
�ʴ�Ϊ������ȣ���ȣ�ƫС��
���������
�����Ѷȣ�һ��
4������� 50mL?1.0mol?L-1�����50mL?1.1mol?L-1����������Һ��ͼ1װ���н����кͷ�Ӧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȣ��Իش��������⣺
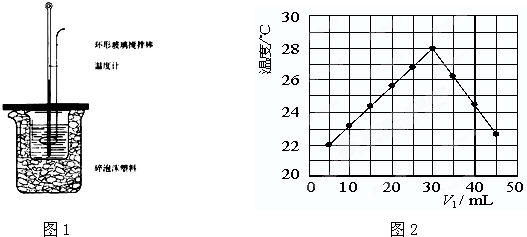
��1����С�ձ�����������ĭ���ϵ�����______��
��2��______����ܡ����ܡ��������β����������Ϊ����ͭ������ԭ����______��
��3�����ձ����粻��Ӳֽ�壬������к�����ֵ��Ӱ����______���ƫ�ߡ���ƫ�͡�����Ӱ�족����
��4���������60mL?1.0mol?L-1�����50mL?1.1mol?L-1����������Һ���з�Ӧ����������ʵ����ȣ���������______�������ӡ��������١����䡱���������к�����ֵ______�������ӡ��������١����䡱��
��5��ij�о�С�齫װ�����ƺ�V1?mL?1.0mol/L?HCl��Һ��V2?mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ������ͼ2��ʾ��ʵ����ʼ�ձ���V1+V2=50mL�����ش��������⣺�о�С������ʵ��ʱ�����¶�______������ڡ��������ڡ����ڡ���22�森
�ο��𰸣���1���������ȼƵĹ����ʵ��ijɰܹؼ����жϸ�װ�õĴ�С�ձ�����������ĭ���ϵ������DZ��¡����ȣ���ֹ����ɢʧ���ʴ�Ϊ�����¡����ȣ���ֹ����ɢʧ��
��2���к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹���������ͭ�ĵ���Ч�����ڻ��β�����������ʴ�Ϊ�����ܣ��������ȣ���������ɢʧ��
��3�����ձ����粻��Ӳֽ�壬����һ��������ɢʧ����õ��к�����ֵ�����С���ʴ�Ϊ��ƫ�ͣ�
��4����Ӧ�ų����������������Լ�������Ķ����йأ�������60mL0.25mol?L-1H2SO4��Һ��50mL0.55mol?L-1NaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ������������أ�������50mL0.50mol?L-1�������H2SO4��Һ��������ʵ�飬����к�����ֵ��ȣ��ʴ�Ϊ�����ӣ����䣻
��5������ʵ����ͼ2��ʾ���ݣ�����֪����ʵ�鿪ʼʱ�¶�һ���ǵ���22�棬�ʴ�Ϊ�����ڣ�
���������
�����Ѷȣ�һ��
5��ʵ���� 50ml?0.5mol��L��1��������50ml?0.55mol��L��1��NaOH?��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ���ش���������
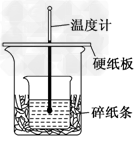
��1����ʵ��װ���Ͽ�����ͼ��֪��װ���в���֮����Ӧ��θ�����______________��
��2���ձ���������ֽ����������_____________��
��3���������Ӳֽ�壬��õ��к�����ֵ________���ƫ��ƫС������Ӱ�족����
��4��ʵ���и���?60?mL?0.50?mol��L��1�������?50mL?0.55?mol��L��1��?NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������______�����ȡ�����ȡ����������к���_______�����ȡ�����ȡ�����
��5������ͬŨ�Ⱥ���ͬ����İ�ˮ����NaOH��Һ��������ʵ�飬����к��ȵ���ֵ��________���ƫ��ƫС������Ӱ�족������������_____________________��
�ο��𰸣���1�����ӻ��β�����������ڴ�С�ձ�����������ĭ����ֽ������ʹС�ձ�������ձ�����ƽ
��2������ʵ������е�������ʧ
��3��ƫС?
��4�����ȣ����
��5��ƫС����Ϊ������ʵĵ�����Ҫ����
���������
�����Ѷȣ�һ��