|
|
|
高考化学必考知识点《盐类水解的原理》考点强化练习(2017年押题版)(五)
2017-03-05 13:38:09
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于电解质溶液的叙述正确的是
A.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ)
B.在0.1mol・L-1的NaHA溶液pH=4,则H2A为强酸
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊呈红色
D.向0.1mol・L-1的氨水中加少量硫酸铵固体,则溶液中c(OH-)/c(NH3・H2O)增大
|
2、选择题 下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-)
C.pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中:c(NH4+)大小顺序:①>②>③
D.含等物质的量的NaHC2O4和Na2C2O4的溶液: 3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
|
3、实验题 (1)(2分)甲同学在用FeSO4固体配制FeSO4溶液时,除了加入蒸馏水外,还需加 和 试剂(填化学式)
(2)(2分)乙同学为标定某醋酸溶液的准确浓度,用0.2000 mol・L―1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号
| 1
| 2
| 3
| 4
|
消耗NaOH溶液的体积(mL)
| 20.05
| 20.00
| 18.80
| 19.95
|
则该醋酸溶液的准确浓度为
。(保留小数点后四位)
(3)丙同学利用:5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O反应,用KMnO4溶液滴定某样品进行铁元素含量的测定。
①(2分)设计的下列滴定方式,最合理的是_____。(夹持部分略去)(填字母序号)
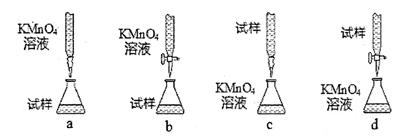
②(2分)判断滴定终点的依据是
。
4、选择题 Al3+ + 3H2O Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
A.加热
B.加适量NaOH溶液
C.通入氯化氢气体
D.加入固体三氯化铝
5、填空题 按要求填空。
Ⅰ:已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____________
Ⅱ:
【小题1】硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因____________如何才能用热水配制出澄清的较浓的CuSO4溶液____________________;
【小题2】稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的反应___________________________
III:依据氧化还原反应:MnO4-+5Fe2++8H+ = Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
①称量绿矾样品15.2g,配成100 mL待测溶液②取10.0ml待测液置于锥形瓶中,并加入一定量的硫酸③将0.1 mol?L-1的KMnO4溶液装入滴定管中,调节液面至8.00mL处④滴定待测液至滴定终点时,滴定管的液面读数18.00 mL
【小题3】如何知道滴定到达终点?
【小题4】下列操作会导致测定结果偏低的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
【小题5】下列每种量器的数量不限,在上述实验中,必须使用的有
A.托盘天平
B.量筒
C.碱式滴定管
D.酸式滴定管
E. 容量瓶
【小题6】FeSO4的质量分数为

 Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是