��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij���͵�أ���NaBH4(B�Ļ��ϼ�Ϊ��3)��H2O2��ԭ�ϣ��õ�ؿ�������ˮ��̽������������Դ���乤��ԭ����ͼ��ʾ������˵����ȷ����? (����)
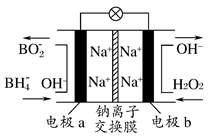
A����ع���ʱNa����b��������a����
B��ÿ����3 mol H2O2��ת��3 mol e��
C��b���ϵĵ缫��ӦʽΪ��H2O2��2e����2H��=2H2O
D��a���ϵĵ缫��ӦʽΪ��BH4����8OH����8e��=BO2����6H2O
�ο��𰸣�D
����������õ�ع���ʱ��a���缫��ӦʽΪBH4����8OH����8e��=BO2����6H2O��b���缫��ӦʽΪ4H2O2��8e��=8OH�������Ų��Ϸŵ磬a������ɼ��٣�b����������࣬��Na����a��������b������ÿ����3 mol H2O2ת��6 mol e������A��B��C����D��ȷ��
�����Ѷȣ�һ��
2��ѡ���� Al��Ag2O�����һ�ֿ�����ˮ�¶�����������Դ����ԭ����ͼ��ʾ���õ�ع���ʱ�ܷ�ӦʽΪ2Al��3Ag2O��2NaOH=2NaAlO2��6Ag��H2O��������˵���������? (����)��

A������ʱ����������ԭ��Ӧ
B�����缫������1.08 g Agʱ����·��ת�Ƶĵ���Ϊ0.01 mol
C��Al�缫�ķ�ӦʽΪAl��3e����4OH��=AlO2����2H2O
D������ʱ���Һ�е�Na������Ĥ����Al�缫
�ο��𰸣�D
�������������������ԭ��Ӧ��A�ԣ�1.08 g�������ʵ���Ϊ0.01 mol��B�ԣ����ܷ�Ӧʽ��֪��Al�缫�Ǹ������缫��ӦʽΪAl��3e����4OH��=AlO2����2H2O��C�ԣ�������Ӧ����������D����
�����Ѷȣ�һ��
3������� 3�֣�����Ƭ��þƬ�õ������Ӻ����NaOH��Һ���ձ������ԭ��أ���ԭ��صĸ���Ϊ___________��缫��ӦʽΪ? __________________________________________��
�ο��𰸣�(3��)Al? Al �C 3e-? + 4OH- = AlO2- + 2H2O
�����������
�����Ѷȣ���
4��ѡ���� ��пƬ��ͭƬ�õ������Ӻ��������ͭ��Һ�У�����ԭ��ط�Ӧ����Ӧǰ����Һ������䣩���ڷ�Ӧ�����У���������������ǣ�������
A��������пƬ����������ͭƬ
B��ͭƬ��������пƬ������
C����Һ��SO42-�����ʵ���Ũ�ȱ��ֲ���
D����Һ��Cu2+����
�ο��𰸣�A��ͭ��п��ϡ������ɵ�ԭ����У��ϻ��ý���п���������ϲ����õĽ���ͭ�����������ӴӸ����ص���������������A��ȷ��
B��ͭ��п��ϡ������ɵ�ԭ����У��ϻ��ý���п���������ϲ����õĽ���ͭ����������B��ȷ��
C��п��ϡ���ᷴӦ��������п��������ʵ�������������δ�μӷ�Ӧ��������Һ��SO42-�����ʵ���Ũ�ȱ��ֲ��䣬��C��ȷ��
D��ԭ��طŵ�ʱ�����ӴӸ����ص�������������������Һ���������������ƶ������������ƶ�����D����
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� ��һ��ȼ�ϵ�أ�����ȼ��ΪH2�Ϳ����������Ϊ���ڵ�K2CO3����ص��ܷ�ӦʽΪ2H2��O2===2H2O��������ӦΪH2��CO ��2e��===H2O��CO2���õ�طŵ�ʱ������˵������ȷ����(����)
��2e��===H2O��CO2���õ�طŵ�ʱ������˵������ȷ����(����)
A��������ӦΪ2H2O��O2��4e��===4OH��
B��CO ���ƶ�
���ƶ�
C�����������������·����
D�������CO �����ʵ���������
�����ʵ���������
�ο��𰸣�B
�������������Ϊ��ԭ��Ӧ��A�������������ƶ���B��ȷ�������ɸ������������룬C�����ܷ�Ӧû������CO32-������CO32-�����ʵ������䣬D����ѡB��
��������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ���ݴ˿��Խ����йص��жϡ�
�����Ѷȣ�һ��