微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5为77.1℃;C2H5OH为78.3℃;C2H5OC2H5(乙醚)为34.5℃;CH3COOH为118℃。实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸,边加热蒸馏。由上面的实验可得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)反应中加入的乙醇是过量的,其目的是?。
(2)边滴加醋酸,边加热蒸馏的目的是?。
将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向产品中加入?(填字母)。
A.无水乙醇? B.碳酸钠粉末? C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡,分离,其目的是?。
(5)然后再向其中加入无水硫酸铜,振荡,其目的是?。最后,将经过上述处理后的液体加入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集沸点在76℃~78℃之间的馏分即得纯净的乙酸乙酯。
参考答案:(1)增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进行
(2)增加醋酸浓度,减小生成物乙酸乙酯的浓度,有利于酯化反应向生成乙酸乙酯的方向进行
(3)B
(4)除去粗产品中的乙醇
(5)除去粗产品中的水
本题解析:(1)制取乙酸乙酯的反应是可逆反应,增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进行;
(2)乙酸乙酯、乙醇、乙醚的沸点较低,边加醋酸边蒸馏,目的使产品蒸出,减小乙酸乙酯的浓度,同时增大醋酸的浓度,使平衡正向进行;
(3)乙酸乙酯不溶于水,醋酸与碳酸钠反应生成醋酸钠、水、二氧化碳气体,所以溶于水的物质在下层,不溶于水的乙酸乙酯在上层,分液可使混合物分离,因此除去产品中的醋酸,应选择碳酸钠溶液,答案选B;
(4)粗产品中仍含有乙醇、乙醚、水,其中乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH,所以加入饱和的氯化钙溶液,目的是除去粗产品中的乙醇;
(5)无水硫酸铜与水结合生成蓝色的CuSO4・5H2O,所以加入无水硫酸铜,振荡,其目的是除去粗产品中的水,然后蒸馏可得乙酸乙酯。
本题难度:一般
2、计算题 在一定温度下,溶质溶解在两种互不相溶的溶剂中的浓度之比是一个常数K,若c(A)、c(B) 分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于
分别表示溶质在A、B两种溶剂中的浓度,则有c(A)/c(B)=K。对于 而言,
而言, 。现有2.0L碘水,其中含
。现有2.0L碘水,其中含 ,若用
,若用 萃取,按两种方法萃取:第一种方法用50mL
萃取,按两种方法萃取:第一种方法用50mL 萃取一次;第二种方法是分两次萃取,每次用25mL
萃取一次;第二种方法是分两次萃取,每次用25mL 。求两种情况下碘水中残余的
。求两种情况下碘水中残余的 的质量,并指出哪种方法效果好。
的质量,并指出哪种方法效果好。
参考答案:0.0064g , 0.0046g ,分两次萃取好
本题解析:第一种方法:
设 ,则
,则

x・2L+85x・0.05L="0.02g?" ?
残余
第二种方法:
第一次萃取:设
a・2L+85a・0.025L=0.020g

残余
第二次萃取:设
则b・2L+85b・0.025L="0.0096g" 
残余
通过比较可知,分两次萃取比一次性萃取好。
本题难度:一般
3、选择题 图中a、b、c表示相应仪器中加入的试剂,可用下图装置制取、净化、收集的气体是

[? ]
气体
?a
?b
c
A.
?NH3
浓氨水
生石灰
?碱石灰
B.
?CO2
盐酸
?碳酸钙
饱和NaHCO3溶液
C.
?NO
稀HNO3?
铜屑
H2O
D.
?NO2
?浓HNO3
铜屑
?NaOH溶液
参考答案:B
本题解析:
本题难度:一般
4、实验题 (14分)某实验小组利用如下仪器组装一套制备氮化硼晶体的装置。
反应原理是B2O3 + 2NH3 ?2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)
?2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)

(1)各仪器接口由左到右的连接顺序为?。
(2)实验过程分为如下操作:①提纯BN ②滴加浓氨水③添加药品④连接装置
⑤加热管式电炉⑥检查装置气密性⑦取出反应混合物⑧停止加热,继续通一段时间的氨气。则正确的操作顺序为_______________________?(填序号)。
(3)装置D的作用是?。
(4)装置C能产生氨气的原因有?(答出其中一项即可)。
(5)管式电炉加热反应前必须进行的一步操作是?,反应结束时,继续通一段时间氨气的目的是?。
(6)除去产物中未反应的B2O3并得到纯净的BN固体的实验操作是__________。
参考答案:(14分)(1)eabcdfgh?(2)④⑥③②⑤⑧⑦①?(3)防止倒吸
(4)氨水中存在可逆反应NH3+H2O  ?NH3?H2O
?NH3?H2O  ?NH4+ + OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH3放出;或生石灰与水反应放出大量热,促进NH3?H2O分解,并使气体溶解度下降,有利于NH3放出。
?NH4+ + OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH3放出;或生石灰与水反应放出大量热,促进NH3?H2O分解,并使气体溶解度下降,有利于NH3放出。
(5)除去装置中的氧气;冷却反应混合物防止BN被氧化。
(6)将粗产品加入适量的热水,充分搅拌后趁热过滤,用热水洗涤滤渣2~3次,烘干
本题解析:(1)C装置是制取氨气的,由于氨气中含有水蒸气,所以首先要干燥氨气,剩余的氨气还需要进行尾气处理。由于氨气极易溶于水,所以还需要装置D来防止倒吸,所以正确的顺序是eabcdfgh。
(2)装置连接好以后,首先要检验装置的气密性。由于BN高温下能被空气氧化,不溶于水,所以反应结束后,还需要继续通一段时间的氨气,所以正确的顺序是④⑥③②⑤⑧⑦①。
(3)由于氨气极易溶于水,所以还需要装置D来防止倒吸。
(4)由于氨水中存在可逆反应NH3+H2O  ?NH3?H2O
?NH3?H2O  ?NH4+ + OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH3放出;或生石灰与水反应放出大量热,促进NH3?H2O分解,并使气体溶解度下降,有利于NH3放出。
?NH4+ + OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH3放出;或生石灰与水反应放出大量热,促进NH3?H2O分解,并使气体溶解度下降,有利于NH3放出。
(5)由于BN高温下能被空气氧化,所以管式电炉加热反应前必须进行的一步操作是除去装置中的氧气;同样分析可知,反应结束时,继续通一段时间氨气的目的是冷却反应混合物防止BN被氧化。
(6)由于B2O3难溶于冷水但可溶于热水,所以除去产物中未反应的B2O3并得到纯净的BN固体的实验操作是将粗产品加入适量的热水,充分搅拌后趁热过滤,用热水洗涤滤渣2~3次,烘干即可。
本题难度:一般
5、选择题 右图是一套实验室制备气体的装置,用于发生、干燥、收集和吸收有毒气体。下列各组物质能利用这套装置进行实验的是
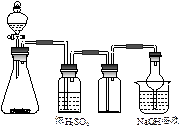
A.电石和水
B.MnO2和浓盐酸
C.Cu片和浓硝酸
D.Na2SO3和浓硫酸
参考答案:CD
本题解析:略
本题难度:一般