微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 主族元素在元素周期表中的位置,取决于元素原子的( )
A.相对原子质量和核电荷数
B.电子层数和中子数
C.电子层数和最外层电子数
D.金属性和非金属性的强弱
参考答案:对主族元素而言,其电子层数就是该元素在元素周期表中的周期序数;其最外层上的电子数就是该元素在周期表中的族序数.由该元素在周期表中的周期和族决定元素的位置.
故选:C.
本题解析:
本题难度:一般
2、选择题 下列各组元素属于p区的是
[? ]
A.原子序数为1、2、7的元素
B.O、S、P
C.Fe、Ar、Cl
D.Na、Li、Mg
参考答案:B
本题解析:
本题难度:简单
3、推断题 X、Y、Z、W是?短周期的四种元素,有关它们的信息如下表所示。

填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X单质分子的结构式是_________?,Z元素原子最外层共有_________种不同运动状态的电子。
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是__________。
(3)常温时,W的硫酸盐溶液的pH________7(填“=”、“>”或“<”),理由是:_____________(用离子方程式表示)。
(4)25℃、101?kPa时,32?g?Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6?kJ的热量,写出该反应的热化学方程式__________________。
参考答案:(1) ;7?
;7?
(2)HClO4>HNO3>H2CO3?
(3)<7?;Al3+ + 3H2O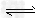 Al(OH)3+3H+?
Al(OH)3+3H+?
(4)CH4(g)+ 2O2(g)?→?CO2(g) + 2H2O(l) + 890.3 KJ
本题解析:
本题难度:一般
4、选择题 科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现Al的超原子结构Al13和Al14.Al13、Al14的性质很象现行周期表中的某主族元素,已知这类超原子当具有40个价电子时最稳定.下列说法正确的是( )
A.All4与ⅡA族元素性质相似
B.Al13、Al14互为同位素
C.Al13和Al14都具有强还原性,容易失去电子生成阳离子
D.Al13超原子中Al原子间是通过离子键结合的
参考答案:A.All4的价电子为3×14=42,当具有40个价电子时最稳定,则易失去2个电子,则与ⅡA族元素性质相似,故A正确;
B.同位素的分析对象为质子数相同而中子数不同的原子,而超原子的质子、中子均相同,故B错误;
C.Al13的价电子为3×13=39,易得电子,形成阴离子,而All4的价电子为3×14=42,易失去电子,形成阳离子,故C错误;
D.Al13超原子中Al原子间是通过共有电子对成键,所以以共价键结合,故D错误;
故选A.
本题解析:
本题难度:一般
5、选择题 某元素的气态氢化物的化学式为H2R,则此元素最高价氧化物对应水化物的化学式可能为
A.H2RO3
B.H2RO4
C.HRO3
D.H3RO4
参考答案:B
本题解析:由H2R知,R的最低负化合价为-2,则R的最高正化合价为+6,即为ⅥA族元素,其最高价氧化物对应水化物的化学式则为H2RO4.
本题难度:简单