| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ��������ԭ���ԭ��������ǿ����ϰ��2017��Ѻ��棩(��)
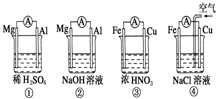 �ο��𰸣�B ��������� �����Ѷȣ��� 3��ѡ���� ������������Դ����Ǧ���أ���ط�Ӧ���£� |
�ο��𰸣�
���������
�����Ѷȣ�һ��
4��ѡ���� (2014���㽭ʡ������ѧ������ѧ����ĩ���ۻ�ѧ�Ծ���
������ijУʵ��С����Ƶ�һ��ԭ���װ�ã������й���������ȷ����
A����װ���ܽ���ѧ��ת��Ϊ����
B��ʯī�缫�ķ�Ӧʽ��O2+2H2O+4e��=4OH��
C��������Cu�缫����������ʯī�缫
D������ܵķ�Ӧ�ǣ�2Cu+O2+4HCl=2CuCl2+2H2O
�ο��𰸣�B
���������
A��ԭ����ܽ���ѧ��ת��Ϊ���ܣ�A��ȷ��B��ԭ����и���ʧȥ���ӷ���������Ӧ�������õ����ӷ�����ԭ��Ӧ����ͭ�Ǹ���������������ͨ�룬���ڵ���������ᣬ���ʯī�缫�ķ�Ӧʽ��O2+4H++4e����2H2O��B����ȷ��C��ͭ�缫�Ǹ�����ʯī���������������Cu�缫����������ʯī�缫��C��ȷ��D������ܵķ�Ӧ�ǣ�2Cu+O2+4HCl=2CuCl2+2H2O��D��ȷ����ѡB��
�����Ѷȣ�һ��
5��ѡ���� �й���ͼװ�õ���������ȷ���ǣ�������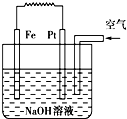
A�����ǵ��NaOH��Һ��װ��
B����װ����PtΪ�������缫��ӦΪO2+2H2O+4e-��4OH-
C����װ����FeΪ�������缫��ӦΪFe-2e-+2OH-��Fe��OH��2
D������һ��ԭ���װ��
�ο��𰸣�A��û����ӵ�Դ��Ϊԭ��أ���A����
B��FeΪ������PtΪ����������������ʴ����������ӦΪO2+2H2O+4e-��4OH-����B��ȷ��
C������Feʧȥ���ӣ�����ӦΪFe-2e-+2OH-��Fe��OH��2����C��ȷ��
D���ɵ缫��������γɱպϻ�·������ԭ��أ���D��ȷ��
��ѡA��
���������
�����Ѷȣ���
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ���߿���ѧ���⡶����ʽ���ṹʽ��.. | ||
| �����Ŀ |