微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有关下列两种溶液的说法中,正确的是( )
溶液①:0.2mo1?L-1?CH3COONa溶液;
溶液②:0.1mo1?L-1H2SO4溶液.
A.相同温度下,溶液中水的电离程度:溶液①<溶液②
B.加水稀释溶液①,溶液中
c(CH3COOH)?c(OH-)
c(CH3COO-)
|
变大
C.等体积混合溶液①和溶液②,所得溶液中c(CH3COO-)+2c(SO42-)=c(Na+)
D.25℃时,向溶液②中滴加溶液①至pH=7,溶液中c(Na+)>c(SO42-)
参考答案:A、溶液①是强碱弱酸盐溶液,醋酸根离子水解显碱性,促进水的电离:溶液②是酸溶液,对水的电离起到抑制作用;相同温度下,溶液中水的电离程度:溶液①>溶液②,故A错误;
B、加水稀释促进醋酸根离子的水解,但不改变水解平衡常数;溶液中c(CH3COOH)?c(OH-)c(CH3COO-)不变,故B错误;
C、溶液①和溶液②等体积混合恰好反应生成醋酸和硫酸钠,溶液呈酸性,溶液中存在电荷守恒分析判断;[Na+]+[H+]=[OH-]+[CH3COO-]+2[SO42-],若c[CH3COO-]+2[SO42-]=[Na+]得到[H+]=[OH-],不符合溶液呈酸性;故C错误;
D、25℃时,溶液混合后PH=7,溶液呈中性,溶液中存在电荷守恒;[Na+]+[H+]=[OH-]+[CH3COO-]+2[SO42-],[H+]=[OH-],c[CH3COO-]+2[SO42-]=[Na+],溶液中c(Na+)>c(SO42-),故D正确;
故选D.
本题解析:
本题难度:一般
2、填空题 (14分)某工业原料主要成分是NH4Cl、FeCl3和AlCl3。利用此原料可以得到多种工业产品。分析下面流程,回答问题。
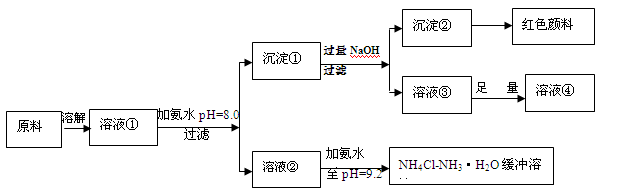
已知:Ksp[Fe(OH)3]=4.0×10-38
(1)用稀硫酸中和等体积等pH值的氨水和烧碱溶液,前者需要消耗的酸液体积 (填“大”“小”或“相同”)
(2)计算溶液②中Fe3+的物质的量浓度为 mol/L
(3)缓冲溶液中存在的平衡体系有: 、 、
此时溶液中c(NH4+) c(Cl-)(填>、=、<)。
(4)在缓冲溶液中加入少量盐酸或者NaOH溶液,溶液的pH值几乎依然为9.2。简述原理:
请举出另一种缓冲溶液的例子(写化学式) 。
(5)常温下向较浓的溶液④中不断通入HCl气体,可析出大量AlCl3・6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
参考答案:(1)大 (2分)
(2)4.0×10-20 (2分)
(3)NH4++H2O NH3・H2O+H+(Ⅰ) NH3・H2O
NH3・H2O+H+(Ⅰ) NH3・H2O NH4++OH-(Ⅱ) H2O
NH4++OH-(Ⅱ) H2O H++OH-(Ⅲ) >
H++OH-(Ⅲ) >
(4分,每空1分)
(4)当加入少量酸时,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。(2分)
CH3COONa-CH3COOH(或其它合理答案) (1分)
(5)AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s) Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。(3分)
Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。(3分)
(从抑制铝离子水解角度答题不得分)
本题解析:(1)pH相同的氨水和烧碱,氨水的物质的量浓度大,所以需要的酸的体积大。(2) 溶液的pH=8,氢离子浓度=10-8mol/L,氢氧根离子浓度=10-6mol/L,根据Ksp[Fe(OH)3]=4.0×10-38计算铁离子浓度=4.0×10-20。
(3)缓冲溶液中有铵根离子,所以存在铵根离子的水解平衡,NH4++H2O NH3・H2O+H+,溶液中有一水合氨,NH3・H2O
NH3・H2O+H+,溶液中有一水合氨,NH3・H2O NH4++OH-,存在一水合氨的电离平衡,溶液中肯定存在水的电离平衡, H2O
NH4++OH-,存在一水合氨的电离平衡,溶液中肯定存在水的电离平衡, H2O H++OH-。由于溶液中的pH=9.2,所以溶液显碱性,说明氢离子浓度小于氢氧根离子浓度,根据电荷守恒,所以铵根离子浓度大于氯离子浓度。(4)缓冲溶液中加入少量盐酸,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。类似的缓冲溶液由CH3COONa-CH3COOH。 (5) 沉淀①为氢氧化铝和氢氧化铁,加入过量氢氧化钠后溶液③为偏铝酸钠,沉淀②为氢氧化铁沉淀,溶液③中加入足量的盐酸,得到的溶液④为氯化铝溶液,在AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s)
H++OH-。由于溶液中的pH=9.2,所以溶液显碱性,说明氢离子浓度小于氢氧根离子浓度,根据电荷守恒,所以铵根离子浓度大于氯离子浓度。(4)缓冲溶液中加入少量盐酸,平衡体系(Ⅱ)产生的OH-与酸反应,消耗了加入的H+,当加入少量碱时,平衡体系(Ⅰ)的NH4+与碱反应,消耗了加入的OH-,从而可在一定范围内维持溶液pH大致不变。类似的缓冲溶液由CH3COONa-CH3COOH。 (5) 沉淀①为氢氧化铝和氢氧化铁,加入过量氢氧化钠后溶液③为偏铝酸钠,沉淀②为氢氧化铁沉淀,溶液③中加入足量的盐酸,得到的溶液④为氯化铝溶液,在AlCl3饱和溶液中存在溶解平衡:AlCl3・6H2O(s) Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。
Al3+(aq) +3Cl―(aq) +6H2O(l),通入HCl气体使溶液中c(Cl―)增大,平衡向析出固体的方向移动从而析出AlCl3晶体。
考点:盐类的水解。
本题难度:困难
3、选择题 25℃,水的电离达到平衡:H2O 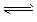 H++OH- ,下列叙述正确的是?
H++OH- ,下列叙述正确的是?
[? ]
A.向水中加入稀醋酸,平衡逆向移动,c(H+)降低
B.向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
参考答案:C
本题解析:
本题难度:一般
4、填空题 (12分) (1)某温度下,Kw=10-12。
①若保持温度不变,某溶液中c(H+)为1×10-7mol・L-1,则该溶液显 性(填“酸”、“碱”或“中”)。
②若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH-)=1010,则此时水电离的c(H+)= mol・L-1。
(2)常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
①混合溶液的pH=8的原因(用离子方程式表示): 。
②混合溶液中离子浓度由大到小的顺序是: 。
③混合溶液中由水电离出的c(H+) 同浓度NaOH溶液中由水电离出的c(H+)
(填“>”、“<”或“=”)。
④求出混合溶液中下列算式的精确计算结果(填具体数据):
c(Na+)-c(A-)= mol/L。
参考答案:(1)①碱(2分) ②10-11(2分)
(2)①A-+H2O HA+OH-(2分) ②c(Na+) >c(A-) > c(OH-)>c(H+)(2分)
HA+OH-(2分) ②c(Na+) >c(A-) > c(OH-)>c(H+)(2分)
③>(2分) ④9.9×10-7 (2分)
本题解析:(1)①溶液中c(OH-)为Kw /c(H+)= 1×10-5mol・L-1,c(OH-)> c(H+),故显碱性;②溶液显酸性,水电离出的c(OH-)= c(H+),
c(H+)=Kw /c(OH-),代人c(H+)/c(OH-)=1010,可得c(OH-)= 10-11,则水电离的c(H+)=10-11;
(2)①反应生成了强碱弱酸盐,会发生水解,即A-+H2O HA+OH-;
HA+OH-;
②该溶液相当于0.05mol/L的NaA溶液,所以c(Na+) >c(A-) > c(OH-)>c(H+);
③混合溶液中水的电离受到促进,同浓度NaOH溶液中水的电离受到抑制,故答案为>;
④混合溶液的pH=8,c(H+)=10-8 mol・L-1, c(OH-)= Kw/ c(H+)=10-6 mol・L-1,根据电荷守恒c(Na+) +c(H+)=c(A-) + c(OH-),所以c(Na+)-c(A-)= c(OH-)-c(H+)=9.9×10-7 mol/L。
考点:水的电离和溶液的酸碱性
点评:本题考查水的电离和溶液的酸碱性,题目难度不大,需要熟悉水的离子积只与温度变化有关。
本题难度:一般
5、实验题 (11分)(1)下图分别是温度计、量筒、滴定管的一部分,
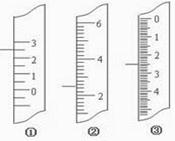
则:量筒应该是 读数为 mL,滴定管应该是 读数为 mL,温度计应该是 。
(2)实验室有一瓶混有氯化钠的氢氧化钠固体试剂,为了验证其纯度,用已知浓度的盐酸进行滴定,试回答下列问题:
①称取一定质量固体试剂配制100mL溶液。
②将标准盐酸装在25.00mL 滴定管中,调节液面位置在 ,并记下刻度。
③取20.00mL待测液,待测定。该项实验操作的主要仪器有 。
用 试剂作指示剂。
④下列实验操作会引起氢氧化钠含量偏高的是 。
A.滴定前滴定管尖嘴有气泡,滴定后滴定管尖嘴无气泡
B.中和滴定时,锥形瓶内有少量蒸馏水
C.酸式滴定管用蒸馏水洗后,用标准液润洗2-3次
D.读取滴定管终点读数时,仰视刻度线