微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氧化还原反应在工农业生产和日常生活中有广泛运用
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:
C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是______________。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有____________。(填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而 Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是_________。(填“氧化作用”或“还原作用”)
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_____________。
(5)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式____________________。
参考答案:(1)C6H12O6
(2)还原性
(3)还原作用
(4)保护FeSO4不被空气中的氧气氧化
(5)2Fe3++Cu==2Fe2++Cu2+
本题解析:
本题难度:一般
2、选择题 当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成深蓝色溶 液。向深蓝色溶液中通入SO2气体,又生成了白色沉淀。将白色沉淀加入稀硫酸中,又生成了红色粉末 状固体和SO2气体,同时溶液呈蓝色。根据上述实验现象分析推测,下列描述正确的是
[? ]
A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子
B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应
C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下发生了自身氧化还原反应
D.反应过程中消耗的SO2与生成的SO2的物质的量相等
参考答案:AC
本题解析:
本题难度:一般
3、填空题 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现请 就三大酸与金属铜反应的情况,填空回答下列问题:
(1)我们知道,稀盐酸不与Cu反应,但在稀盐酸中加入H2O2后,则可使铜顺利溶解,该反应的化学方程式为________。
(2)在一定体积的18 mol.L-1的浓硫酸中加入过量铜片,加热使之反应,被还原 的硫酸为0.9 mol。则浓硫酸的实际体积____(填写“大于”“等于”或 “小于”)100 mL,你认为其主要原因是________。若使剩余的铜 片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为____。
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出这可能是溶液中Cu2+与NO2共存的结果, 请你设计实验探究此说法正确与否(简述实验方案和实验现象及由此得出的结论)____。
参考答案:(l)Cu+H2O2+2HCl=CuCl2+2H2O
(2)大于 ;随着反应的进行,浓硫酸变成稀硫酸,铜和稀硫酸不反应 ;3Cu+8H++2NO3-=3Cu2+? +2NO↑+4H2O
(3)将一定量NO2通入到铜片稀硝酸反应后的溶液中,若溶液颜色变绿,则该同学的结论正确,反之, 不正确(其他合理答案也可)
本题解析:
本题难度:一般
4、选择题 下列叙述正确的是
[? ]
A.Na2O2、Cl2、NO2均能与水发生氧化还原反应
B.在加热的条件下稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
C.Cu、Fe、C分别在氧气中燃烧都只能生成一种氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
参考答案:A
本题解析:
本题难度:简单
5、选择题 取一定质量含Cu、Cu2O、和CuO的固体混合物,将其分成两等份并进行下列转化:
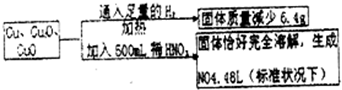
则转化过程中所加稀HNO3的物质的量浓度为( )
A.3.2mol/L
B.3.6mol/L
C.4.0mol/L
D.4.4mol/L
参考答案:A
本题解析:
本题难度:简单