微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 T°C时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
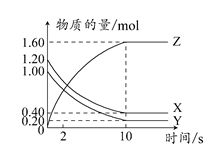
下列描述正确的是? ( )
A.平衡时,X、Y的转化率相同
B.达到平衡后,将容器体积压缩为1 L,平衡向正反应方向移动
C.T°C时,该反应的化学方程式为:X(g)+Y(g) 2Z(g),平衡常数K=40
2Z(g),平衡常数K=40
D.T°C时,若起始时X为0.71 mol,Y为1.00 mol,则平衡时Y的转化率约为60%
2、填空题 氨是氮循环中的重要物质,氨的合成是目前普遍使用的人工固氮方法.
(1)已知:H-H键能为436kJ?mol-1,N≡N键能为946kJ?mol-1,N-H键能为391kJ?mol-1.写出合成氨反应的热化学方程式:______
(2)恒温下,往一个4L的密闭容器中充人5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30
c(NH3)/mol?L-1
0.08
0.14
0.18
0.20
0.20
0.20
|
①5min内,消耗H2的平均反应速率为______
②N2的平衡转化率______
③此条件下该反应的化学平衡常数K=______.反应达到平衡后,若维持容器体积不变,温度不变,往平衡体系中加入H2、N2和NH3各8mol,化学平衡将向______方向移动(填“正反应”或“逆反应”);化学平衡常数值______(填变大、变小、不变);
④若温度维持不变,只将容器体积由4L变为2L,达新平衡时N2的平衡浓度______0.4mol?L-1(填大于、小于与等于)
3、填空题 373K时,某 1L密闭容器中加入1molPCl5发生如下可逆反应: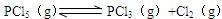 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。
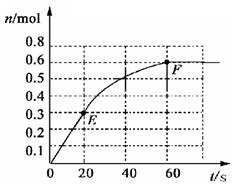
(1 )前 20
)前 20 s内 PCl5(g)的平均反应速率为?
s内 PCl5(g)的平均反应速率为?
(2)373K时该反应的平衡常数的值为?
(3)若在此平衡体系中再加入 1mol的 PCl5,与原平衡比较,新平衡时 PCl5的转化率?(填“增大”或“减小”,下同)。PCl5的平衡浓度?。
(4)将原平衡升温至 473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为 PCl5的3倍,该反应的正反应为(填“放热反应”或 “吸热反应”)?,为增大平衡体系中 Cl2的物质的量,下列措施正确的是(其它条件相同)?
a.升高温度? b.扩大容器的体积
c.加入合适的催化剂? d.再充入 PCl3
4、选择题 在密闭容器中进行如下可逆反应:X2(g)+Y2(g) = 2XY(g),已知X2、Y2、XY三者起始浓度分别为0.l mol/L、0.3 mol/L、0.2 mol/L,在一定条件下反应达到平衡,此时容器中不可能的情况是?
[? ]
A.X2为0.2 moI/L
B.Y2为0.35 mol/L
C.XY为0.3 mol/L
D.X2、Y2、XY总浓度为0.6 mol/L
5、选择题 对可逆反应4NH3(g) + 5O2(g) 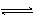 ?4NO(g) + 6H2O(g),下列叙述正确的是(?)
?4NO(g) + 6H2O(g),下列叙述正确的是(?)
A.达到化学平衡时,4v正(O2) = 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,与原平衡相比,则正反应速率增大,逆反应速率减小,平衡正向移动
D.反应温度不变时,若物质的平衡浓度改变,该反应的平衡常数也会发生改变