微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
①盐酸是一种既有氧化性,又有还原性的强酸;②向淀粉碘化钾溶液中通入一种气体时,如果溶液变蓝,则通入的气体一定是氯气;③漂白粉在空气中长期放置会变质,是由于被氧气氧化的缘故;④金属氧化物与盐酸的化学反应都是复分解反应;⑤在氧化还原反应中,还原剂得到的电子总数与氧化剂失去的电子总数一定相等。
A.全部
B.①
C.①②③④
D.①⑤
2、实验题 硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
I.对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是??。
第1组
| 第2组
| 第3组
|
S (单质)
| SO2、H2SO3、M、NaHSO3
| SO3、H2SO4、Na2SO4、 NaHSO4
|
?
Ⅱ.某校化学学习小组用下图所示的实验装置研究SO2气体还原Fe3+、Br2的反应。
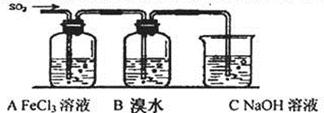
(1)下列实验方案可以用于在实验室制取所需SO2的是??。
A.Na2SO3溶液与HNO3?B.Na2SO3固体浓硫酸
C.固体硫在纯氧中燃烧?D.铜与热的浓硫酸
(2)装置C的作用是除去多余的SO2,防止污染空气。已知在用氢氧化钠溶液吸收SO2的 过程中,往往得到Na2SO3和NaHSO3的混合溶液,常温下,溶液pH随n(SO32―):n(HSO3―)变化关系如下表
n(SO32―):n(HSO3―)
| 91:9
| 1:1
| 9:91
|
pH
| 8.2
| 7.2
| 6.2
|
?
当吸收液中n(SO32―):n(HSO3―) =10:1时,溶液中离子浓度关系正确的是??。
A.c(Na+)+ c(H+)= 2c(SO32―)+ c(HSO3―)+ c(OH―)
B.c(Na+)>c(HSO3―)>c(SO32―)>c(OH―)>c(H+)
C.c(Na+)>c(SO32―)>c(HSO3―)>c(OH―)>c(H+)
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中反应后的溶液分成三份,并设计了如下探究实验,请你评价并参与他们的探究过程(限选试剂:KMnO4溶液、KSCN溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝 酸、Ba(NO3)2溶液、新制的氯水)
序号
| 实验方案
| 实验现象
| 结论
|
方案①
| 往第一份试液中加入KMnO4溶液溶液
| 紫红色褪去
| SO2与Fe3+反应生成了Fe2+
|
方案②
| 往第二份试液中加入
| ?
| SO2与Fe3+反应生成了Fe2+
|
方案③
| 往第二份试液中加入
| ?
| SO2与Fe3+反应生成了SO42―
|
?
上述方案①得出的结论是否合理?,原因??。
如果他们设计的方案②与方案③均合理并且得到相应结论,请你将上面表格补充完整。
(4)装置B中能表明Br―的还原性弱于SO2的现象是??。
3、选择题 下列说法正确的是(?)
A.置换反应一定属于氧化还原反应
B.分解反应均不属于氧化还原反应
C.复分解反应有的属于氧化还原反应
D.化合反应有的属于氧化还原反应
4、填空题 (10分)氧化还原反应在农业生产中和日常生活中有广泛的运用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6),提供能量以维持生命活动,反应的化学方程式为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是?。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有?(填“氧化性”或“还原性”)
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中,维生素C所起的作用是?填“氧化作用”和“还原作用”)
(4)全世界每年有近1/10的钢铁因生锈而损失,人们常用稀硫酸除去钢铁表面的铁锈(Fe2O3),请写出除铁锈的离子方程式:?,然而这并不能解决根本问题,实质上我们应该怎样防止铁生锈,生活中通常采用?方法(符合题意一种即可)防止铁生锈。
5、选择题 下列褪色过程不是因为氧化还原反应而褪色的是?(?)
A.SO2气体通入溴水使溴水褪色
B.氯水使滴有酚酞的NaOH溶液褪色,加入N aOH后不变红
aOH后不变红
C.将苯滴入溴水中振荡,溴水层褪色
D.将含有碘单质的淀粉溶液,加入NaOH溶液后蓝色褪去