微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.某一反应的活化分子百分数是个定值
B.升高温度会加快化学反应速率,其原因是增加了活化分子百分数
C.活化分子之间发生的碰撞一定为有效碰撞
D.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子百分数,从而使反应速率增大
参考答案:B
本题解析:A 错误,某一反应的活化分子百分数不是定值,随温度、压强的改变而改变。
B 正确,升温,活化分子百分数增多,有效碰撞增多,反应速率加快。
C 错误,活化分子之间发生的碰撞不一定为有效碰撞
D 错误,对有气体参加的化学反应,加压,可增加活化分子数,活化分子百分数不变。
本题难度:一般
2、选择题 肯定能使化学反应速率加快的方法是?(?)
①升高温度②加入催化剂③增加反应物浓度④将固体块状反应物磨成粉末
A.②
B.①②
C.①③④
D.①②③④
参考答案:D
本题解析:增大反应速率的外因可以是:升温、加入催化剂、增加浓度、增加固体的接触面积。
本题难度:简单
3、选择题 已知反应A+3B=2C+D在某段时间内以A的浓度变化表示的反应速率为1mol/(L?min),则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5?mol/(L?min)
B.1?mol/(L?min)
C.2?mol/(L?min)
D.3?mol/(L?min)
参考答案:对于反应A+3B=2C+D,以A的浓度变化表示的反应速率为1mol/(L?min),速率之比等于化学计量数之比,
所以1:2=1mol/(L?min):v(C),解得v(C)=2mol/(L?min),
故选C.
本题解析:
本题难度:简单
4、选择题 下列关于化学反应速率的说法正确的是
[? ]
A.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加
B.化学反应速率为0.8mol/(L・s)是指1s时某物质的浓度为0.8mol/L
C.根据化学反应速率的大小可以知道化学反应速率的快慢
D.对于任何化学反应来说,反应速率越大,反应现象就越明显
参考答案:C
本题解析:
本题难度:简单
5、填空题 (8分)为了研究MnO2与双氧水(H2O2)的反应速率,某学生加少许的MnO2粉末于 50 mL密度为1.1g?cm-3的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如下图所示。请依图回答下列问题:
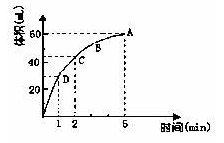
(1)实验时放出气体的总体积为 ___ ;
(2)放出一半气体所需要的时间为 ___ ;
(3)ABCD四点化学反应速率的由快到慢顺序为 ____ _______ ;
(4)在5min后,收集到的气体体积不再增加,原因是 。
参考答案:(8分) (1)60mL ; (2)1min ; (3) D>C>B>A ;(每空2分)
(4)此时双氧水已经完全分解;(2分)
本题解析:(1)根据图像可知,当气体的体积达到60ml时,就不再发生变化,所以实验时放出气体的总体积是60ml。
(2)当反应中生成3ml气体时,所用的时间是1min。
(3)反应速率越大,反映在曲线上,斜率就越大,所以ABCD四点化学反应速率的由快到慢顺序为D>C>B>A。
(4)5min后,收集到的气体体积不再增加,这说明反应物双氧水已经完全分解,不再产生氧气。
本题难度:一般