微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某恒温密闭容器发生可逆反应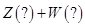

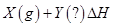 ,在
,在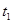 时刻反应达到平衡,在
时刻反应达到平衡,在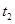 时刻缩小容器体积,
时刻缩小容器体积, 时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
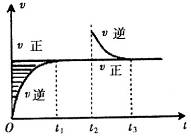
A.Z和W在该条件下至少有一个是为气态
B. 时间段与
时间段与 时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C.若在该温度下此反应平衡常数表达式为K=c(X),则 时间段与
时间段与 时刻后的X浓度不相等
时刻后的X浓度不相等
D.若该反应只在某温度 以上自发进行,则该反应的平衡常K随温度升高而增大
以上自发进行,则该反应的平衡常K随温度升高而增大
参考答案:D
本题解析:A、根据图象可知,正反应速率不随反应时间和压强的改变而改变,故Z和W都是不是气体,故A错误;B、结合图象可知,只有X是气体,所以反应过程中气体的摩尔质量始终不变,故B错误;C、由于化学平衡常数只与温度有关,该温度下平衡常数的表达式K=c(X)是定值,则t1~t2时间段与t3时刻后的c(X)相等,故C错误;D、由于该反应在温度为T0以上时才能自发进行,根据△H-T△S<0,得出该反应是吸热反应,升高温度平衡正向移动,平衡常数增大,故D正确;
本题难度:一般
2、填空题 (16分)“温室效应”是哥本哈根气候变化大会研究的环境问题之一,CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有?(填字母编号)。
a.采用节能技术,减少化石燃料的用量? b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)另一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l) =C2H4(g)+3O2(g)
ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l) = C2H5OH(1)+3O2(g)?错误!未找到引用源。ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇的热化学方程式是?。
(3)在一定条件下,6H2(g) +2CO2(g) CH3CH2OH(g)+3H2O(g)。?
CH3CH2OH(g)+3H2O(g)。?
 CO2转化率(%) CO2转化率(%)
n(H2)/n(CO2)
| 500
| 600
| 700
| 800
|
1.5
| 45
| 33
| 20
| 12
|
2
| 60
| 43
| 28
| 15
|
3
| 83
| 62
| 37
| 22
|
根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率?(填“增大”、“减小”或“不变”)。
②该反应的正反应为?(填“吸热”或“放热”)反应。
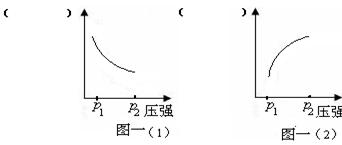
③在答卷的坐标系中作图,说明压强由p1增大到p2时,压强对该反应化学平衡的影响(图中纵坐标所表示的物理量需自己定义)。
参考答案:(1)abc(3分)
(2)C2H4(g)+H2O(l) = C2H5OH(l)?△H=-44.2 kJ/mol(3分)
(3)①增大(3分)?②放热(3分)
③CO2(或H2)的含量如图一(1);CO2(或H2)的转化率或乙醇的含量如图一(2)(4分,答案合理即可)
本题解析:略
本题难度:简单
3、选择题 在一定温度下,可逆反应N2(g)+3H2(g)?2NH3(g)达到化学反应限度的标志是( )
A.NH3的生成速率与H2的生成速率相等
B.单位时间内生成nmolN2同时生成3nmolN2
C.N2、H2、NH3的浓度不再变化
D.N2、H2、NH3分子数之比为1:3:2
参考答案:A、化学平衡是动态平衡,当反应达到平衡状态时,NH3的生成速率与H2的生成速率之比为2:1,而不是相等,故A错误;
B、单位时间内生成n mol N2同时生成3n mol N2,都表示的逆向,与正向无关,故B错误;
C、当体系达平衡状态时,N2、H2、NH3的浓度不再变化,说明正逆反应速率相等,故C正确;
D、当体系达平衡状态时,N2、H2、NH3分子数之比为1:3:2,也可能不是1:3:2,与各物质的初始浓度及转化率有关,故D错误;
故选C.
本题解析:
本题难度:一般
4、计算题 工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:

 (1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(1)己知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:______________________________________________;当温度升高时,该反应的平衡常数K值___________(填“增大”、“减小”或“不变”)。
(2)硝酸厂尾气常用的处理方法是催化还原法:催化剂存在时用H2将NO2还原为N2。已知:
2H2(g)+O2(g)=2H2O(g)?△H= a? kJ・mol-1
N2(g)+2O2(g)=2NO2(g)?△H= b? kJ・mol-1
H2O(1)=H2O(g)?△H= c? kJ・mol-1
则反应2NO2(g)+4H2(g)=N2(g)+4H2O(1)的△H=_________。(用a、b、c表示)
(3)①合成氨反应的化学方程式为N2+3H2 2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
2NH3,该反应在固定容积的密闭容器中进行。下列各项标志着该反应达到化学平衡状态的是____________(填序号)
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.3v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的相对分子质量保持不变
E.1mol N≡N键断裂,同时1mol H―H键断裂
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2L的密闭容器中,5min反应达平衡,n(N2)=1mol,n(H2)=1mol,n(NH3)=2mol,则反应速率v(N2)=________________,H2的平衡转化率=_________________;若保持容器的温度不变,在10min时将容器的容积压缩为lL,请在答题卡坐标图中,画出从反应开始至15min时c(NH3)随时间变化曲线示意图。

参考答案:(16分)
(1)4NH3+5O2 4NO + 6H2O? (2分)?减小(2分)
4NO + 6H2O? (2分)?减小(2分)
(2)(2a―b―4c)kJ/mol (2分,不写单位扣1分)
(3)①B C D(3分)
②0.1mol/(L・min)? (2分,不写或写错单位0分)? 75%(2分)

(共3分,前10min的曲线1分;10~15min的曲线2分,到达平衡的时间应小于15min,NH3平衡浓度小于2.67 mol/L)
本题解析:(1)氨气具有还原性,与氧气在催化剂加热作用下发生反应,生成一氧化氮和水,该反应是氧化还原反应、可逆反应、放热反应,氮元素由―3升为+2价,氧元素由0降为―2价,根据最小公倍数法配平,则4NH3+5O2 4NO + 6H2O;由于升高温度平衡向吸热方向移动,正反应是放热反应,则升高温度平衡向逆反应方向移动,则生成物浓度减小,反应物浓度增大,所以重新平衡时生成物浓度幂之积与反应物浓度幂之积的比值减小,即升高温度时该反应的平衡常数K减小;(2)先将4个热化学方程式分别编号为①②③④,由于①×2―②―③×4=④,根据盖斯定律,则④的焓变=①的焓变×2―②的焓变―③的焓变×4=(2a―b―4c)kJ/mol;(3)①容器内各组分浓度等于化学方程式的系数比,不能说明反应达到平衡,因为各组分变化浓度之比一定等于系数之比,而平衡浓度不一定等于系数之比,各组分浓度不随时间改变而改变才能说明达到平衡,故A错误;同一物质表示的正、逆反应速率相等,不同物质表示的正、逆反应速率之比等于化学方程式中对应系数之比时,都能说明反应达到平衡,v正(N2)/v逆(H2)=1/3,则3v正(N2)=v逆(H2),故B正确;合成氨是气体物质的量减小的反应,随着反应的进行,容器内混合气体的物质的量逐渐减小,则压强也逐渐减小,当混合气体总的物质的量保持不变或压强不变时,说明反应达到平衡,故C正确;由于各组分都是气体,因此混合气体的总质量始终不变,M=m/n=Mrg/mol,随着反应的进行,由于混合气体的总物质的量逐渐减小,则混合气体摩尔质量逐渐减小或相对分子质量逐渐减小,当混合气体物质的量不变或相对分子质量不变时,反应达到平衡,故D正确;N≡N键断裂、H―H键断裂都是正反应速率,故E错误;②由于氮气、氢气的起始物质的量未知,所以不能直接用定义式求氮气表示的速率,而氨气是生成物,起始时为0,则v(NH3)=
4NO + 6H2O;由于升高温度平衡向吸热方向移动,正反应是放热反应,则升高温度平衡向逆反应方向移动,则生成物浓度减小,反应物浓度增大,所以重新平衡时生成物浓度幂之积与反应物浓度幂之积的比值减小,即升高温度时该反应的平衡常数K减小;(2)先将4个热化学方程式分别编号为①②③④,由于①×2―②―③×4=④,根据盖斯定律,则④的焓变=①的焓变×2―②的焓变―③的焓变×4=(2a―b―4c)kJ/mol;(3)①容器内各组分浓度等于化学方程式的系数比,不能说明反应达到平衡,因为各组分变化浓度之比一定等于系数之比,而平衡浓度不一定等于系数之比,各组分浓度不随时间改变而改变才能说明达到平衡,故A错误;同一物质表示的正、逆反应速率相等,不同物质表示的正、逆反应速率之比等于化学方程式中对应系数之比时,都能说明反应达到平衡,v正(N2)/v逆(H2)=1/3,则3v正(N2)=v逆(H2),故B正确;合成氨是气体物质的量减小的反应,随着反应的进行,容器内混合气体的物质的量逐渐减小,则压强也逐渐减小,当混合气体总的物质的量保持不变或压强不变时,说明反应达到平衡,故C正确;由于各组分都是气体,因此混合气体的总质量始终不变,M=m/n=Mrg/mol,随着反应的进行,由于混合气体的总物质的量逐渐减小,则混合气体摩尔质量逐渐减小或相对分子质量逐渐减小,当混合气体物质的量不变或相对分子质量不变时,反应达到平衡,故D正确;N≡N键断裂、H―H键断裂都是正反应速率,故E错误;②由于氮气、氢气的起始物质的量未知,所以不能直接用定义式求氮气表示的速率,而氨气是生成物,起始时为0,则v(NH3)=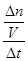 =
= 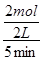 =0.2mol/(L?min);由于v(N2)/ v(NH3)=1/2,则v(N2)= 0.1mol/(L?min);设氮气、氢气的起始物质的量分别为xmol、ymol,则它们的起始浓度分别为x/2mol/L、y/2mol/L,则:
=0.2mol/(L?min);由于v(N2)/ v(NH3)=1/2,则v(N2)= 0.1mol/(L?min);设氮气、氢气的起始物质的量分别为xmol、ymol,则它们的起始浓度分别为x/2mol/L、y/2mol/L,则:
N2?+? 3H2? ?2NH3
?2NH3
起始浓度/ mol・L-1? x/2? y/2? 0
变化浓度/ mol・L-1? 1/2? 3/2? 1
平衡浓度/ mol・L-1? 1/2? 1/2? 1
则x/2―1/2=1/2,y/2―3/2=1/2,解得:x=2,y=4
氢气的平衡转化率= ×100%=
×100%=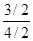 ×100%=75%。
×100%=75%。
画图要点:①t=0时,氨气浓度为0;t=5min,氨气浓度为1mol/L;0<t<5min时,氨气浓度逐渐增大;5min≤t<10min时,氨气浓度始终为1mol/L;②t=10min时,由于容器容积缩小1半,则反应物、生成物浓度立即增大一倍,则氨气浓度变为2mol/L;③缩小容器容积,就是增大压强,反应速率增大,达到平衡的时间大约是起始时达到平衡时间的一半,因此达到平衡的时间约为5/2min;若正反应能进行到底,氮气过量,4mol氢气最多可以生成8/3mol氨气,由于可逆反应不能进行到底,则浓度一定小于8/3mol/L≈2.67mol/L;10min<t≤12.5min时,由于正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,所以氨气浓度从2mol/L逐渐增大到2.5mol/L左右;④12.5min<t≤15min时,氨气浓度始终为2.5mol/L左右。
本题难度:一般
5、填空题 1体积SO2和3体积空气混合后,在450℃以上通过V2O5催化剂发生如下反应:2SO2(气)+O2(气)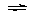 2SO3(气),若在同温同压下测得反应前后混合气体的密度比为0.9:1。则反应掉的SO2是原有SO2的___________%。
2SO3(气),若在同温同压下测得反应前后混合气体的密度比为0.9:1。则反应掉的SO2是原有SO2的___________%。
参考答案:80
本题解析:由阿伏加德罗定律的推论可知: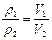 ,V2=0.9×(3+1)=3.6体积。
,V2=0.9×(3+1)=3.6体积。
设参加反应的SO2为x体积,由差量法
2SO2 + O2 2SO3?ΔV
2SO3?ΔV
2? 3-2=1
x ?4-3.6=0.4
2:1=x:0.4?解得x=0.8体积,所以反应掉的体积是原有SO2的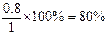 。
。
本题难度:一般