��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �������(KMnO4)��һ�ֳ��õ���������
(1)�����б仯��CO32����CO2��C2O42����CO2��Fe3����Fe2�����ҳ�����һ���仯�롰MnO4����Mn2�������һ����Ӧ��д���÷�Ӧ�����ӷ���ʽ��?��
(2)������ؿɴ����������������ȡCl2����Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ?��
(3)��������������������·�Ӧ��10FeS��6KMnO4��24H2SO4=3K2SO4��6MnSO4��5Fe2(SO4)3��10S��24H2O����������Ӧǰ����������������2.8 g������Ԫ����KMnO4֮�䷢��ת�Ƶĵ�����ĿΪ?��
�ο��𰸣�(1)2MnO4����16H����5C2O42��=2Mn2����10CO2����8H2O
(2)1��5��(3)0.15NA(��9.03��1022)
���������(1)MnO4����Mn2��Ϊ��ԭ���̣�����֮��Ӧ��ӦΪ��������C2O42����CO2�����ݵ�ʧ�����غ㽫����ʽ��ƽ���ɡ�(2)���������£�KMnO4��Һ�������Խ�ǿ������Ũ���ᷴӦʱ������ԭΪMn2�������ݵ����غ��֪�������ͻ�ԭ��(HCl)���ʵ���֮��Ϊ1��5��(3)���ݷ���ʽ�ɵù�ϵʽ��
10FeS������10S��������m������e��
880 g? 320 g? 560 g? 30 mol
2.8 g? n(e��)
n(e��)��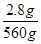 ��30 mol��0.15 mol��
��30 mol��0.15 mol��
�����Ѷȣ�һ��
2��ѡ���� ��ұ�������ȼ���״������һ����ҵ������ͼ��ʾ��������������Դ�������ʣ����ٻ�����Ⱦ��
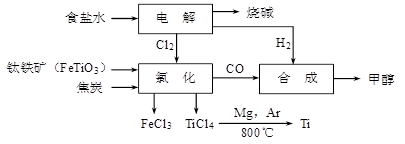
��ش��������⣺
��1��Fe��ԭ������Ϊ26��������������Ϊ2����д����ԭ�ӽṹʾ��ͼ_______��
��2��д���������ڸ������뽹̿���Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ?��
��3���ȼ���Cl2�����ӷ���ʽΪ??
?
| TiCl4
| Mg
| MgCl2
| Ti
|
�۵�/��
| ��25��0
| 648��8
| 714
| 1667
|
�е�/��
| 136��4
| 1090
| 1412
| 3287
|
?
��4����TiCl4��Ti��Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը���?�漴�ɡ�
��5��Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ ??ʱ��������Cl2�����������
�ο��𰸣���1��
��2��2FeTiO3��6C��7Cl2����2FeCl3��2TiCl4��6CO ��2�֣�
��3��2Cl- + 2H2O  ?H2�� + Cl2�� + 2OH-��2�֣�
?H2�� + Cl2�� + 2OH-��2�֣�
��4��1412?��2�֣�
��5��7��1
�����������1����λ��Ԫ�����ڱ��ĵ�4���ڵڢ��壬�ǹ��ɽ���Ԫ�صĴ�����ԭ������Ϊ26�����Ӳ�ṹΪ��
��2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪFeTiO3��6C��7Cl2����2FeCl3��2TiCl4��6CO��
��3����ҵ���õ�ⱥ��NaCl��Һ�ķ�������ȡNaOH��Cl2��H2����������Ϊԭ������һϵ�л�����Ʒ����Ϊ�ȼҵ��������Ӧ��2Cl����2e��=Cl2����������Ӧ����������Ӧ��2H��+2e��=H2������ԭ��Ӧ������ˣ���ⱥ��ʳ��ˮ���ܷ�Ӧ���Ա�ʾΪ��2Cl�� + 2H2O  ?H2�� + Cl2�� + 2OH����
?H2�� + Cl2�� + 2OH����
��4��Ar���н��з�ֹ�ѡ�þ�������������¶�ʹTiCl4��Mg��MgCl2ת��Ϊ������Ti���ۻ������¶��Ը���1412�棻
��5������2Cl�� + 2H2O  ?H2�� + Cl2�� + 2OH�����ٸ���ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+
?H2�� + Cl2�� + 2OH�����ٸ���ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+ 2FeCl3+2TiCl4+6CO���ó���ϵʽ2FeTiO3?~? 7Cl2?~ 14NaCl������Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ7��1ʱ��������Cl2�����������
2FeCl3+2TiCl4+6CO���ó���ϵʽ2FeTiO3?~? 7Cl2?~ 14NaCl������Ϊ�˼��ٲ�ҵ������ʱ�����Ĺ�ҵ���϶Ի�������в����NaCl��FeTiO3�����ʵ���֮��Ϊ7��1ʱ��������Cl2�����������
�����Ѷȣ�һ��
3��ѡ���� ��һ�������£�RO3n-�ͷ����ɷ������·�Ӧ��RO3n-+ F2 + 2OH-�T�T RO4-+ 2F-+ H2O ���Ӷ���֪��
RO3n-�У�Ԫ��R�Ļ��ϼ���
[? ]
A��+4
B��+5
C��+6
D��+7
�ο��𰸣�B
���������
�����Ѷȣ���
4������� ��6�֣�����ͭ��������ӻ�ͭ��ʼ����ͭ��ı��չ�������Ҫ��Ӧ֮һ�Ļ�ѧ����ʽΪ��2CuFeS2+O2= +2FeS+SO2��������ʽ����ƽ��
+2FeS+SO2��������ʽ����ƽ��
��1�������е�����ӦΪ_________?
��2������1 molSO2 ���ɣ���Ӧ�е���ת����ĿΪ____? _____
��3��SO2��?���
�ο��𰸣�(6��) (1)��Cu2S (2)�� 6NA? (3)������
�����������1������ԭ���غ��֪������������2��ͭԭ�Ӻ�1��Sԭ���γɵģ�������Cu2S��
��2�����ݷ���ʽ��֪��ÿ����2molCuFeS2�����б�������SԪ����1mol������ʧȥ���ӵ����ʵ�����[4������2��]mol��6mol�����ת�Ƶ��ӵ���Ŀ��6NA��
��3��SO2�ǻ�ԭ���е�SԪ�������������ģ��������������
�����Ѷȣ�һ��
5������� ��16�֣��Ĵ���֦���̲طḻ�ķ����ѡ�����Դ����������������Ҫ�ɷ�ΪTiO2 ��FeO��Fe2O3,Ti������ϼ�Ϊ+4����ԭ�ϣ�������ɫ���϶������ѵ�
��FeO��Fe2O3,Ti������ϼ�Ϊ+4����ԭ�ϣ�������ɫ���϶������ѵ� ��Ҫ�������£�
��Ҫ�������£�
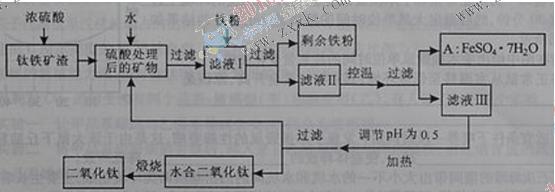
��ش��������⣺
��1��?������������ѷ�Ӧ�Ļ�ѧ����ʽ��____________________________________��
��2��?����ҺI�м������ۣ�������Ӧ�����ӷ���ʽΪ��_________________________��_______________________________________��
(3)��ʵ�����������У����ˮ�м�����Һ��ʹ���ҺpH��0.5�����ο�ʼˮ�⡣ˮ������в���ͨ�����ˮ������ά����Һ����һ��ʱ�䣬���γ��ˮ������ˮ�϶������ѳ�����������ѧ��ѧƽ��ԭ������ͨ�����ˮ���������ã�_______________________________________________��
���˷����ˮ�϶������ѳ�������Һ���ص���ҪĿ���dz��������Һ�е����Ρ�___________��______________��_______________________���ѧʽ�������ٷ����ŷš�
��4��A������������ɫ���ϣ�Fe2O3��,�䷽���ǣ���556a kg A��Ħ������Ϊ278 g/mol������ˮ�У�������������������Һǡ����ȫ��Ӧ�����������������裬�������ɫ���壻������ ɫ�����м���3336b kg A��112c kg���ۣ����������������裬��Ӧ��ɺ��д���Fe2O3�����ڽ����������Գ�����ʽ���������˺������������յú�ɫ���ϡ���������Һ������ֻ�������ƺ����������������Ͽ�������ɫ����_______________________kg��
ɫ�����м���3336b kg A��112c kg���ۣ����������������裬��Ӧ��ɺ��д���Fe2O3�����ڽ����������Գ�����ʽ���������˺������������յú�ɫ���ϡ���������Һ������ֻ�������ƺ����������������Ͽ�������ɫ����_______________________kg��
�ο��𰸣�
(1) 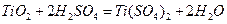 ��
��
(2)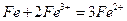 ?
?
(3) ��ˮ�ٽ�����ˮ�⣬���ȴٽ�����ˮ�⣬���� Ũ�ȴٽ�����ˮ��
Ũ�ȴٽ�����ˮ��
 ?
? ?
?
(4) 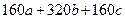
�����������
�����Ѷȣ���