微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C、D四种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D为同一主族,C元素的价电子排布为ns2πp2n,D在空气中燃烧可以得到淡黄色固体。又知四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体。请回答下列问题:
(1)D在元素周期表中的位置是?。
(2)比较元素B和C的第一电离能:B?C(填“大于”、“小于”或“不确定”),将BA3通入溴水中可发生反应,生成B的单质和一种盐Y,B的单质中的σ键和π键个数比为?,盐Y的晶体类型是?。
(3)D与A形成的粒子个数比为1:1的简单化合物可与水反应生成A的单质,该反应的化学方程式为?。
(4)已知B2A4和过氧化氢混合可作火箭推进剂。12.8g液态B2A4与足量过氧化氢反应生成B的单质和气态水,放出256.65kJ的热量:

写出液态B2A4和氧气反应生成B的单质和液态A2C的热化学方程式?。
参考答案:(1)第三周期IA族(2分)
(2)大于(2分)? 2(2分)?离子晶体(2分)
(3)NaH+H2O=NaOH+H2↑? (2分)
(4)N2H4(l)+O2(g)=N2(g)+2H2O(l)?△H="-621.2" kJ・mol-1(2分)
本题解析:由D在空气中燃烧得到淡黄色固体可知D为Na,再结合A、D同主族以及四种元素分别形成的常见单质在常温常压下有三种是气体,一种是固体可知,A一定为H,再结合B的价电子排布可推知B、C分别为N、O。(2)因N的2p轨道处于半充满的稳定状态,故第一电离能大于同周期相邻的氧元素;由氧化还原反应规律可得到盐Y为NH4 Br,属于离子晶体,在单质N2中存在氮氮三键,其中1个σ键和2个π键。(3)NaH与H2O发生归中反应得到H2与NaOH。(4)利用题给信息可知:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-641.6kJ/mol,然后利用“盖斯定律”结合已知热化学方程式进行变形即可。
本题难度:一般
2、选择题 下列说法中肯定不正确的是( )
①某原子K层上只有1个电子
②某原子M层上的电子数为L层上电子数的4倍
③某离子M层上和L层上的电子数均为K层的4倍
④某离子的核电荷数与最外层电子数相等
A.①③
B.②
C.③④
D.④
参考答案:B
本题解析:M层电子数最多为18个,L层电子数为8。
本题难度:一般
3、填空题 (15分)有A、B、C、D、E五种元素,元素A的一种原子无中子,元素B和C都有2 个电子层,它们能生成无色无味的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ar的电子层结构相同,试回答:
(1)元素名称是:? A______B______C______D_____E________。
(2)C元素位于第________周期,第________族
(3)B的最高价氧化物与E的最高价氧化物对应水化物反应
的离子方程式:?
(4)A和D的化合物与C和D的化合物(DC2)能否反应?
若能反应写出反应方程式。
参考答案:(1)氢、碳、氧、硫、钾(每空1分)?(2)二? VIA(每空1分)
(3)CO2+2OH-=CO32-+H2O 或? CO2+OH-= HCO3-?(3分)
(4)能(2分)2 H2S+SO2=3S↓+2H2O(3分)
本题解析:考查元素周期表的结构阳极原子核外电子排布。只有氢元素的原子才有可能没有中子,所以A是H。元素B和C都有2 个电子层,属于第二周期,它们能生成无色无味的气体BC2,气体是CO2,所以B是C,C是O。元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2,所以D是S,气体是SO2。E的阳离子E+的电子层结构与Ar的电子层结构相同,Ar的原子序数是18,则E是K。A和D的化合物与C和D的化合物(DC2)分别是H2S和SO2,其中S的化合价分别为-2价和+4价,所以二者可以发生氧化还原反应,生成酯基价态的单质硫,方程式为2 H2S+SO2=3S↓+2H2O。
本题难度:一般
4、选择题 列关于同主族元素的说法错误的是(? )
A.同主族元素随原子序数递增,元素原子的得电子能力逐渐增强
B.同主族元素随原子序数递增,单质氧化能力逐渐减弱
C.同主族元素原子最外层电子数都相同
D.同主族元素的原子半径,随原子序数增大而逐渐增大
参考答案:A
本题解析:主族元素随原子序数递增,元素原子的半径逐渐增大,所以失电子能力逐渐增强,得电子能力逐渐减弱。故A选项是错误的
本题难度:简单
5、填空题 (2009・安徽理综)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第_____周期第______族。W的气态氢化物稳定性比H2O(g)_____(填“强”或“弱”)。
(2)Y基态原子核外电子排布式是________,Y第一电离能比X的___?(填“大”或“小)
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是________________________________________________________________________。
(4)已知下列数据:Fe(s)+ (g)===FeO(s) ΔH=-272.0 kJ・mol-1
(g)===FeO(s) ΔH=-272.0 kJ・mol-1
2X(s)+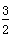 O2(g)===X2O3(s) ΔH=-1 675.7 kJ・mol-1
O2(g)===X2O3(s) ΔH=-1 675.7 kJ・mol-1
X的单质和FeO反应的热化学方程式是_________________________________________。
参考答案:(11分)(1)二 ⅤA 弱 ? (2)1s22s22p63s23p4 大
(3)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(4)3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s) ΔH=-859.7 kJ・mol-1
本题解析:W、Y的氧化物是导致酸雨的主要物质,则W是N元素,Y是S元素。X的基态原子核外有7个原子轨道填充了电子,且原子序数小于S的,所以X是Al元素。Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物,则Z是Cu。
(1)氮元素位于第二周期第ⅤA族。氮元素的非金属性弱于氧元素的,所以氨气的稳定性小于H2O的。
(2)根据构造原理可知,S元素基态原子的核外电子排布式是1s22s22p63s23p4。非金属性越强,第一电离能越大,则S元素的第一电离能大于Al元素的第一电离能。
(3)Y的最高价氧化物对应水化物的浓溶液是浓硫酸,所以与Cu的单质反应的化学方程式是Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(4)根据盖斯定律可知,①×3-②即得到3FeO(s)+2Al(s)===Al2O3(s)+3Fe(s),所以该反应的反应热ΔH=-272.0 kJ・mol-1×3+1 675.7 kJ・mol-1=-859.7 kJ・mol-1。
点评:该题是中等难度的试题,也是该中的常见考点和题型。试题综合性强,难易适中,侧重对学生能力的培养和解题方法与技巧的指导和训练。该题主要是以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般