微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 依据事实,写出下列反应的热化学反应方程式。
(1)在25℃、101kPa下,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为 。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量,则表示该反应的热化学方程式为 _________________________________________________。
(4)已知拆开1molH―H键,1molN―H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 。
参考答案:(1)CH3OH(l)+1.5O2(g)
本题解析:
本题难度:一般
2、填空题 (14分)燃煤和汽车尾气是造成空气污染产生雾霾的原因之一。消除汽车尾气是减少城市空气污染的热点研究课题。
(1)已知:①N2(g)+O2(g)=2NO(g) △H=+180.5kJ・mol-1
②CO(g)+1/2 O2(g)=CO2 (g) △H=-283kJ・mol-1
则汽车尾气中NO和CO在催化转化器中相互反应成无污染的气体的热化学方程式是_______________。
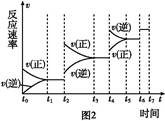
(2)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
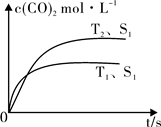
已知当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)在一定温度下,将2.0mol NO、2.4mol气体CO通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如图所示:

①有害气体NO的转化率为__________,0~15min NO的平均速率v(NO)=__________mol/(L・min)。(保留两位有效数字)
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是________(选填序号)。
a.缩小容器体积 b.增加CO的量
c.降低温度 d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将______移动(选填“向左”、“向右”或“不”),移动后在达到平衡时的平衡常数的值是_______(保留两位有效数字)。
(4)汽车尾气中的SO2和过氧化氢可设计成酸性原电池,请写出它的正极反应的方程式__________。
参考答案:(1)2NO(g)+2CO(g)=N2(g)+2CO2(g)) △H=-746.5kJ・mol-1;(2)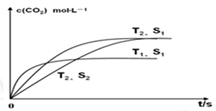
(3)①40% , 0.027;②c d;③向左,0.14 ;(4)H2O2+2e-+2H+=2H2O。
本题解析:(1)NO和CO转化成无污染的气体N2和CO2,②×2-①得出:2CO(g)+2CO(g)=N2(G)+2CO2(g) △H=-283×2-180.5kJ・mol-1=-746.5kJ・mol-1;(2)根据题意增大固体表面积可提高化学反应速率,S1>S2,在温度相同的情况下S1反应速率快达到平衡所用的时间短,图像:
 ;
;
(3)①消耗的n(CO)=(1.2-0.8)×2mol=0.4mol,根据反应方程式消耗的n(CO)和消耗的n(NO)是相等的,即消耗n(NO)=0.8mol,NO的转化0.8/2×100%=40%,0~15minNO的反应速率:v(NO)=0.8/(2×15)mol/(L・min)=0.027)mol/(L・min);②a、减小容器的体积,虽然平衡右移,但各组分的的浓度是增加的,错误;b、增加CO的量,CO的浓度增大,错误;c、此反应是放热反应,降低温度,平衡右移,CO的浓度减少,正确;d、增大容器的体积,虽然平衡左移,但各组分的浓度减小,正确,选项cd正确;③15min的平衡常数K=[c(N2)×c2(CO2)]/[c2(NO)×c2(CO)]=(0.2×0.42)/(0.82×0.62]=0.14,温度不变平衡常数不变,20min后再次达到化学平衡的平衡常数仍为0.14,K=[c(N2)×c2(CO2)]/[c2(NO)×c2(CO)]=(0.4×0.42)/(0.82×0.82]=0.16>0.14,化学平衡向左移动;(4)根据原电池的工作原理,正极上发生还原反应化合价降低,SO2具有还原性,H2O2具有氧化性,因此过氧化氢在正极上得电子,H2O2中的O是-1价变成0价,得到2mole-,根据反应前后所带电荷数相等,推出有H+参加反应,即H2O2+2H++2e-=2H2O。
考点:考查反应热的计算、化学平衡及化学平衡常数的计算、电极反应式的书写等知识。
本题难度:困难
3、填空题 (16分)I.一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g) FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H>0。1100℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示。
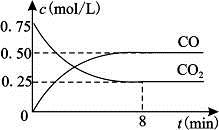
(1)8分钟内,CO的平均反应速率v(CO)=___________(结果保留3位有效数字)。
(2)1100℃时该反应的平衡常数K= (填数值);该温度下,若在8分钟时CO2和CO各增加0.5mol/L,此时平衡 移动(填“正向”、“逆向”或“不”)。
(3)1100℃时,2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器
| 甲
| 乙
|
反应物投入量
| 3molFe、2molCO2
| 4molFeO、3molCO
|
CO的浓度(mol/L)
| C1
| C2
|
CO2的体积分数
| φ1
| φ2
|
体系压强(Pa)
| P1
| P2
|
下列说法正确的是___________(填序号);
A.2C1 = 3C2 B.φ1 = φ2 C.P1<P2
II.(4)已知:①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq);ΔH=" a" kJ?mol-1
②H2O(l) H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
H+(aq)+OH-(aq);ΔH="b" kJ?mol-1
请写出Fe3+发生水解反应的热化学方程式: 。
(5)柠檬酸(用H3R表示)可用作酸洗剂,除去水垢中的氧化铁。
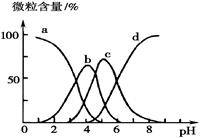
溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系如图所示。图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因是 (结合必要的方程式解释)。调节柠檬酸溶液的pH=4时,溶液中上述4种微粒含量最多的是 (填微粒符号)。
III.(6)高铁酸钠(Na2FeO4)广泛应用于净水、电池工业等领域,工业常用电解法制备,其原理为
Fe+2OH--+2H2O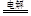 FeO42--+3H2↑
FeO42--+3H2↑
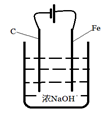
请设计一个电解池并在答题卡的方框内画出该装置的示意图并作相应标注。

其阳极反应式为:________________________________。
参考答案:(1)v(CO)=0.0625mol?L-1?min-1
(2)2 正
(3)B C
(4)Fe3+(aq) +3H2O(l)  Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1
Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1
(5)随溶液pH增大,平衡H3R H2R- + H+向右移动,所以,H3R的百分含量减小 ;H2R-
H2R- + H+向右移动,所以,H3R的百分含量减小 ;H2R-
(6)装置如图: Fe - 6e-+ 8OH-= FeO42-+ 4 H2O
Fe - 6e-+ 8OH-= FeO42-+ 4 H2O
本题解析:(1)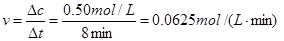 ;
;
(2)K= =
=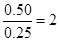 ,该温度下,在8分钟时CO2和CO各增加0.5mol/L,此时平衡正向移动;
,该温度下,在8分钟时CO2和CO各增加0.5mol/L,此时平衡正向移动;
(3)由数据可知,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡,且为等效平衡,达到平衡时,物质的浓度、转化率不随时间的变化而变化,故BC正确;
(4)①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
Fe3+(aq)+3OH-(aq) ; ΔH=" a" kJ?mol-1
②H2O(l)  H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
H+(aq)+OH-(aq) ;ΔH=" b" kJ?mol-1
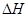 =
=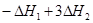 =(3b-a)kJ/mol
=(3b-a)kJ/mol
所以水解的热化学方程式为 Fe3+(aq) +3H2O(l)  Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1;
Fe(OH)3(aq) +3H+(aq) △H=(3b-a)kJ・mol-1;
(5)溶液中H3R、H2R-、HR2--、R3-的微粒数百分含量与pH的关系可由图可得,图中a曲线所代表的微粒数的百分含量随溶液pH的改变而变化的原因随溶液pH增大,平衡H3R H2R- + H+向右移动,所以,H3R的百分含量减小;调节柠檬酸溶液的pH=4时,溶液显酸性,使H3R
H2R- + H+向右移动,所以,H3R的百分含量减小;调节柠檬酸溶液的pH=4时,溶液显酸性,使H3R H2R- + H+被抑制,平衡逆移,这时含量最多的微粒为H2R-;
H2R- + H+被抑制,平衡逆移,这时含量最多的微粒为H2R-;
(6)由题可知反应原理为Fe+2OH--+2H2O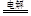 FeO42--+3H2↑,那么阳极为铁,故电极反应为Fe - 6e-+ 8OH-= FeO42-+ 4 H2O,电解池的装置图为
FeO42--+3H2↑,那么阳极为铁,故电极反应为Fe - 6e-+ 8OH-= FeO42-+ 4 H2O,电解池的装置图为
考点:反应速率的计算,平衡常数的计算,平衡移动方向的判断,热化学方程式的书写, 溶液中微粒种类的判断
本题难度:困难
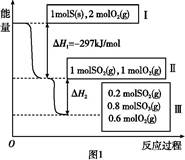
4、填空题 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。已知:2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
ΔH="-196.6" kJ/mol。
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式: 。
(2)ΔH2= 。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比
参考答案:
本题解析:
本题难度:困难
5、填空题 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据)。根据下图回答下列问题:
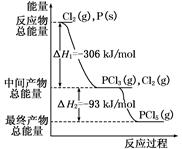
(1)P和Cl2反应生成PCl3的热化学方程式是 ;
(2)P和Cl2分两步反应生成1 mol PCl5的ΔH3= ,P和Cl2一步反应生成1 mol PCl5的ΔH4 ΔH3(填“大于”、“小于”、或“等于”)。
参考答案:(1)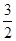 Cl2(g)+P(s)=PCl3(g) ΔH=-306 kJ/mol
Cl2(g)+P(s)=PCl3(g) ΔH=-306 kJ/mol
(2)-399 kJ/mol 等于
本题解析:(1)产物的总能量减去反应物的总能量就等于反应热,结合图像可知,PCl3和反应物P和Cl2的能量差值为306 kJ,因此该热化学反应方程式为:
P(s)+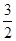 Cl2(g)=PCl3(g) ΔH=-306 kJ/mol。
Cl2(g)=PCl3(g) ΔH=-306 kJ/mol。
(2)根据盖斯定律求得:ΔH3=-399 kJ/mol,且ΔH3=ΔH4,与反应的途径无关,只与起始物质、最终物质有关。
本题难度:一般