微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (8分)标准状态下,将11.2 LHCI气体溶于水,制成250ml溶液。
(1)试求该盐酸溶液的物质的量浓度;
(2)如果用质量分数为36.5%密度为1.2 g/cm3 ?的浓盐酸来配制上述溶液,则应量取该浓盐酸多少毫升进行稀释。
参考答案:2 mol・L-1?41.7ml
本题解析:略
本题难度:简单
2、选择题 用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子
B.标准状况下,2.24 L水中含有6.02×1022个水分子
C.2.24 L氨气分子中含6.02×1023个电子
D.2.4 g金属镁变为镁离子时失去6.02×1022个电子
参考答案:A
本题解析:1.6g臭氧中含有氧原子的物质的量是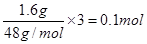 ,因此选项A正确;标准状况下,水不是气态,不能适用于气体摩尔体积,B不正确;C中没有指明氨气的状态,无法确定氨气的物质的量,C不正确;镁在反应中失去2个电子,则选项D中2.4 g金属镁变为镁离子时失去0.2×6.02×1023个电子,D不正确,答案选A。
,因此选项A正确;标准状况下,水不是气态,不能适用于气体摩尔体积,B不正确;C中没有指明氨气的状态,无法确定氨气的物质的量,C不正确;镁在反应中失去2个电子,则选项D中2.4 g金属镁变为镁离子时失去0.2×6.02×1023个电子,D不正确,答案选A。
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。
本题难度:一般
3、选择题 下列各溶液中NO3-物质的量浓度最大的是
A.20 mL 2 moL/L Mg(NO3)2
B.100 mL 2.5 mot/L NaNO3
C.25 mL 1.0mol/L Al(NO3)3
D.30 mL 2.5 mol/L NH4NO3
参考答案:A
本题解析:电解质产生的离子的浓度等于电解质的浓度与化学式中该离子的个数的乘积。A? C(NO3-)="2×2" moL/L="4" moL/L。B C(NO3-)="1×1.5" moL/L="1.5" moL/L。C C(NO3-)=3×1.0moL/L="3" moL/L。D C(NO3-)="1×2" .5moL/L="2.5" moL/L。所以浓度最大的是A。
本题难度:一般
4、选择题 将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是
A.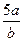 mol/L
mol/L
B.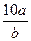 mol/L
mol/L
C.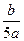 mol/
mol/ L
L
D.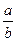 mol/L
mol/L
参考答案:B
本题解析:略
本题难度:一般
5、选择题 设NA表示阿伏加德罗常数,下列说法正确的是
A.在含有NA个CH3COO-的醋酸溶液中, H+ 数目略大于NA
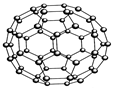
B.N60结构如右图,28gN60单质中含有的N-N键个数为NA
C.2.9g 熟石膏(2 CaSO4・H2O)含有的结晶水分子数为0.02NA
D.在标准状况下,2.24L的CCl4中含有C―Cl键的数目约为0.4NA
参考答案:A
本题解析:A正确,因为醋酸溶液中除了存在醋酸分子的电离平衡,也存在水的电离平衡;
B错,N60分子中的共价键数60×3÷2=90,28gN60物质的量为28g/(60×28)g.mol-1=1/60mol,
含有的共价键数90/60moL=1.5moL;
C错,2.9g熟石膏的物质的量为0.01mol,含有结晶水为0.01mol。
D错,四氯化碳在标准状况下是液体。
本题难度:一般