|
�߿���ѧ֪ʶ���������Ȼ�ѧ����ʽ����Ƶ����̣�2017�����°棩(��)
2017-07-10 19:58:17
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и���仯�У���H��Qǰ��С�ں��ߵ�һ����(����)��
��CH4(g)��2O2(g)=CO2(g)��2H2O(l)����H1
CH4(g)��2O2(g)=CO2(g)��2H2O(g)����H2
��2H2(g)��O2(g)=2H2O(l)����H1
H2(g)��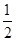 O2(g)=H2O(l)����H2 O2(g)=H2O(l)����H2
��t ��ʱ����һ�������£���1 mol SO2��1 mol O2�ֱ����ں��ݺͺ�ѹ�������ܱ������У��ﵽƽ��״̬ʱ�ų��������ֱ�ΪQ1��Q2
��CaCO3(s)=CaO(s)��CO2(g)����H1
CaO(s)��H2O(l)=Ca(OH)2(s)����H2
A���٢ڢ�
B���ڢ�
C���ڢۢ�
D���ۢ�
|
�ο��𰸣���A
�������������������Һ̬ˮ�ų��������࣬����HΪ��ֵ�����Ԧ�H1<��H2�����Ц�H1��2��H2<0�����к�ѹ�����·�Ӧ���еij̶ȴų��������ࣻ���Ц�H1>0����H2<0��
�����Ѷȣ�һ��
2������� ��1���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壬�ٽ�����ȼ�����Ӻ���ȡ��������ȼ�����ڻ����ɷų��������壮�Խ�����ԭ��______��
��ȡ356g����ʽΪCH4?9H2O�ġ���ȼ�����������ͷŵļ�����ȫȼ������Һ̬ˮ���ɷų�1?780.6kJ��������������ȼ����Ϊ______��
��2�������ѧ��������һ��ȼ�ϵ�أ�һ���缫ͨ���������һ�缫ͨ��Һ��ʯ��������C4H10��ʾ������صĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2-��
����֪�õ�صĸ�����ӦΪC4H10+13O2--26e-�T4CO2+5H2O����õ�ص�������ӦΪ______����ع���ʱ�������O2-��______���ƶ���
��Һ��ʯ����ȼ�ϵ�������ϰ���������Ӧ����ȫ��������______����д���ʵ����ƣ������缫������ͨ����
�ο��𰸣���1���١���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壬�ʴ�Ϊ������ȼ���������Ǹ�ѹ�¼�����ˮ�γɵģ��Ӻ���ȡ����ѹǿ��С�����ù��屾�����Ӽ�����������������Ի�ų��������壮
��356?g?CH4?9H2O�����ͷų�2?mol?CH4��������ȼ����Ϊ1?780.6?kJ��2?mol=890.3?kJ/mol��
��2���ٴ���Ϣ��ʾ��������ӦΪC4H10+13O2--26e-�T4CO2+5H2O��������Ӧ��ΪO2+4e-�T2O2-���õ��������ɸ��������O2-����������������ƶ���
��Һ��ʯ����������Ӧ����ȫ���ܲ���CO��C��CO���ܶ����缫������ͨ������ӦΪ����̿��
�ʴ�Ϊ����1���١���ȼ���������Ǹ�ѹ�¼�����ˮ�γɵģ��Ӻ���ȡ����ѹǿ��С�����ù��屾�����Ӽ�����������������Ի�ų��������塡��890.3?kJ/mol
��2����O2+4e-�T2O2-�������ڹ���̿
���������
�����Ѷȣ�һ��
3��ѡ���� �±��У����й����ӷ���ʽ���Ȼ�ѧ����ʽ�����ۺ�������
[? ]
���ӷ���ʽ���Ȼ�ѧ����ʽ
����
A.
NaHSO4�����ڣ�=Na++HSO4-
����HSO4-Ӧ����ΪH+��SO42-
B.
HCO3-+H2O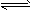 CO32-+H3O+? CO32-+H3O+?
��ȷ����HCO3-ˮ������ӷ���ʽ
C.
2H2(g)+O2(g)=2H2O(g) ��H=-241.8 kJ/mol
��ȷ��������ȼ����Ϊ-241.8 kJ/mol
D.
H+(aq) +OH-(aq)=H2O(l) ��H=+57.3 kJ/mol
�����кͷ�ӦΪ���ȷ�Ӧ
�ο��𰸣�D
���������
�����Ѷȣ���
4��ѡ���� ����˵����ȷ����
A����4molHCl��Ũ����������MnO2��ַ�Ӧ��ת��2NA������
B��500�桢30MPa�£���0.2mol N2��0.6molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������7.72kJ�����Ȼ�ѧ����ʽΪ��N2(g) + 3H2(g) 2NH3(g)��H=��38.6kJ��mol��1 2NH3(g)��H=��38.6kJ��mol��1
C�����ڿ��淴ӦN2(g)+3H2(g)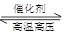 2NH3(g)��H 2NH3(g)��H
�ο��𰸣�
���������
�����Ѷȣ�һ��
5������� 2SO2(g)+O2(g)  2SO3(g)��Ӧ���̵������仯��ͼ��ʾ�� 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ��
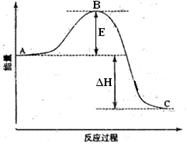
��֪1mol SO2(g)����Ϊ1mol SO3�Ħ�H=-99kJ��mol-1.��ش��������⣺
��1��ͼ��C��ʾ ;�÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�㽵�ͣ������� ��
��2��ͼ�С�H= kJ��mol-1��
��3�������Ӧ���ʦԣ�SO2��Ϊ0.05 mol��L-1��min-1,��ԣ�O2��= mol��L-1��min-1��
��4����֪�������ȼ����Ϊ296 KJ��mol-1��������S(s)����3 molSO3(g)�ġ�H= ��
�ο��𰸣�(1)�������������������ܽ��ͷ�Ӧ����Ҫ�������������Ӱٷ���
��2��-198 ��3��0.025 ��4��-1185kJ/mol
�����������1��ͼ��A��ʾ��Ӧ����������C��ʾ��������������EΪ��ܣ�ʹ�ô�������ܽ��ͣ�����������ӣ�����Ӱٷ������ӡ�
��2��1mol SO2(g)����Ϊ1mol SO3�Ħ�H=-99kJ��mol-1������2SO2(g)+O2(g)  2SO3(g) ��H=-198kJ��mol-1�� 2SO3(g) ��H=-198kJ��mol-1��
��3����ѧ��Ӧ���ʱȵ��ڻ�ѧ�������ȡ�
��4�������ȼ���ȿ�д���Ȼ�ѧ����ʽ��S(g)+O2(g)=SO2(g) ��H=-296kJ��mol-1����2SO2(g)+O2(g)  2SO3(g) ��H=-198kJ��mol-1���ø�˹���ɵ�S(g)+O2(g)=SO3(g) ��H=-395kJ��mol-1����������3 molSO3(g)�ġ�H=-1185kJ/mol�� 2SO3(g) ��H=-198kJ��mol-1���ø�˹���ɵ�S(g)+O2(g)=SO3(g) ��H=-395kJ��mol-1����������3 molSO3(g)�ġ�H=-1185kJ/mol��
���㣺��ѧ��Ӧ������ ��� �Ȼ�ѧ����ʽ ��˹����
�������Ȼ�ѧ�����л�ѧ��������ʾ���ʵ�����
�����Ѷȣ�һ��
|