|
|
|
高考化学知识点整理《热化学方程式》高频试题巩固(2017年最新版)(五)
2017-07-10 19:58:17
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据热化学方程S(s)+ O2(g)= SO2(g)△H = -297.23 kJ/mol(反应在25℃,101kPa下发生)分析下列说法不正确的是
[? ]
A.标况下,燃烧1mol S放出的热量为297.23 kJ
B.S(g)+ O2(g)= SO2(g)放出的热量大于297.23 kJ
C.S(g)+ O2(g)= SO2(g)放出的热量小于297.23 kJ
D.形成1mol SO2(g)的化学键所释放的总能量大于断裂1 mol S(s)和 1mol O2(g)的化学键所吸收的总能量
2、填空题 (10分)氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。常用电离常数Kb和电离度α来定量表示氨水的电离程度,它们均可通过各浓度氨水对应的c(OH-)进行换算。下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50 mL碱式滴定管、100mL烧杯、 0.10 mol・L-1氨水
【实验数据】(不必填表格)
烧杯号
| V氨水 (mL)
| V水(mL)
| c (NH3・H2O) (mol・L-1)
| c(OH-)
| Kb
| α
| 1
| 50.00
| 0.00
|
| 1.34×10-3
|
|
| 2
| 25.00
| 25.00
|
| 9.48×10-4
|
|
| 3
| 5.00
| 45.00
|
| 4.24×10-4
|
|
|
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb 。 。
(2)用0.10mol・L―1盐酸分别滴定20.00mL0.10mol・L―1
的NaOH溶液和20.00mL0.10mol・L―1氨水所得的滴定曲线如图。

请指出盐酸滴定氨水的曲线为 (填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 。
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料。其总反应式为4NH3+3O2= 2N2+6H2O,正极上的电极反应式为O2+2H2O+4e―=4OH―,则负极上的电极反应式为 。
3、填空题 (8分)氨气主要用作致冷剂及制取铵盐和氨肥
(1)某研究小组在673K、30MPa条件下,在体积为VL的密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g),其n(H2)和n(NH3)随时间变化的关系如图所示.
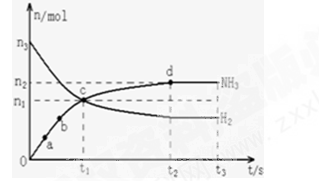
下列叙述正确的是 .
A.点a的正反应速率比点b的大
B.点c处反应达到化学平衡状态
C.若t3时由673K升至773K,则n(H2)将增大
D.t2、t3时刻,n(N2)不相等
| (2)在一定温度和催化剂下,将6.4mol H2和2.4molN2混合于一个容积为4L的密闭容器中发生反应,在3min末时反应恰好达平衡,此时生成了1.6mol NH3.①3min内以H2表示的化学反应速率 ;②该条件下的平衡常数
(3)已知:N2(g)+O2(g)=2NO(g)△H= +180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H= -92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H= -483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式:
4、填空题 (18分)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用研究。
(1)如将CO2与H2以1:3的体积比混合。
①适当条件下合成某烃和水,该烃是___ _(填序号)。
A.烷烃
B.烯烃
C.炔烃
D.苯的同系物
|
②适当条件下合成燃料甲醇和水。在体积为2L的密闭容器中,充入2 mol CO2和6 mol H2,
一定条件下发生反应:CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H=-49.0 kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。

的转化率=
;能使平衡体系中n(CH3OH)增大的措施有
。
(2)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。
己知:①CH4(g)+2O2(g)=CO2(g)+2H2O( l ) △H=-890.3kJ/mol
②2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是
。
(3)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池。写出以氢氧化钾为电解质的甲醇燃料电池负极反应式
。当电子转移的物质的量为________时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表。
溶解度(s)/g
| 溶度积(Ksp)
|
Ca(OH)2
| Ba(OH)2
| CaCO3
| BaCO3
|
0.16
| 3.89
| 2.9×10-9
| 2.6×10-9
|
吸收CO2最合适的试剂是__
__(填“Ca(OH)2”或“Ba(OH)2”)溶液。
5、选择题 已知热化学方程式C2H2(g)+5/2O2(g)=2CO2(g)+H2O(g);△H=-1256kJ/mol,下列说法正确的是
A.乙炔的燃烧热为1256kJ/mol
B.若转移10mol电子,则消耗2.5mol O2
C.若生成2mol液态水,则△H=-2512kJ/mol
D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ
