微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验装置(固定装置略去)和操作正确的是
[? ]
A.探究NH4HCO3的热稳定性
B.证明温度对平衡移动的影响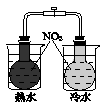
C.验证化学能转化为电能
D.碳酸、苯酚酸性强弱比较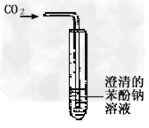
参考答案:BD
本题解析:
本题难度:一般
2、选择题 下述实验能达到预期目的是
A.A
B.B
C.C
D.D
参考答案:A
本题解析:分析:A.Na2CO3溶液中存在水解平衡,加入CaC12溶液水解平衡逆向移动,c(OH-)减小;
B.发生氧化还原反应;
C.水解后应利用碱中和酸至碱性;
D.乙醇易挥发,且乙醇能被高锰酸钾氧化.
解答:A.因Na2CO3溶液中存在水解平衡,加入CaC12溶液,碳酸根离子与钙离子结合生成沉淀,导致水解平衡逆向移动,c(OH-)减小,所以红色褪去,故A正确;
B.将SO2通入中KMnO4溶液中发生氧化还原反应,说明SO2具有还原性,故B错误;
C.淀粉溶液和稀H2SO4混合加热,水解后生成葡萄糖,然后应加碱中和酸至碱性,然后加新制的Cu(OH)2悬浊液加热至沸腾检验葡萄糖,故C错误;
D.乙醇易挥发,且乙醇能被高锰酸钾氧化,所以将乙醇与浓硫酸共热制得的气体中有乙烯和乙醇,通入酸性KMnO4溶液中褪色,不能确定一定是乙烯,故D错误;
故选A.
点评:本题考查实验方案的评价,题目难度中等,明确物质的性质及发生的化学反应、反应的条件等时解答本题的关键,选项C为易错点.
本题难度:简单
3、简答题 某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3?H2O.该小组探究过程如下:
●查阅资料:
①镁、铝、锌都是银白色的金属
②锌(Zn)可以与NaOH溶液反应生成H2
③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O
④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+
|
●提出假设:
(1)假设①:该混合金属粉末中除镁外还含有______元素
假设②:该混合金属粉末中除镁外还含有______元素
假设③:该混合金属粉末中除镁外还含有铝、锌元素
●实验探究:
甲同学基于假设③设计实验方案如下:乙同学同样基于假设③设计另一实验方案如下:

(2)试剂M是______;沉淀B是______.
(3)丙同学认为乙同学的方案比甲同学的好,理由是______.
(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是______.
(5)操作Ⅰ的主要过程是:在滤液中逐滴加入______,直至生成的沉淀刚好溶解,再加入足量的______.
(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图象正确的是______.
参考答案:(1)除Mg外,还含有Al、Zn中的一种或两种,因此粉末的组成有三种可能,即除Mg外只含Al、只含Zn、或既含Al又含Zn,故答案为:Al;Zn;
(2)由实验方案可知镁盐、铝盐和锌盐形成的沉淀分三次分离,第一次为:Mg(OH)2,试剂M为NaOH溶液,第二次为:Al(OH)3,铝盐和锌盐加过量的强碱先生成了沉淀,然后沉淀溶解,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解又形成了铝盐和锌盐,锌盐加过量的弱碱先生成了沉淀,然后沉淀溶解,铝盐加过量的弱碱也生成了沉淀,然后沉淀不溶解,实现了Al(OH)3沉淀的分离;第三次为Zn(OH)2,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加入适量的NaOH溶液,形成沉淀,故答案为:NaOH溶液;Al(OH)3;
(3)对比甲、乙两同学的实验,发现甲比乙多了第一步加稀硫酸,故答案为:步骤简单,节约试剂;
(4)锌、铝都能与NaOH溶液反应溶解,而镁不能与NaOH溶液反应,所以只需将沉淀C洗涤、小心干燥后称量即可得到镁的质量,故答案为:将沉淀C洗涤、小心干燥后称量;
(5)铝盐和锌盐加过量的强碱先生成了沉淀,然后沉淀溶解,在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,又形成了铝盐和锌盐,锌盐加过量的弱碱先生成了沉淀,然后沉淀溶解,铝盐加过量的弱碱也生成了沉淀,然后沉淀不溶解,这样实现了Al(OH)3沉淀的分离,故答案为:稀硫酸;稀氨水;?
(6)先发生的反应是Al3+和Zn2+与OH-生成沉淀,随后随着NaOH的加入,沉淀减少直至消失,此时是因为生成的沉淀都能溶解在NaOH溶液中,但Al(OH)3~NaOH,Zn(OH)2~2NaOH,所以相同物质的量的沉淀溶解消耗的NaOH不同,最后NH4+和OH-反应生成NH3?H2O,故选:B.
本题解析:
本题难度:一般
4、实验题 Ⅰ.某同学欲测定硫酸铜晶体中结晶水的含量。他列出的实验用品为:硫酸铜晶体试样、研钵、坩埚、坩埚钳、酒精灯、三脚架、玻璃棒、药匙、托盘天平。回答下面问题:
(1)完成本实验还需要的实验用品有_________。
(2)下面的情况有可能造成测定结果偏低的是_________?(填序号)?。
A.试样中含有易挥发的杂质?
B.加热时有晶体溅出
C.晶体加热脱水不完全?
D.实验前坩埚未完全干燥?
E.硫酸铜受热分解
Ⅱ.该同学发现硫酸铜晶体加热后变黑,查阅资料得知:?硫酸铜在加热条件下生成 。现用下图所示的装置验证硫酸铜在加热分解时有SO2产生,并测量产生的O2的体积。试填写下列空白:
。现用下图所示的装置验证硫酸铜在加热分解时有SO2产生,并测量产生的O2的体积。试填写下列空白:
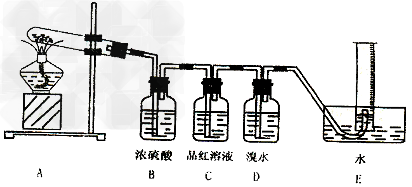
(3)硫酸铜受热分解的化学方程式为_________。
(4)装置B的作用是_________?,装置D的作用是_________。
(5)停止加热时,测量收集到的气体体积必须包括以下几步:
①__________________;?
②调整量筒内外液面高度使之相同;
③读取量筒内气体的体积。
(6)测量收集到的气体体积时,如何使量筒内外液面的高度相同?__________________。
(7)Y为ⅥA族元素构成的气态单质,将Y和SO2分别通入品红溶液,都能使品红溶液褪色。则Y的化学式为_________;简述区别二者的实验方法__________________。
参考答案:(1)泥三角、干燥器
(2)?C
(3)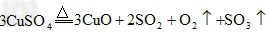
(4)吸收反应后的三氧化硫气体;除尽二氧化硫
(5)使试管和量筒内的气体都冷却至室温
(6)慢慢将量筒下移
(5)O3;加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2,否则为O3。
本题解析:
本题难度:一般
5、选择题 下列实验不能达到预期目的的是
[? ]
实验操作 实验目的
A.Cl2、Br2分别与H2反应 比较Cl2、Br2的非金属性强弱
B.Cl2、S分别与Fe反应 比较Cl2、S的氧化性强弱
C.测定相同浓度的Na2CO3、Na2SO4两溶液的pH 比较碳酸、硫酸的稳定性强弱
D.测定相同浓度的盐酸、醋酸两溶液的导电性 比较盐酸、醋酸的酸性强弱?
参考答案:C
本题解析:
本题难度:一般