��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��Ӧ��2SO2+O2
2SO3������Ӧ���ʷֱ���v��SO2����v��O2����v��SO3����ʾ�������й�ϵ��ȷ���ǣ�������
A��v��SO2��=v��O2��
B��v��SO2��=v��SO3��
C��v��O2��=v��SO3��
D��2v��SO2��=v��O2��
�ο��𰸣����ڷ�Ӧ2SO2+O2����
���������
�����Ѷȣ���
2������� �����������Һ��ϡ����ķ�Ӧ����ʽΪ��Na2S2O3+H2SO4�TNa2SO4+S��+SO2+H2O��ijʵ����ȤС������ͼ��ʾ��ʵ��װ��̽����������Ի�ѧ��Ӧ���ʵ�Ӱ�죨���������ͼг���������ʡ�ԣ���
��1��ʵ��Ŀ�ģ�װ�üף�̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죻װ���ң�̽��______�Ի�ѧ��Ӧ���ʵ�Ӱ�죮
��2��ͨ���ס���װ�ã��ֱ����������ʵ�飬���ݼ�¼���£����������ó���ؽ��ۣ�
ʵ��
��� | �¶� | Na2S2O3��Һ | H2SO4 | ����H2O����� | ���ֳ�������ʱ��
���
Ũ��
���
Ũ��
��
0��
5mL
0.1mol?L-1
10mL
0.1mol?L-1
5mL
8s
��
0��
5mL
0.1mol?L-1
5mL
0.1mol?L-1
10mL
12s
��
30��
5mL
0.1mol?L-1
5mL
0.1mol?L-1
10mL
4s
|
����1���ɢ�͢��������ݿ�֪______��
����2���ɢ�͢��������ݿ�֪______��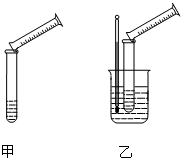
�ο��𰸣���1���������¶ȼƣ��¶ȼƵ������Dz�����Һ���¶ȣ��ʴ�Ϊ���¶ȣ�
��2������1����͢��������ݵIJ�ͬ����ϡ����������ˮ����������ֳ�����ʱ�䣬����ϡ�����Ũ�ȱȢ��д��г��ֳ����Ȣ����磬���Ԣ�Ӧ���ʱȢ��д�������������һ��ʱ����Ӧ��Ũ��Խ������Խ�죻
��͢��������ݵIJ�ͬ���ǣ�����¶ȱȢ�ߣ�����ֵij����Ȣ��磬���ԣ���ķ�Ӧ���ʱȢ��������������һ��ʱ���¶�Խ�ߣ�����Խ�죮
�ʴ�Ϊ����������һ��ʱ����Ӧ��Ũ��Խ������Խ�죻��������һ��ʱ���¶�Խ�ߣ�����Խ�죮
���������
�����Ѷȣ�һ��
3��ѡ���� A��B���ݻ�Ϊ1 L���ܱ������з�����Ӧ��aA(s)+bB(g) cC(g)+dD(g)��t1����t2ʱ�̷ֱ��ò����������±���
cC(g)+dD(g)��t1����t2ʱ�̷ֱ��ò����������±���

����˵����ȷ����
A��0��t1ʱ����ڣ�ƽ����Ӧ����v(B)=O��04/t1 mol��(L��min)-1
B������ʼʱn(D)=0����t2ʱv(D)=0��20/t2 mol��(L��min)-1
C�������¶ȣ�v(B)��vC)��v(D)������
D��b��d=6��1
�ο��𰸣�C
���������A�� B����ʼ������֪�������0��t1min�ڵ�ƽ�����ʡ�B�� v(D)=0��20/t2 mol��(L��min)-1Ϊ0��t1ʱ�����ƽ�����ʶ���t1ʱ�̵�˲ʱ���ʡ���B����C�������¶ȣ���ѧ��Ӧ����������ȷ��D���ɱ������ݿɵã�t1��t2ʱ�����
aA(s)+bB(g)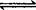 cC(g)+dD(g)
cC(g)+dD(g)
��n /mol 0.06 0.06 0.1
���ԣ�b��c:d=3:3:5 ��D����
���㣺�˽⻯ѧ��Ӧ���ʵĸ����Ӧ���ʵĶ�����ʾ�������������������Ũ�ȡ��¶ȡ�ѹǿ�������ȣ��Է�Ӧ���ʵ�Ӱ�죬��ʶ��һ����ɡ�
�����Ѷȣ�һ��
4������� ij��Ӧ�ڴ����������£��������������У���һ����X+Y=Z;�ڶ�����Y+Z=M+N+X���˷�Ӧ�ܵĻ�ѧ����ʽ��____________________����Ӧ�Ĵ�����___________��
�ο��𰸣�2Y=M+N��X
���������
�����Ѷȣ�һ��
5��ѡ���� п����ϡ���ᷴӦһ��ʱ���Ӧ���ʼ�������ʱ�����Ȼ����Ũ���ᣬ�÷�Ӧ�������Լӿ졣�ɴ��жϣ�Ӱ�컯ѧ��Ӧ���ʵ�������
[? ]
���¶� �ڹ���ı���� �۷�Ӧ���״̬ ����Һ��Ũ�� �ݴ���
A���٢�
B���ڢ�
C���٢�
D���٢ڢۢܢ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��