��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪��EΪ�����������ʣ�C��D��F��I��Ϊ�������壬����C��DΪ���ʣ�F��IΪ����������Ԫ����ͬ��D��F�ж���IΪֱ���ͷǼ��Է��ӣ����������¿�ͼ��ϵ��

��1����Ӧ�������ĵ缫��Ӧʽ?��
��2����Ӧ�۵Ļ�ѧ����ʽ?��
��3����Ӧ�ܵ����ӷ���ʽΪ?��
��4��K��һ��������ˮ�Ĺ��壬K���ȷֽ������H��ʵ����G��Һ��K��ת��ʱ���Լ�����Լ��ǣ���дѡ����ĸ��?
A��NaOH��Һ?B����ˮ ?C��Na2CO3��Һ?D��NaHCO3��Һ
��5����G�ı�����Һ���뵽��ˮ�У��������ȿɵú��ɫҺ�壬д����Ӧ�����ӷ���ʽ��??
��Һ���ֱͨ�����___? __��������ɫ������ֹ��̽���____? _��
��6����E�к��кϽ�Ԫ�أ��ᵼ��G�������ⶨG����������ͨ�����õ������ⶨ����ȡmg��ˮG��Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ���ݣ�ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���õ�����ָʾ������cmol��L-1Na2S2O3��Һ�ζ���I2+2S2O32-=2I�� +S4O62����������ȥVmL�������ʲ����뷴Ӧ�� ����Ʒ��G����������Ϊ��?����??��
����Ʒ��G����������Ϊ��?����??��
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2������� a��b��c��d��e�Ǻ���һ����ͬԪ�ص��������ʣ��ɷ�����ͼת�������У�a�ǵ��ʣ�b�����壻c��d�������e������������Ӧ��ˮ���
��1�����a��һ�ֵ���ɫ��ĩ���壬���ƶ����������ʣ������Ʊ�ʾ����
a______��b______��c______��d______��e______��
��д����c����d�Ļ�ѧ����ʽ______
��2�����aΪ��������һ�ֳ������壬���ƶ����������ʣ��û�ѧʽ��ʾ����
a______��b______��c______��d______��e______��
��д����d����e�Ļ�ѧ����ʽ______��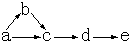
�ο��𰸣�����ɫ����Ϊ�������ܷ���������������Ӧ�ķ�Ӧ����͵�Ԫ�ص�ת����
��1��a�����ǵ���ɫ��ĩ�����ܹ���������������������a�����Ƿǽ�����bΪ���⣬cΪ��������dΪ��������eΪ���ᣬc����d�ķ�ӦΪ2SO2+O2����
���������
�����Ѷȣ�һ��
3������� ��֪����ӵ�Դ���������ĵ缫Ϊ���ص�����������ӵ�Դ���������ĵ缫Ϊ���ص�����������ʯīΪ�缫���ʱ���������Һ�е�����������������������Ӧ���������Һ�е�������������������ԭ��Ӧ����֪�����ӵõ��ӵ����������Ӧ�����Ľ������˳���෴��ע�⣺Fe3+��Cu2+��Fe2+����������ʧ���ӵ�����ΪS2-��I-��Br-��Cl-��OH-������������ӣ�F-����ͼ��ʾ����ʯīΪ�缫���A��ˮ��Һ����������һϵ��ʵ�飬�Ը���ʵ����������������⣮�����A��ˮ��Һ��ɫ��Ӧ��dz��ɫ��
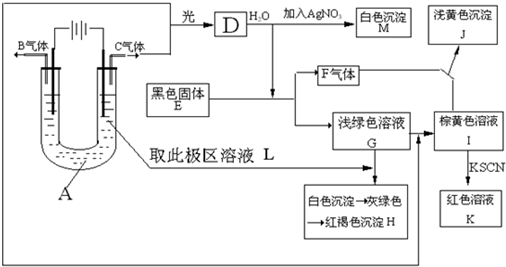
��1��д��A�Ļ�ѧʽΪ______��E������Ϊ______��
��2��I��F���õ����ӷ���ʽ��______
��3��G����L������İ�ɫ���������ɺ��ɫ����H�Ļ�ѧ����ʽ��______
��4����������ֱ�ӵ����ӷ���ʽ��֤��Fe3+��Cu2+��Fe2+��������ǿ��˳����Fe3+��Cu2+��Fe2+
��______����______��
�ο��𰸣������A��ˮ��Һ��ɫ��Ӧ��dz��ɫ���ɴ˿�֪�����A���м�Ԫ�أ�������������dz��ɫ������G�����������ӣ�G��L��Ӧ����H������ʵ������֪��H ������������������ҺL�����������ӣ������A���Һ�к������������ӣ�C��G��Ӧ����I��I�����軯�ط�Ӧ���ɺ�ɫ��ҺK�������������Ի�ɫ������I�����������ӣ����������Ӻ�C��Ӧ�������������ӣ�����C��������I���Ȼ�����Һ��G���Ȼ�������Һ������A���Ȼ��أ�����Ȼ�����Һʱ�����������������������������أ�����B��������L������������Һ��B��C��������D���������������������Ȼ��⣬����D���Ȼ��⣻�Ȼ�������ˮ�����ᣬ�������������Ӧ���ɰ�ɫ�����Ȼ���������M���Ȼ�������ɫ����E�����ᷴӦ����������������F��F���Ȼ�����Ӧ���ɵ���ɫ����J������ɫ�����й������ơ����廯����������������Һ�в����ڣ����Բ��ǹ������ƣ��Ȼ��������岻�������廯�������Ե���ɫ��������ɫ������������������F���������壮
��1��ͨ�����Ϸ���֪��AΪKCl��E����������
�ʴ�Ϊ��A��KCl?E����������
��2��ͨ�����Ϸ���֪��I���Ȼ�����Һ��F�����⣬�Ȼ����������ԣ������л�ԭ�ԣ������Ȼ����������ܷ���������ԭ��Ӧ�����Ȼ����������ʡ����ᣬ���ӷ���ʽΪ��2Fe3++H2S=2Fe2++S��+2H+��
�ʴ�Ϊ��2Fe3++H2S=2Fe2++S��+2H+��
��3��ͨ�����Ϸ���֪��G���Ȼ�������Һ��L������������Һ���Ȼ��������������Ʒ�Ӧ�����������������������������ȶ����ܱ������е�������������������������Ӧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3 ��
�ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3 ��
��4����ΪFe3+��Cu2+��Fe2+��������ǿ��˳����Fe3+��Cu2+��Fe2+������ֻҪ��ͬһ��Ӧ����ʽ��Fe3+����������
Cu2+���������T��֤�����������ӵ������Դ���ͭ���ӵ������ԣ�2Fe3++Cu=2Fe2++Cu2+��?����һ��Ӧ����ʽ�У�ͭ�������������������������������T��֤��ͭ���ӵ������Դ����������ӵ�������Fe+Cu2+=Fe2++Cu��
�ʴ�Ϊ��2Fe3++Cu=2Fe2++Cu2+��Fe+Cu2+=Fe2++Cu��
���������
�����Ѷȣ�һ��
4������� ����A��B��C��D��E��F��G��H��I��J��K������ͼת����ϵ����������D��EΪ���ʣ��Իش�

��1��AԪ�ص�ԭ�ӽṹʾ��ͼΪ______��
��2��д���������ʵĻ�ѧʽ��E��______��K��______��
��3��������B����______���������ӡ����ۡ�����
��4��ʵ���Ҽ���J�������Ľ�������ʱ������J����Һ�м���______��Һ��
��5��д����Ӧ��F��G���Ļ�ѧ����ʽ��______��
��6��д����Ӧ��I��J�������ӷ���ʽ��______��
�ο��𰸣�KΪ���ɫ��������ӦΪFe��OH��3������ҺJ�к���Fe3+������HΪFe��DӦΪH2��EӦΪCl2��BΪHCl����IΪFeCl2��JΪFeCl3��KΪFe��OH��3����ɫ����F�����ڹ���NaOH��Һ����FΪAl��OH��3��GΪNaAlO2��AΪAl��CΪAlCl3��
��1��AΪAl��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3����ԭ�ӽṹʾ��ͼΪ

��
�ʴ�Ϊ��

��
��2�������Ϸ�����֪EΪCl2��KΪFe��OH��3���ʴ�Ϊ��Cl2��Fe��OH��3��
��3��BΪHCl��Ϊ���ۻ�����ʴ�Ϊ�����ۣ�
��4��JΪFeCl3���������軯�ط�����ɫ��Ӧ����Һ�ʺ�ɫ����������������Һ�����������������ɫ������
�ʴ�Ϊ�����軯����Һ������������Һ��
��5��FΪAl��OH��3��GΪNaAlO2����Ӧ��F��G���Ļ�ѧ����ʽΪAl��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��Al��OH��3+NaOH=NaAlO2+2H2O��
��6��IΪFeCl2��JΪFeCl3����Ӧ��I��J�������ӷ���ʽΪ2Fe2++Cl2=2Fe2++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe2++2Cl-��
���������
�����Ѷȣ�һ��
5������� �����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ�����
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ
A
��Ԫ�ص�һ��ԭ�ӣ�ԭ�Ӻ���û������
B
���������Ӳ㣬��K��M�������֮�͵���L�������
C
����Ϊ˫ԭ�ӷ��ӣ����⻯���ˮ��Һ�ʼ���
D
Ԫ�����������+7��
E
1mol?E�ĵ�����������ϡ���ᷴӦ���ɵõ�����33.6L?����״����
|
��1��д��BԪ����Ԫ�����ڱ��е�λ��______��
��2��д��CԪ����̬�⻯��ĵ���ʽ______��
��3��Ԫ��D��Ԫ��B��ȣ��ǽ����Խ�ǿ����______����Ԫ�ط��ű�ʾ����������������֤����һ��ʵ����______����������ţ���
�ٳ�����D�ĵ��ʺ�B�ĵ���״̬��ͬ
��D����̬�⻯���B����̬�⻯���ȶ�
��BԪ������������ˮ��������ǿ��DԪ������������ˮ��������
��4���ɱ���Ԫ���γɵij�������X��Y��Z��M��N��������ת����ϵ��

��N�Ļ�ѧʽΪ______��
��X��Һ��Y��Һ��Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�A����Ԫ�ص�һ��ԭ�ӣ�ԭ�Ӻ���û�����ӣ�������Ԫ�أ�
B��K���M���ϵ�����֮�͵���L���ϵ����ӣ����ԣ��������K�㣬�������M�㣬K����2�����ӣ�L����8�����ӣ�M����6�����ӣ���������Ԫ�أ�
C�������µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��ԣ������ǵ�Ԫ�أ�
D�����������Ϊ+7�ۣ�����Ԫ�ص�������=�����������������Ƕ�����Ԫ�أ���û�������ϼۣ���������Ԫ�أ�
E��1mol?E�ĵ�����������ϡ���ᷴӦ���ɵõ�����33.6L?����״���������ݵ��ӵ�ʧ�غ㣬��֪E�Ļ��ϼ�Ϊ+3�ۣ�Ϊ��Ԫ�أ�
��1����Ԫ�ص�ԭ�ӽṹʾ��ͼ��

��λ�����ڱ����������� �ڢ�A�壬�ʴ�Ϊ���������ڵڢ�A�壻
��2��CԪ����̬�⻯��ΪNH3�������ʽΪ��

���ʴ�Ϊ��

��
?��3������ͬ���ڷǽ������ʵı仯���ɼ��ȽϷǽ����Եķ�����������Cl�ķǽ����Ա�SԪ��ǿ��Cl���⻯���S���⻯���ȶ���ClԪ������������ˮ��������ǿ��SԪ������������ˮ����������˵��Z�ķǽ�����ǿ���ʴ�Ϊ��Cl���ڣ�
��4�����ݰ�ɫ����M���ȵõ�Z����֪MΪ����������NΪ���������ٸ���X+Y+H2O=Al��OH��3+M��ֻ���ǽ������Σ�����֪MΪ��Σ�����ʵ�����Ʊ�����������һ�ֳ���������
����NΪ����������ѧʽ��Al2O3���ʴ�Ϊ��Al2O3��
���Ȼ������ڰ�ˮ��Ӧ�õ������������Ȼ�泥�AlCl3++3NH3?H2O�TAl��OH��3��+3NH4Cl��
�ʴ�Ϊ��Al3++3NH3?H2O=Al��OH��3��+3NH4+��
���������
�����Ѷȣ�һ��