|
|
|
高考化学知识点总结《化学反应与能量》高频考点特训(2017年练习版)(三)
2017-07-10 20:20:43
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 离子间能大量共存,当溶液中c(H+)=10-1mol.L-1时有气体产生,而当溶液中c(H+)=10-13mol.L-1时又能产生沉淀,下列各组离子中符合上述要求的一组是
A.Ba2+、K+、S、Cl-
B.Na+、Cu2+、N、C
C.Mg2+、N、S、Cl-
D.Fe2+、Na+、S、N
2、选择题 下列4组实验操作或装置图(略去部分夹持仪器)中,有错误的图为几个
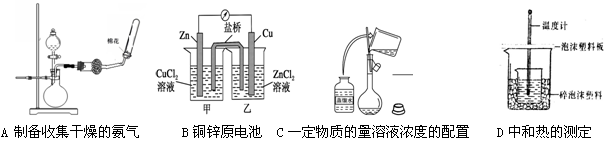
3、选择题 25℃、101kPa下:①2Na(s) + 1/2O2 (g)= Na2O(s) △H1 = -414kJ/mol
②2Na(s) + O2 (g)= Na2O2(s) △H2 = -511kJ/mol。下列说法正确的是
A.①的反应物总能量低于生成物总能量
B.因为△H2<△H1,所以Na2O2比Na2O稳定
C.常温下Na与O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa下,Na2O2(s) +2Na(s) =" 2" Na2O(s) △H = -317kJ/mol
|
4、选择题 已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g) △H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
A.△H1>△H2>△H3>△H4
B.△H4>△H2>△H3>△H1
C.△H3>△H4>△H1>△H2
D.△H4>△H3>△H2>△H1
|
5、填空题 Ⅰ.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表为一些化学键的键能数据
化学键
| Si-Si
| O=O
| Si-O
|
键能/kJ・mol-1
| a
| b
| c
|
写出硅高温燃烧的热化学方程式
。
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。写出下列电解池中总反应的离子方程式:

电解池A
。
电解池B
。
(2)若电解池A中生成3.36 L H2(标准状况),计算电解池B中生成Fe2+的物质的量为
mol。
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生如下反应:N2(g)+3H2(g)

2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
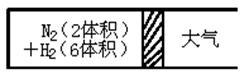
请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2 和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同。
①a=1,c=2,则b=
。在此情况下,反应起始时将向
反应方向(填“正”或“逆”)进行。
②若需规定起始时反应向逆方向进行,则c的取值范围是
。
(2)在上述恒压装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是
,原因是
。

 2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。
2NH3(g);△H<0,反应达到平衡后,测得混合气体为7体积。