微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的pH怎样变化?
A.不变
B.先变小后变大
C.逐渐变大
D.逐渐变小
参考答案:C
本题解析:试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,铜是正极,氢离子在正极得到电子,生成氢气而逸出,所以溶液中氢离子的难点降低,则pH逐渐增大,答案选C。
考点:考查题型原电池的有关判断、pH的计算
点评:该题是基础性试题的考查,属于常规性试题,难度不大。学生记住原理即可,该题有利于培养学生的学习自信心。
本题难度:困难
2、选择题 下列各组物质的晶体中,化学键类型和晶体类型都相同的是( )
A.CO2和SiO2
B.SiCl4和CCl4
C.白磷和金刚石
D.H2O2和Na2O2
参考答案:A.CO2和SiO2中均为共价键,但CO2为分子晶体,SiO2为原子晶体,故A不选;
B.SiCl4和CCl4中均为共价键,且均为分子晶体,故B选;
C.白磷和金刚石中均为非极性共价键,但白磷为分子晶体,金刚石为原子晶体,故C不选;
D.H2O2中含有共价键,为分子晶体,而Na2O2中含有离子键、共价键,为离子晶体,故D不选;
故选B.
本题解析:
本题难度:简单
3、实验题 50 mL 0.50 mol・L-1盐酸与50 mL 0.55 mol・L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
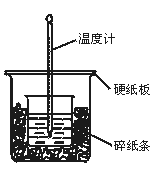
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol・L-1盐酸跟50 mL 0.55 mol・L-1NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等”“不相等”),所求中和热 (填“相等”“不相等”),简述理由: 。
参考答案:(1)环形玻璃搅拌棒(2)减少实验过程中的热量损失(3)减小
(4) 不等 相等 因为中和热是指酸和碱发生中和反应生成1molH2O所放出的热量,
与酸碱的用量无关
本题解析:中和热的测定过程中使用的酸和碱的量不同,反应放出的热量不同,但是中和热是指生成1mol水时放出的热量,所以中和热相同。
考点:中和热的测定。
本题难度:一般
4、选择题 下列晶体中,化学键种类相同,晶体类型也相同的是
A.CO2和SiO2
B.NaCl和HCl
C.O2和H2O
D.Si和N2
参考答案:C
本题解析:A中前者是含有极性键的分子晶体,后者是含有极性键的原子晶体。B中前者是含有离子键的离子晶体,后者是含有极性键的分子晶体。C中都是含有共价键的分子晶体。D中前者是含有非极性键的原子晶体,后者是含有非极性键的分子晶体。所以答案选C。
本题难度:一般
5、选择题 已知在101kPa,25℃条件下,1mol氢气燃烧生成水蒸气放出242kJ热量,下列热化学方程式正确的是
A.H2(g)+  O2(g)=H2O(g) ΔH=+242kJ?mol-1
O2(g)=H2O(g) ΔH=+242kJ?mol-1
B.2H2(g)+O2(g)=2H2O(g)ΔH=-484kJ?mol-1
C.H2(g)+  O2(g)=H2O(l)ΔH=-242kJ?mol-1
O2(g)=H2O(l)ΔH=-242kJ?mol-1
D.2H2(g)+O2(g)=2H2O(g)ΔH=-242kJ?mol-1