微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是?
[? ?]
A.从明矾是常用的净水剂可推测凡含有铝元素的物质都有净水作用
B.不同物质各有其特性,明矾可用作净水剂,Al2(SO4)3就不一定有净水作用
C.净水剂就是指能杀灭水中细菌和有害微生物的化学试剂
D.从理论上说,铝盐和铁盐都可用作净水剂
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列氧化物不能跟铝粉组成铝热剂的是( )。
A.Cr2O3
B.MnO2
C.MgO
D.V2O5
参考答案:C
本题解析:MgO和Al不能在熔融状态发生置换反应。
本题难度:简单
3、简答题 在标准状况下进行下列实验:甲、乙各取?30.0ml同浓度的盐酸,加入同一镁-铝合金粉末产生气体,有关数据列表如下:
| 实验序号 | 甲 | 乙 | 丙
合金质量/mg
255
385
510
气体体积/ml
280
336
336
|
(1)盐酸的物质的量浓度为______?mol/L,在表中可作为计算依据的是______?(填实验序号,符合要求的全部写出)
(2)据______(填实验序号)中的数据,可计算此镁-铝合金中镁与铝的物质的量之比______.
(3)在乙实验中,可以判断______
A、金属过量?B、恰好反应?C、金属不足?D、无法判断
(4)在丙实验之后,向容器中加入一定量的1.00mol/l的NaOH溶液能使合金中的铝粉恰好完全溶解,再过滤出不溶性的固体,请填下表:
| 滤液中的溶质 | NaCl | NaAlO2
对应物质的量/mol
加入NaOH溶液的体积/ml |
参考答案:(1)由表中数据可知,30.0ml同浓度的盐酸加入255mg金属,盐酸有剩余,金属完全反应.加入385mg金属与加入510mg金属生成的氢气体积一样多,故加入385mg金属,盐酸完全反应,此时生成氢气336mL,氢气的物质的量为0.336L22.4L/mol=0.015mol,根据氢元素守恒可知n(HCl)=2n(H2)=2×0.015mol=0.03mol,故盐酸的物质的量浓度为0.03mol0.03L=1mol/L.
故答案为:1mol/L;乙、丙.
(2)由表中甲、乙数据可知,甲中盐酸有剩余,金属完全反应,此时生成氢气280mL,故可以根据甲组数据计算金属的物质的量之比.
令镁、铝的物质的量分别为xmol、ymol,根据二者质量可知24x+27y=0.255,根据电子转移守恒有2x+3y=0.28L22.4L/mol×2,联立方程解得:x=0.005、y=0.005,故合金中镁与铝的物质的量之比为0.005mol:0.005mol=1:1.
故答案为:甲;1:1.
(3)甲中盐酸有剩余,255mg金属完全反应,此时生成氢气280mL,故生成336mL氢气需要金属的质量为255mg×336mL280mL=306mg,故金属有剩余.
故选:A.
(4)丙实验之后,向容器中加入一定量的1.00mol/l的NaOH溶液能使合金中的铝粉恰好完全溶解,溶液中溶质为氯化钠、偏铝酸钠.
由(2)中计算Mg、Al的物质的量可知丙中Al的物质的量为0.005mol×510mg255mg=0.01mo,根据铝元素守恒计算偏铝酸钠的物质的量为0.01mol,根据氯离子守恒可知n(NaCl)=1mol/L×0.03L=0.03mol,根据钠离子守恒可知n(NaOH)=n(NaCl)+n(NaAlO2)=0.03mol+0.01mol=0.04mol,故需要氢氧化钠溶液的体积为0.04mol1mol/L=0.04L=40mL.
故答案为:滤液中的溶质NaClNaAlO2对应物质的量/mol0.030.01加入NaOH溶液的体积/ml40
本题解析:
本题难度:一般
4、选择题 在氯化铝溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入的量(X)与溶液中沉淀物的量(Y)的关系示意图中,正确的是
[? ]
A.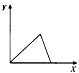
B.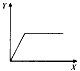
C.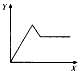
D.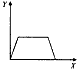
参考答案:A
本题解析:
本题难度:一般
5、选择题 下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是(?)
①NaHCO3?②Al2O3?③Al(OH)3?④Al
A.③④
B.②③④
C.①③④
D.全部
参考答案:D
本题解析:①NaHCO3属于弱酸酸式盐,既能与硫酸反应,生成CO2气体,又能与氢氧化钠反应,生成碳酸钠,故①正确;②Al2O3属于两性氧化物,既能与硫酸反应,生成Al3+离子,又能与氢氧化钠反应生成AlO2-离子,故②正确;③Al(OH)3?属于两性氢氧化物,既能与酸反应,生成Al3+离子,又能与碱反应生成AlO2-离子,故③正确;④金属铝与硫酸反应生成Al3+和氢气,与氢氧化钠反应生成AlO2-和氢气,故④正确。
本题难度:一般
|