微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
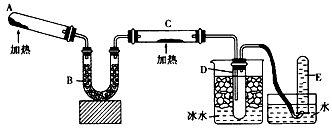
1、实验题 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中加入的物质是__________,发生反应的化学方程式是________________
(2)B中加入的物质是__________,其作用是__________________________,
(3)实验时在C中观察到的现象是_______________,发生反应的化学方程式是____________________;
(4)实验时在D中观察到的现象是_______________,D中收集到的物质是___________ ,检验该物质的方法和现象是_________________。
参考答案:(1)固体NH4Cl和Ca( OH)2;
(2)碱石灰(或CaO);除去NH3气流中的水汽
(3)黑色粉末部分逐渐变为红色;2NH3+3CuO N2+3H2O +3Cu
N2+3H2O +3Cu
(4)出现无色液体;氨水;用红色石蕊试纸检验、试纸变蓝,用无水硫酸铜检验、无水硫酸铜变蓝
本题解析:
本题难度:一般
2、填空题 工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾(?FeSO4?7H2O?).
(1)若用98%?1.84g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1:______.
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00g铁粉充分反应,收集到224mL(标准状况)气体,剩余固体质量为3.88g,测得反应后的溶液中Fe2+的物质的量为0.14mol(不含Fe3+).则该样品中Fe2+离子的氧化率为______.
(3)硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液.现取0.4g?Cu2S和CuS的混合物在酸性溶液中用40mL?0.150mol/L?KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O,6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O,反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与V?mL?0.2mol/L?(NH4)2Fe(SO4)2溶液完全反应.已知:MnO4-+Fe2++H+--Mn2++Fe3++H2O(未配平)①V的取值范围为______;②若V=35,试计算混合物中CuS的质量分数.
参考答案:(1)设浓硫酸的体积为xmL,水的体积为ymL;稀释前后硫酸的质量不变,
所以1.84x×98%1.84x+1.0y×100%=28%,解得x:y=1:4.6,故答案为:4.6;
(2)设与酸反应生成氢气需要的铁的质量为x,生成的硫酸亚铁的物质的量为y,
? Fe+2H+=Fe 2++H2 ↑
? ?56g?1mol?22.4L
? x?y?0.224L
解得x=0.56g,y=0.01mol,
与Fe3+反应需要的铁的质量为5.00g-3.88g-0.56g=0.56g,
与铁反应需要的三价铁离子的物质的量为m,生成的二价铁离子的物质的量为n,
Fe+2Fe3+=3Fe2+
56g?2mol?3mol
0.56g m?n
解得m=0.02mol,n=0.03mol,
所以原来溶液中二价铁离子的物质的量为0.14mol-0.01mol-0.03mol=0.1mol,
所以氧化率为0.02mol0.1mol+0.02mol=16.7%,
?故答案为:16.7%;
(3)①高锰酸钾的物质的量为:0.040L×0.150mol/L=0.006mol,
假设固体混合物全部为Cu2S,需要高锰酸钾的物质的量为x,
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
8? 5
x? 0.4g160g
x=0.004mol
剩余的高锰酸钾的物质的量为0.006mol-0.004mol=0.002mol,
0.002mol高锰酸钾和(NH4)2Fe(SO4)2溶液完全反应.
?MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
1mol?5mol
0.002mol?1×10-3VL×0.2mol/L
解得V=50,
假设固体混合物全部为CuS,需要高锰酸钾的物质的量为y,
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
6? 5
y?0.4g96g
y=0.005mol
剩余的高锰酸钾的物质的量为0.006mol-0.005mol=0.001mol.
0.001mol高锰酸钾和(NH4)2Fe(SO4)2溶液完全反应.
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
1mol? 5mol
0.001mol? 1×10-3VL×0.2mol/L
解得V=25,
故答案为:25<V<50;?
?②若V=35,与35mL(NH4)2Fe(SO4)2溶液完全反应需要高锰酸钾的物质的量为:
? MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
? 1mol? 5mol
0.014mol?0.035L×0.2mol/L
所以高锰酸钾的物质的量为0.0014mol,
故与固体混合物反应的高锰酸钾的物质的量为0.006mol-0.0014mol=0.0046mol,
设Cu2S的质量为xg,CuS的质量为yg,x+y=0.40g.
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
8mol? 800g
0.01xmol?xg
?6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
?6mol?480g
0.0125ymol?yg
本题解析:
本题难度:一般
3、实验题 绿矾(FeSO4・7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法
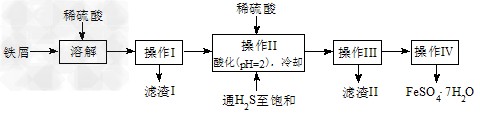
已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验制得的绿矾晶体中是否含有Fe3+的实验操作是________________________________________________________。
(2)操作II中,通入硫化氢至饱和的目的是_________________;在溶液中用硫酸酸化至pH=2的目的是_________________。
(3)操作IV的顺序依次为:_________、冷却结晶、_____________?。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;②______________________。
(5)测定绿矾产品中Fe2+含量的方法是:
a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O)。
①判断此滴定实验达到终点的方法是_______________。
②计算上述样品中FeSO4・7H2O的质量分数为___________(用小数表示,保留三位小数)
③若用上述方法测定的样品中FeSO4・7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有_____________;_____________。
参考答案:(1)取少量晶体溶于水,滴加KSCN溶液,若溶液不显现红色,表明溶液不含Fe3+
(2)除去溶液中的Sn2+离子,并防止Fe2+被氧化;防止Fe2+离子生成沉淀
(3)蒸发浓缩;过滤洗涤
(4)降低洗涤过程中FeSO4・7H2O的损耗
(5)①滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;②0.975;③样品中存在少量的杂质;样品部分被氧化
本题解析:
本题难度:一般
4、实验题 某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是 一个放热反应)。
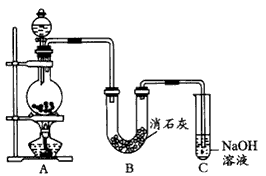
请回答下列问题:
(1)A为实验室制氯气的发生装置,反应原理为____。 某学生用12mol.L-1的浓盐酸l00mL和足量的MnO2反应制Cl2,实际得到的Cl2___6.72L(填“<”或 “>”或“=”)。
(2)漂白粉将在U形管中产生,其化学反应方程式是____。
(3)此实验所得漂白粉的有效成分偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是________。
②试判断另一个副反应是________,为避免此副反应的发生,可将装置作何改进______。
(4)C装置的作用是________。
参考答案:(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O ;<
MnCl2+Cl2↑+2H2O ;<
(2)2Cl2 +2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
(3)①冷却B装置(或将B装置放在冷水浴中);
②氯气中含有HCl,会与氢氧化钙反应[2HCl+Ca(OH)2=CaCl2+2H2O];
在A与B 之间连接一个装有饱和氯化钠溶液的洗气瓶
(4)吸收未反应完的氯气,防止污染空气
本题解析:
本题难度:一般
5、选择题 在实验室制备CH3COOC2H5时在反应试管中不需要添加的试剂是( )
A.C2H5OH
B.CH3COOH
C.浓硫酸
D.碳酸钠溶液
参考答案:D
本题解析:
本题难度:一般