微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
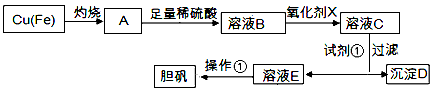
已知:
请回答:
(1)溶液B中含有的阳离子有________(填离子符号)。
(2)下列物质中最适宜做氧化剂X的是________(填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择________(填化学式)。
(4)操作①的名称是________。
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是________
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6) 沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是
________________(用离子方程式表示),还需要加入过量的盐酸,原因是________________。
参考答案:(1)Fe2+、Fe3+、 H+、Cu2+
(2)b
(3)CuO或CuCO3或Cu(OH)2
(4)蒸发结晶
(5)c
(6)2Fe3++Fe=3Fe2+;抑制Fe2+水解
本题解析:
本题难度:困难
2、实验题 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
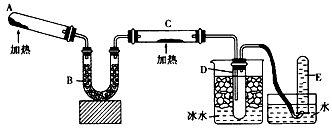
回答下列问题:
(1)A中加入的物质是__________,发生反应的化学方程式是________________
(2)B中加入的物质是__________,其作用是__________________________,
(3)实验时在C中观察到的现象是_______________,发生反应的化学方程式是____________________;
(4)实验时在D中观察到的现象是_______________,D中收集到的物质是___________ ,检验该物质的方法和现象是_________________。
参考答案:(1)固体NH4Cl和Ca( OH)2;
(2)碱石灰(或CaO);除去NH3气流中的水汽
(3)黑色粉末部分逐渐变为红色;2NH3+3CuO N2+3H2O +3Cu
N2+3H2O +3Cu
(4)出现无色液体;氨水;用红色石蕊试纸检验、试纸变蓝,用无水硫酸铜检验、无水硫酸铜变蓝
本题解析:
本题难度:一般
3、实验题 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料,黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH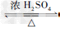 C2H5OOCCH3+H2O
C2H5OOCCH3+H2O
请根据要求回答下列问题:
(1)浓硫酸的作用是催化剂和________,欲提高乙酸的转化率,可采取的措施有________,________等。
(2)若用如下图所示的装置来制备少量乙酸乙酯,产率往往偏低,其原因可能为_______________________,_________________等。

(3)此反应以浓硫酸为催化剂,可能会造成____________________, ____________________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。

①根据表中数据,下列________(添字母)为该反应的最佳条件。
A.120?℃,4?h
B.80?℃,2?h
C.60?℃,4?h?
D.40?℃,3?h
②当反应温度达到120?℃时,反应选择性降低的原因可能为______________________。
参考答案:(1)吸水剂;增大乙醇浓度;移出生成物
(2)原料来不及反应就被蒸出;温度过高,发生了副反应;冷却效果不好,部分产物挥发(任选其二)
(3)产生了大量酸性废液,造成环境污染,部分原料碳化;催化剂重复使用困难;催化剂效果不理想(任选其二)
(4)①C;②乙醇脱水生成了乙醚
本题解析:
本题难度:一般
4、简答题 聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4?7H2O)过程如下:

(1)验证固体W焙烧后产生的气体含有SO2的方法是______.
(2)实验室制备、收集干燥的SO2,所需仪器如下.装置A产生SO2,按气流方向连接各仪器接口,顺序为a→______→______→______→______→f装置D的作用是______,装置E中NaOH溶液的作用是______.
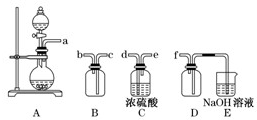
(3)制备绿矾时,向溶液X中加入过量______,充分反应后,经______操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾.
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为______.若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏______.
参考答案:(1)检验二氧化硫的一般方法是:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫.
故答案为:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫;
(2)收集二氧化硫应先干燥再收集.二氧化硫的密度比空气大,要从c口进气,最后进行尾气处理.因为二氧化硫易于氢氧化钠反应,故D的作用是安全瓶,防止倒吸;E的作用为尾气处理.故答案为:d;e;c;b;安全瓶,防止倒吸;尾气处理,防止污染;
(3)因为在烧渣中加入了硫酸和足量氧气,故溶液Y中含有Fe3+,故应先加入过量的铁粉,然后过滤.故答案为:铁粉;
(4)用pH试纸测定方法为:将试纸放在表面皿上,用洁净的玻璃棒蘸取待测液,点在试纸的中央,然后与标准比色卡对比.氢氧化铁的含量比硫酸亚铁高,若溶液Z的PH偏小,则聚铁中生成的氢氧根的含量减少,使铁的含量减少.故答案为:将试纸放到表面皿上,用洁净的玻璃棒蘸取少许待测液,滴在试纸的中央.然后与标准比色卡对比;偏低.
本题解析:
本题难度:一般
5、实验题 硬铝废料(含90%铝、2.5%镁和7.5%铜)可制取明矾 KAl(SO4)2・12H2O,某探究小组设计了下列实验。?

请回答以下问题:
(1)写出步骤②的离子方程式___________;简述用pH试纸测定溶液 pH的过程:_____________。
(2)步骤④包括三个操作环节,分别是___________、_____________、_____________。
(3)步骤⑤不直接用水洗的原因是_________________,洗涤的操作是___________。
(4)有人建议:直接将硬铝溶于稀H2SO4中,过滤:滤液中加适量K2SO4得到溶液丙,再进行后续实验。请你评价此建议的可行性_____________。
参考答案:(1)AlO2-+H++H2O=Al(OH)3↓ 或Al(OH)4-+H+=Al(OH)3↓+H2O? ;用洁净的玻璃棒沾取溶液滴到pH试纸上,待变色后,与比色卡对照,读出pH
(2)加热浓缩 ;冷却结晶 ;过滤
(3)减少产品的损失(或“减少晶体的溶解”或“明矾 在酒精中的溶解度小”等) ;往漏斗中加入洗涤剂 至浸没固体,自然流出,重复2~3次
(4)不可行 ,因为按此方法获得的溶液中还含有 Mg2+ ,最后得到的产品不纯
本题解析:
本题难度:一般