| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《物质组成与性质实验方案的设计》高频试题特训(2017年最新版)(四)
①a g绿矾的实际质量为________ g。 ②上述操作步骤的正确顺序为__________________。 ③若配制时遗漏步骤④,会使所配溶液的浓度________(填“偏高”“偏低”或“无影响”)。 ④若加蒸馏水时不慎超过刻度线,处理方法是________________;若操作步骤②时有溶液溅在容量瓶外,处理方法是________________。 参考答案:(1)AD 本题解析:(1)中B项测量溶液pH时,试纸不能润湿,否则可能产生误差;C项配制溶液不能在量筒中进行; 本题难度:一般 3、简答题 硫酸铵是一种常用的铵态氮肥.下表是硫酸铵化肥品质的主要指标.?
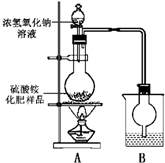 .? [观察外观] ?该硫酸铵化肥无可见机械杂质.? [实验探究] ?按如图所示装置进行实验.? (1)烧瓶内发生反应的离子方程式为:______烧杯中盛放的试剂最好是______(填“浓硫酸”、“稀硫酸”或“水”) (2)实验过程中,需往烧瓶中加入足量浓氢氧化钠溶液并充分加热的原因是______ [交流讨论] 甲同学:根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:______ 乙同学:实验装置中还存在另一个明显缺陷是:______ 经过大家充分讨论一致认为:针对甲、乙两位同学指出的实验装置中存在的明显缺陷,需改进实验装置,重新进行实验 [探究结论] 称取13.5g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重3.4g.得出探究结论为______. 参考答案:(1)硫酸铵和氢氧化钠反应生成硫酸钠、水和氨气,反应方程式为:(NH4)2SO4+2NaOH?△?.?Na2SO4+2NH3↑+2H2O,离子反应为NH4++OH-?△?.?NH3↑+H2O,烧杯中盛放的试剂是用来吸收氨气的,所以用稀硫酸, 本题解析: 本题难度:一般 4、简答题 由A和B两种盐组成的混合物,进行了下列实验: 参考答案:(1)根据质量守恒知混合物中含有:SO42-、Cu2+、CO32-、K+,这些离子可以组成两种可溶性物质是K2CO3 、CuSO4, 本题解析: 本题难度:一般 5、选择题 下列关于测定胆矾晶体里结晶水含量的实验操作,会引起测定结果偏高的是 参考答案:A 本题解析:略 本题难度:简单 | |||||||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《氧化剂和还.. | |