微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 如图是常见的一些单质及其化合物之间的转化关系图.常温常压下,D、F、K均为无色无刺激性气味的气体,C为活泼的金属单质,B是最常见的无色液体,A是有单质C在D中燃烧生成的淡黄色固体,I是焙制糕点所用的发酵粉的主要成分之一.(反应中生成的部分物质已略去)
请回答下列问题:
(1)K的分子式为______.
(2)物质A的常见用途为______(任写一种即可).
(3)反应①的离子方程式为______;反应②的化学方程式为______.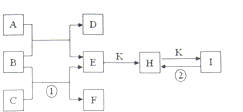
参考答案:A是有单质C在D中燃烧生成的淡黄色固体,淡黄色固体为Na2O2,则A为Na,C为O2,D为Na2O2,I是焙制糕点所用的发酵粉的主要成分之一,应为NaHCO3,B是最常见的无色液体,应为H2O,则E为NaOH,F为H2,K为CO2,H为Na2CO3,
(1)由以上分析可知K为CO2,故答案为:CO2;
(2)A为Na2O2,具有漂白性、氧化性,可与水或二氧化碳反应生成氧气,可用于供氧剂,故答案为:漂白剂或供氧剂;
(3)反应①为Na和水的反应,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,NaHCO3不稳定,加热可分解生成Na2CO3和CO2,反应的方程式为2NaHCO3?△?.?Na2CO3+CO2↑+H2O,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2NaHCO3?△?.?Na2CO3+CO2↑+H2O.
本题解析:
本题难度:一般
2、推断题 A、B、C、D均为氢化物,其分子中所含原子数依次为2、3、4、4。A、C的分子中原子个数比均为1:1,且电子总数均为18;B与C的元素种类相同;B、D的分子均含10个电子,B 与D反应得到一种一元弱碱。 请回答:
(1)A分子的电子式是____________。
(2)实验室制备D的化学方程式是____________________;检验D是否收集满的方法是________________。
(3)实验室利用稀硫酸与过氧化钡发生复分解反应来制备C,该反应的化学方程式是________________。
(4)工业上利用电解KHSO4溶液所得的产物与水反应制备C。电解KHSO4溶液时,阳极反应式是
2HSO4- -2e- = S2O82- +2H+,阴极反应是__________;已知1 mol S2O82- 与水反应得到C时转移了2mol e-,则该反应的离子方程式是___________________。
参考答案:(1)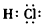
(2)2NH4Cl + Ca(OH)2 CaCl2+2NH3↑+2H2O;用湿润的红色石蕊试纸接近容器口,观察到试纸变蓝,证明已收集满
CaCl2+2NH3↑+2H2O;用湿润的红色石蕊试纸接近容器口,观察到试纸变蓝,证明已收集满
(3) BaO2+ H2SO4 = H2O2+ BaSO4↓
(4) 2H+ + 2e- = H2↑;S2O82- + 2H2O = H2O2 + 2HSO4-
本题解析:
本题难度:一般
3、填空题
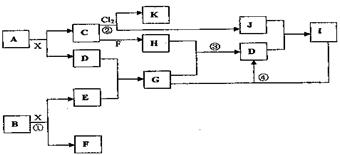
请按要求回答:
(1)写出A的化学式?H的电子式?
(2)反应①中每生成l mol F,转移电子的物质的量为?
(3)反应②进行的条件为?
(4)反应③的化学方程式为?
(5)反应④的离子方程式为?
参考答案:
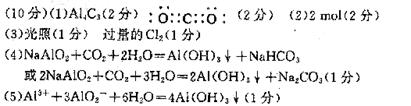
本题解析:本题是典型的无机推断题,主要考查学生元素化合物的综合应用能力,属难题。由B是一种淡黄色固体,且为化合物,不难推知B为Na2O2,再利用Na2O2的化学性质,可推知X液体为水。C和K都是由极性键构成的非极性分子,且C又是重要的能源也可推知C为CH4。A能与水反应生成CH4,则A可能为金属碳化物,再由A中有元素的质量分数为75%,可推出A为Al4C3。
本题难度:一般
4、填空题 (11分)A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。A、B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol・L―1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。 C的最高价氧化物的水化物是所有含氧酸中酸性最强的;D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的水化物的化学式为____________。
(2)A元素是_______,B元素是______,D元素是______。(写元素符号)
(3)A与D形成的原子个数比为2:1的化合物的化学式是___ _ ____,
用电子式表示它的形成过程?
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,
其离子方程式为______________________________ __________________。
参考答案:(1)三?VIIA? HClO4(2)Na? Mg? O?(3)Na2O?略
(4)Cl2 + 2OH-?="?" Cl-?+ ClO - + H2O
本题解析:略
本题难度:简单
5、推断题 A-J是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂。回答下列问题
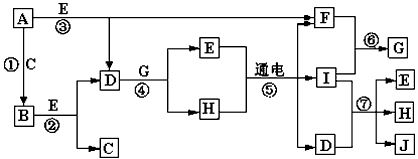
(1)B中的化学键有________(填“离子键”、“极性键”或“非极性键”) E的电子式________。
(2)写出反应⑦的离子方程式 __________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式_____________________。
(4)常温下1克F单质在足量C单质中燃烧生成稳定的液态物质E释放出142.9kJ热量,写出液态E分解的热化学方程式________________。
(5)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则在________(填“阴或阳”)极附近溶液由无色变为红色,其原因是________________。
参考答案:(1)离子键、非极性键;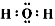 ?
?
(2)Cl2+2OH-=Cl-+ClO-+H2O
(3)4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
(4)H2O(l) = H2(g) +1/2O2(g) △H=+285.8kJ/mol
(5)阴极;在阴极由于H+得到电子产生H2,破坏了水的电离平衡,促进水继续电离,导致溶液中
c(OH-)>c(H+),溶液呈碱性,所以阴极附近溶液变为红色
本题解析:
本题难度:一般