微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 要使含Ag+、Cu2+、Mg2+、Ba2+、Al3+的溶液中各离子逐一形成沉淀析出,下列所选择的试剂和加入试剂的顺序均正确的是( )
A.H2SO4→HCl→K2S→NaOH→CO2
B.NaCl→Na2SO4→Na2S→Na2OH→CO2
C.NaCl→Na2SO4→NaS→NH3?H2O→HCl
D.Na2S→Na2SO4→NaCl→NaOH→CO2
参考答案:A.先加入硫酸,可生成硫酸银、硫酸钡沉淀,故A错误;
B.可依次生成AgCl、BaSO4、CuS、Cu(OH)2、Al(OH)3等沉淀,符合题目要求,故B正确;
C.加入硫化钠之后加入氨水可同时生成氢氧化铝和氢氧化镁沉淀,故C错误;
D.先加入硫化钠,可同时生成硫化银、硫化铜、氢氧化铝(水解生成)等沉淀,故D错误.
故选B.
本题解析:
本题难度:一般
2、实验题 (18分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气
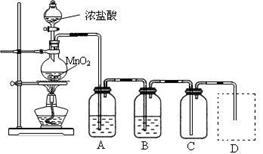
写出A、B中所盛放最佳化学试剂的名称?、?,画出虚线框内所需装置图并标明所需试剂的名称。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:?;假设③:?。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
?实验方法
| 实验现象
| 结论
|
在溶液中加
KSCN溶液
| ?
| 固体物质中有FeCl3
|
向a溶液中滴加
酸性KMnO4溶液
| KMnO4溶液紫色
不褪色
| 固体物质中不含______
|
由此得出结论:假设?成立(填序号①②③)。
Ⅲ、为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2]
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
IV、a溶液常作印刷电路铜板的腐蚀剂,写出发生反应的离子方程式?。活动小组的同学们又设计了两种从上述废液中回收Cu的方案:
方案1:设计流程图如下:

请分别写出操作①和试剂②的名称_________,_______。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,铜作________极。当观察到阴极有少量气泡产生时,停止电解,这时要回收的Cu已全部析出。
评价:方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:?。
参考答案:(共18分)
Ⅰ、饱和食盐水(1分);浓硫酸(1分); 其它合理装置也对(2分)
其它合理装置也对(2分)
Ⅱ、(1)FeCl2(1分);FeCl3和FeCl2的混合物(1分)
(2)
实验方法
实验现象
结论
在溶液中加
KSCN溶液
溶液为红色(1分)?
固体物质中有FeCl3
向a溶液中滴加
酸性KMnO4溶液
KMnO4溶液紫色
不褪色
固体物质中不含FeCl2(1分)
本题解析:略
本题难度:一般
3、实验题 某化学兴趣小组欲研究一种镁铝合金,以下是部分实验。请完成填空。
【实验一】从镁铝合金片上剪下一小块,先称重,然后投到盛有10 mL 10 mol・L-1 NaOH溶液(足量)的锥形瓶里。实验测得不同时刻气体体积如下图:?

(1) t0~t1过程中速率比t1~t2速率____(填“快”或“慢”),其主要原因是___。
(2)影响过程t1~t2速率的主要原因是:①___, ②___。
(3)欲利用此反应测定合金中铝的含量,请仿照方法①将另一种不同方法所需数据填入下表。

【实验二】向实验一的锥形瓶里滴加1 mol.L-1 HCl,使镁、铝两种元素恰好只以氯化物的形式存在。写出此过程中含铝元素的化合物所发生的离子反应方程式:____。
【实验三】取实验二的锥形瓶里的溶液10 mL,向其中滴加a mLc1mol.L-1 NaOH之后,改成滴加 c2mol.L-1HCl,所得沉淀y(mol)与试剂总体积 V(mL)间的关系如下图所示。据此,回答下列问题:
(1)图中CD段消耗盐酸的体积是AB段消耗的 NaOH溶液体积的两倍,则c1/c2=____,
(2)所加入NaOH溶液的体积a=____mL。
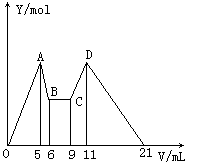
参考答案:【实验一】(1)慢 ;合金表面有氧化膜
(2)①形成原电池;②反应放热,温度升高
(3)②“测定残留固体镁的质量”或“测定反应消耗或剩余的NaOH的量”或“测定生成的NaAlO2的量” 【实验二】AlO2-+4H+=Al3+ +2H2O
【实验三】(1)2或2:1;
(2)7
本题解析:
本题难度:一般
4、选择题 只用一种试剂就可将AgNO3、KSCN、稀H2SO4、NaOH四种无色溶液区别分开,这种试剂是( )
A.BaCl2溶液
B.FeCl2溶液
C.FeCl3溶液
D.AlCl3溶液
参考答案:A.加入BaCl2溶液不能检验AgNO3和H2SO4,二者都生成沉淀,故A错误;
B.加入FeCl2溶液,不能检验KSCN和稀H2SO4,二者都无现象,故B错误;
C.加入FeCl3溶液,FeCl3溶液生成白色沉淀,KSCN溶液变为红色,稀H2SO4无现象,NaOH溶液生成红褐色沉淀,可鉴别,故C正确;
D.加入AlCl3溶液,不能检验,检验KSCN和稀H2SO4,二者都无现象,故D错误.
故选C.
本题解析:
本题难度:简单
5、选择题 实验用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体经历下列过程,Fe3+在PH=5时已完全沉淀,其分析错误的是( )

A.用18mol/L浓硫酸配制溶解所用4mol/L的稀硫酸,玻璃仪器一般只有3种
B.利用Cu(OH)2替代CuO也可调试溶液PH不影响实验结果
C.洗涤晶体:向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次
D.若要实验测定所得硫酸铜晶体中结晶水的数目要用到坩埚和坩埚钳
参考答案:A.用18mol/L浓硫酸配制溶解所用4mol/L的稀硫酸,用到量筒、烧杯、胶头滴管、玻璃棒以及容量瓶等仪器,故A错误;
B.Cu(OH)2和CuO都与溶液中H+反应,起到调节溶液PH的作用,并不引入新的杂质,故B正确;
C.固体具有吸附性,过滤时表面有可溶性物质,可向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次,可洗涤晶体,故C正确;
D.测定结晶水的含量,通过解热固体,脱去结晶水,称量质量的变化可的结晶水的个数,加热用到坩埚和坩埚钳,故D正确.
故选A.
本题解析:
本题难度:简单