微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列图示变化为吸热反应的是

参考答案:A
本题解析:A中反应物的总能量低于生成物的总能量,则反应是吸热反应;B中反应物的总能量高于生成物的总能量,反应是放热反应;C中是浓硫酸的稀释是放热过程,但属于物理变化;D中是放热反应,答案选A。
点评:该题是基础性试题的考查,主要是考查学生对常见放热反应和吸热反应的了解情况,意在巩固学生的基础知识,提高学生的应试能力。该题的关键是记住常见的放热反应和吸热反应,即一般金属和水或酸反应,酸碱中和反应,一切燃烧,大多数化合反应和置换反应,缓慢氧化反应如生锈等是放热反应。大多数分解反应,铵盐和碱反应,碳、氢气或CO作还原剂的反应等是吸热反应。
本题难度:一般
2、选择题 下列对化学反应的认识正确的是
A.化学反应必然引起物质状态的变化
B.化学反应一定有化学键的断裂和生成
C.需要加热的反应一定是吸热反应
D.若反应物的总能量高于生成物的总能量,则该反应是吸热反应
参考答案:B
本题解析:化学反应不一定引起物质状态的变化,A不正确;化学反应的实质就是旧键断裂和新键的形成,选项B正确;反应是放热反应还是吸热反应,与反应条件无关系,只与反应物和生成物总能量的相对大小有关系。如果反应物的总能量关于生成物的总能量,反应就是放热反应,反之是吸热反应,CD均不正确,答案选B。
点评:该题是基础性试题的考查,试题紧扣教材,针对性强。有利于巩固学生的基础,调动学生的学习兴趣,提高学生的应试能力和学习效率。注意有关知识的积累和总结,难度不大。
本题难度:简单
3、填空题 实验室利用如图装置进行中和热的测定。回答下列问题:
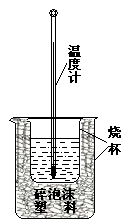
(1)该图中有两处实验用品未画出,它们是?、 ?;
(2)在操作正确的前提下提高中和热测定的准确性的关键是:?。
(3)如果用0.5mol?L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将?(填“偏大”、“偏小”、“不变”)原因是?。
参考答案:⑴环形玻璃搅拌棒、烧杯上方的泡沫塑料盖或硬纸板;
⑵提高装置的保温效果或尽量减少热量损失?⑶偏大?固体NaOH溶于水放热
本题解析:(1)由装置图可以看出:该图中有两处实验用品未画出的是用于混合溶液的环形玻璃搅拌棒;及为了防止热量散失而在烧杯上方盖的泡沫塑料盖或硬纸板。(2)在操作正确的前提下提高中和热测定的准确性的关键是提高装置的保温效果或尽量减少热量损失。(3)由于NaOH溶解在水中会放出热量,所以如果用0.5mol?L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将偏大。
本题难度:一般
4、选择题 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
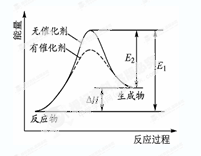
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能
参考答案:C
本题解析:A、由图可知,反应物的总能量低于生成物的总能量,所以反应是吸热反应,错误;B、催化剂改变反应的活化能,不能改变反应的焓变,错误;C、有催化剂的活化分子的能量低于无催化剂活化分子的能量,所以催化剂降低反应的活化能,正确;D、正逆反应的活化能是相同的,错误,答案选C。
本题难度:一般
5、填空题 (1)(3分)以下反应:①木炭与水制备水煤气 ②氯酸钾分解 ③炸药爆炸 ④酸与碱的中和反应 ⑤生石灰与水作用制熟石灰 ⑥ Ba(OH)2・8H2O与NH4Cl,属于放热反应的是?(填序号),写出反应⑥的化学方程式__?____。
(2)(5分)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:4HCl+O2 ?2Cl2+2H2O
?2Cl2+2H2O
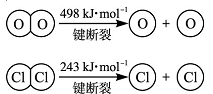
已知:i.反应A中, 4mol HCl被氧化,放出115.6 kJ的热量。
 ①H2O的电子式为__________。
①H2O的电子式为__________。
②反应A中反应物的总能量_____________ 生成物的总能量。(填“大于、小于或等于”)
③断开1 mol H―O 键与断开 1 mol H―Cl 键所需能量相差约为________kJ,H2O中H―O键比HCl中H―Cl键________(填“强”或“弱”)。
参考答案:(8分)(1)③? ④? ⑤ (1分)?
Ba(OH)2・8H2O+2NH4Cl=BaCl2 + 2NH3↑+ 10H2O 或2NH3・H2O + 8H2O (2分)
(2) ①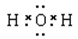 (1分) ②大于(1分)? ③31.9(2分) ?强 (1分)
(1分) ②大于(1分)? ③31.9(2分) ?强 (1分)
本题解析:(1)根据反应的特点可知,属于放热反应的是③④⑤,其余都是吸热反应。反应⑥的化学方程式是Ba(OH)2・8H2O+2NH4Cl=BaCl2 + 2NH3↑+ 10H2O。
(2)①水是含有极性键的共价化合物,所以电子式是H2O的电子式是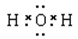 。
。
②4mol HCI被氧化,放出115.6kJ的热量,所以该反应的热化学方程式是4HCl+O2 ?2Cl2+2H2O。
?2Cl2+2H2O。
③1 mol H―O 与1 mol H―Cl的键能分别是设为x和y。因为反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以有4x+498kJ/mol-2×243KJ/mol-2×2×y=-115.6kJ/mol,解得x-y=31.9 kJ/mol,所以H2O中H―O 键比HCl中H―Cl键强。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,贴近高考,在注重对学生基础知识的巩固和训练的同时,侧重对学生基础知识的巩固和训练。有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该类试题主要是考查学生能够敏捷、准确地获取试题所给的相关信息,并与已有知识整合,在分析评价的基础上应用新信息的能力。
本题难度:一般