��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ҵ������������Ҫ�ɷ�ΪAl2O3��������Fe2O3��SiO2����ȡ��������ұ������ԭ�ϣ���ȡ�IJ����������£�

�ɹ�ѡ����Լ���ϡ���ᡢNaOH��Һ��ϡ��ˮ��CO2��
��д��������Ƶķ����и���Ӧ�Ļ�ѧ����ʽ��
��______��
��______��
��______��
��______��
�ο��𰸣�����һ������Ϊ���ᣬ���ڢٵõ���Һ�к��������ӡ������ӣ�����Ϊ�������裮��Ϊ����������Һ����ȥ�����ӣ���������ת��Ϊƫ�����������ڵõ���Һ���Լ���Ϊ������̼����ƫ�����ת��Ϊ�����������������ȷֽ����������
�������������ᷴӦ�����Ȼ�����ˮ����Ӧ����ʽΪAl2O3+6HCl�T2AlCl3+3H2O��
�����������ᷴӦ�����Ȼ�����ˮ����Ӧ����ʽΪ?Fe2O3+6HCl�T2Fe2Cl3+3H2O��
�ʴ�Ϊ��Al2O3+6HCl�T2AlCl3+3H2O��Fe2O3+6HCl�T2Fe2Cl3+3H2O��
���Ȼ������������Ʒ�Ӧ�������ǻ������������Ȼ��ƣ���Ӧ����ʽΪAlCl3+4NaOH�TNa��Al��OH��4��+3NaCl��
�Ȼ������������Ʒ�Ӧ���������������Ȼ��ƣ���Ӧ����ʽΪ?FeCl3+3NaOH�TFe��OH��3��+3NaCl��
�ʴ�Ϊ��AlCl3+4NaOH�TNa��Al��OH��4��+3NaCl��FeCl3+3NaOH�TFe��OH��3��+3NaCl��
�����ǻ�����������Һ�������̼��Ӧ����������������̼�����ƣ���Ӧ����ʽΪNa��Al��OH��4��+CO2�TAl��OH��3��+NaHCO3��
�ʴ�Ϊ��Na��Al��OH��4��+CO2�TAl��OH��3��+NaHCO3��
�������������ȷֽ�������������ˮ����Ӧ����ʽΪ2Al��OH��3?��?.?Al2O3+3H2O��
�ʴ�Ϊ��2Al��OH��3?��?.?Al2O3+3H2O��
��������Ϊ����������Һ�����ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ�����Ϊ����������Ϊ���ᣬ��ȥ��������ӣ���ƫ���������ת��Ϊ�����ӣ�����ڵõ���Һ���Լ���Ϊ��ˮ����������ת��Ϊ�����������������ȷֽ����������
��Al2O3+2NaOH+3H2O�T2Na��Al��OH��4����SiO2+2NaOH�TNa2SiO3+H2O��
��Na��Al��OH��4��+4HCl�TAlCl3+NaCl+4H2O��Na2SiO3+2HCl�TH2SiO3��+2NaCl��
��AlCl3+3NH3?H2O�TAl��OH��3��+3NH4Cl����2Al��OH��3�TAl2O3+3H2O����
���������
�����Ѷȣ�һ��
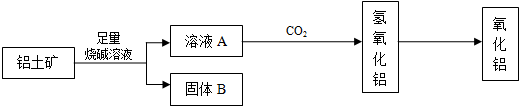
2������� ����������Ҫ�ɷ���Al2O3����RO2��Fe2O3�����ʣ�����ȡAl2O3��һ�ֹ����������£�
��1��Ԫ��Rλ�����ڱ��еĵ������ڣ�����������ϼۺ����ϼ۵ľ���ֵ��ȣ�RO2����;�У�д��1�����ɣ�______��
��2����������������ռ���Һ����Ҫ��Ӧ�����ӷ���ʽΪ
��______��
��______��
��3����ҵ��ͨ������������ͱ���ʯ������Һ��ұ������������֪�缫����Ϊ���Բ��ϣ�������ӦʽΪ______��
��4���������뽹̿�Ļ�����ڵ����и��¼��ȷ�Ӧ���Ƶ����ͷǽ�������AlN��һ����ѧ��������X����֪ÿת��3mol?e-����1.5mol������X���ɣ��˷�Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣���1����������ϼۺ����ϼ۵ľ���ֵ��ȣ�������������Ϊ4��Ԫ��Rλ�����ڱ��еĵ������ڣ�����RΪ��Ԫ�أ�RO2����SiO2������;�У��������ˡ���Ʒ���������ϡ�ʯӢ������ʯӢ�����ȣ�
�ʴ�Ϊ���������ˡ���Ʒ���������ϡ�ʯӢ������ʯӢ�����ȣ�
��2����������������ռ���Һ��Al2O3��SiO2���������Ʒ�Ӧ�������������������Ʒ�Ӧ��
�����������������Ʒ�Ӧ����ƫ�����ƺ�ˮ����Ӧ���ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O��?
�ڶ�������������������Һ��Ӧ���ɹ����ƺ�ˮ�����ӷ���ʽΪSiO2+2OH-=SiO32-+H2O��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��?
?��3������������ͱ���ʯ������Һ������������������Ԫ���������ϱ������������������缫��ӦʽΪ2O2--4e-=O2����
�ʴ�Ϊ��2O2--4e-=O2����?
��4������Ԫ���غ��֪XΪ̼��������ɵ���ת���غ㣬�ɵ���X��C�Ļ��ϼ�Ϊ3mol1.5mol=2������X��CO�����Ը÷�Ӧ�Ļ�ѧ����ʽΪAl2O3+N2+3C?����?.??2AlN+3CO��
�ʴ�Ϊ��Al2O3+N2+3C?����?.??2AlN+3CO��
���������
�����Ѷȣ�һ��
3��ѡ���� Ҫ��ȥ�Ȼ������������Ȼ����������е���
A��ͨ������
B������KSCN ��Һ
C������ͭ��
D����������
�ο��𰸣�A
����������������Ļ����������
���ӵĹ����в��������µ����ʣ��ʿ�����Һ��ͨ���������Ȼ�������������Ϊ�Ȼ�������ΪA����������ѡ���е����ʾ������Ȼ�����Ӧ���ų�
�����Ѷȣ�һ��
4��ѡ���� �������ʷ�Ӧ��һ���У�3�������ɵ���
[ ? ]
�ٹ�����Fe��Cl2��Ӧ����Fe�����ϡH2SO4��Ӧ���������м���KNO3��
��Fe��Fe2O3�Ļ��������������
A����?
B���٢�
C���٢�?
D��ȫ��
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� ����˵����ȷ����(? )
A��ͭ������FeCl3��Һ���ɵ�ԭ����У�Cu +2 Fe3+ = Cu2+ + 2Fe2+
B�����϶�пʱ��������6.5gп����Һ�м���Zn2+��Ϊ0.1mol
C���ڷ�Ӧ:4CuS + 5O2 = 2Cu2O + 4SO2��CuS�������������ǻ�ԭ��
D��������ŨH2SO4���ȷ�Ӧ�ɲ���SO2��CO2����
�ο��𰸣�CD
���������ͭ������FeCl3��Һ���ɵ�ԭ����У�����ͭ���ã�������������˷�Ӧԭ����Fe +2 Fe3+ = 3Fe 2+?��A����Ƴ����Ժ��е�ƽ������ӵ���Һ��Ϊ���Һ�ģ������Ǵ��ƽ�����������϶�пʱ��������6.5gп����Һ�е�Zn2+�����٣�B�����ڷ�Ӧ4CuS + 5O2 = 2Cu2O + 4SO2��CuS��Cu���ϼ۽��ͣ���S�Ļ��ϼ����ߣ����CuS�������������ǻ�ԭ����C��ȷ���������е���Fe��C�����߾������ڼ��������º�Ũ���ᷴӦ�������SO2��CO2���������D��ȷ����ѡCD��
�����Ѷȣ�һ��