��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�����ܱ������У����淴ӦA(s) B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
A������B��״ֻ̬��Ϊ��̬��Һ̬
B��ƽ��ʱ����λʱ����n(A)���ĩsn(C)����=1�s1
C������������䣬��ƽ����ϵ�м���B��ƽ��������淴Ӧ�����ƶ�
D������ʼʱ�������м���1molB��1molC���ﵽƽ��ʱ�ų�����Q
2��ѡ���� ���з�Ӧ��ϵ�У������ڿ��淴Ӧ����
A��Cl2�ܽ���ˮ
B�������ܽ���ˮ
C����ҵ�ϳɰ�
D��ˮ�������H2��O2��H2��O2��ȼ������H2O
3������� T��ʱ���мף��������ܱ������������������Ϊ1L�������������Ϊ2L���ֱ���ס����������м���
6mol A��3mol B��������Ӧ���£� 3A��g����b B��g��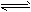 3C��g����2D��g����(bΪ3��������) ��
3C��g����2D��g����(bΪ3��������) ��
4min��������ڵķ�Ӧ�ﵽƽ�⣬A��Ũ��Ϊ2.4mol/L��B��Ũ��Ϊ1.8mol/L��t min���������ڵķ�Ӧ�ﵽƽ�⣬B��Ũ��Ϊ0.8mol/L�������������Ϣ�ش��������⣺
��1���������з�Ӧ��ƽ������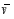 ��B����______________��
��B����______________��
��2�����¶�T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ__________________�� ���±����ݿ�֪�÷�ӦΪ______________������ȡ������ȡ�����Ӧ����ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±�
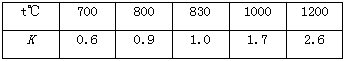
��3��T��ʱ������һ�����������ͬ�ı������У�Ϊ�˴ﵽƽ��ʱB��Ũ����ȻΪ0.8mol/L����ʼʱ����������м���C��D�����ʵ����ֱ�Ϊ3mol��2mol���������A��B�����ʵ����ֱ���___________��
___________��
4������� ��9�֣���4molSO2��2molO2�Ļ��������������ɱ�ĺ�ѹ�����У���һ�������·������·�Ӧ2SO2(g)+ O2(g) ?2SO3(g)? ��H<0���÷�Ӧ��ƽ��ʱ,������������ʵ���Ϊ4.2mol���Իش�
?2SO3(g)? ��H<0���÷�Ӧ��ƽ��ʱ,������������ʵ���Ϊ4.2mol���Իش�
��1���ڸ�ƽ��ʱ��n(SO3)=?mol ?
��2������ʼʱ����1.2molSO2��0.6molO2��xmolSO3���ﵽƽ��ʱ�������������������ƽ��״̬��ͬ����x��ȡֵ��Χ��?
��3������Ӧ��ʼʱv(��)> v(��),�ﵽ����ƽ��״̬ʱ,����������ʵ�����Ϊ4.2mol������ʼʱn(SO3)��ȡֵ��Χ��?
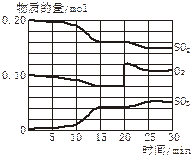
��4������Ӧ������SO2��O2��SO3���ʵ����仯��ͼ��ʾ����Ӧ������20minʱ�����߷����仯��ԭ����______________________�������ֱ����10 min��15 min�����߱仯��ԭ�������_________(��д���)��
A�����˴���
B�����������
C�������¶�
D������SO3�����ʵ���
5��ѡ���� �������ݻ����¶���ȫ��ͬ�ļס�������ܱ������У��ֱ�Ͷ��1 mol N2,3 mol H2��2 mol N2,6 mol H2��һ��ʱ��ﵽƽ���������N2��ռ�������ΪM%������N2��ռ�������ΪN%����M��N��ȷ�Ĺ�ϵ��(? )
A��M>N
B��M<N
C��M="N"
D�����Ƚ�